Clear Sky Science · de
Eine automatisierte Bildanalyse‑Pipeline für Weitfeld‑optische Redoxbildgebung von patientenabgeleiteten Krebs‑Organoiden
Warum diese Krebs‑Bildgebungsstudie wichtig ist
Das passende Medikament für den Krebs jeder einzelnen Person zu finden, ist nach wie vor ein langsamer, zufallsbasierter Prozess. Diese Studie geht das Problem an, indem sie winzige, im Labor aus Patientenmaterial gezüchtete Tumoren — sogenannte Organoide — mit einer schnellen, kamera‑basierten Methode kombiniert, um zu beobachten, wie sich deren Energieverbrauch ändert, wenn Medikamente zugegeben werden. Die Autorinnen und Autoren zeigen, wie eine neue automatisierte Computer‑Pipeline große Stapel von Mikroskopbildern durchsieben, Hunderte von Organoiden über mehrere Tage verfolgen und aufdecken kann, welche Behandlungen wirken — und zwar deutlich schneller und zuverlässiger als manuell möglich.
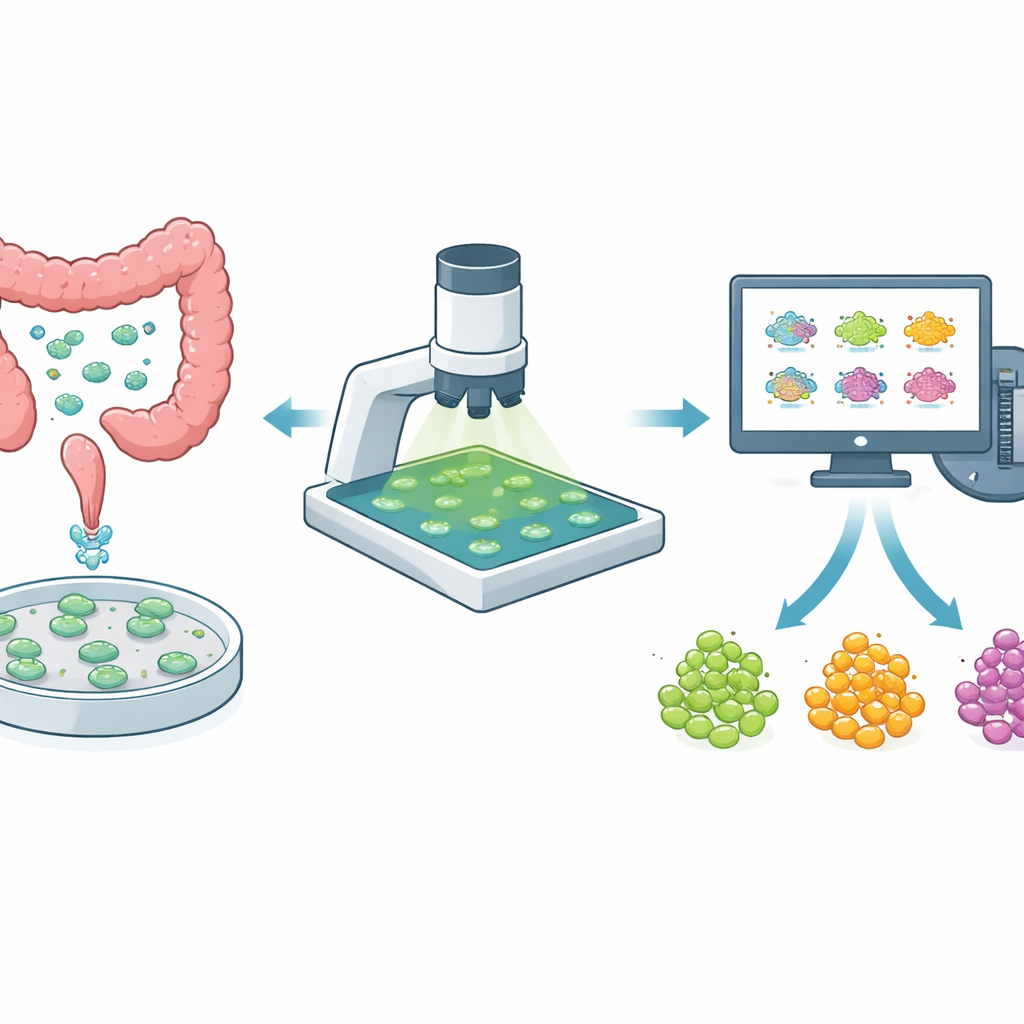
Mini‑Tumoren in einer Schale als Testfelder
Anstatt sich nur auf in flachen Schichten gezüchtete Krebszellen zu stützen, verwenden Forschende zunehmend dreidimensionale Organoide, die direkt aus dem Tumor einer Patientin oder eines Patienten gewonnen werden. Diese Mini‑Tumoren bewahren die Mischung aus Zelltypen und die versteckten Nester von medikamentenresistenten Zellen besser als flache Kulturen. Besonders beim kolorektalen Krebs, bei dem Tumoren von Person zu Person und sogar innerhalb desselben Patienten stark variieren, sind Organoide ein leistungsfähiges Mittel, um die Wirksamkeit neuer und etablierter Medikamente zu testen. Damit solche Organoid‑Tests klinisch nützlich sind, müssen sie jedoch schonend sein — so dass dasselbe Organoid über die Zeit beobachtet werden kann — und schnell genug, um viele Wirkstoffe und Dosen zu screenen.
Den Tumor‑„Kraftstoffverbrauch" mit Licht beobachten
Das Team verwendet eine Technik namens optische Redoxbildgebung, die auf dem schwachen natürlichen Leuchten von Molekülen in Zellen beruht, die an der Energieproduktion beteiligt sind. Durch das Anregen mit bestimmten Lichtfarben und das Erfassen des emittierten Leuchtens kann ein einfaches Weitfeldmikroskop eine Karte erstellen, wie „oxidiert“ oder „reduziert“ jedes Organoid ist — ein Schnappschuss seines Stoffwechselzustands. Im Gegensatz zu aufwendigeren High‑End‑Mikroskopen nutzt dieser Aufbau Standardkomponenten, die viele Labore bereits besitzen, und ist daher relativ leicht übernehmbar. Veränderungen in diesem Redoxsignal treten oft früher auf als Veränderungen in Organoidgröße oder Zelltod und dienen somit als Frühindikator dafür, ob ein Medikament wirkt oder versagt.
Rohbilder in verlässliche Zahlen verwandeln
Bislang bedeutete die Analyse dieser Bilder, dass eine Person jedes Organoid per Hand umzeichnen, Hintergrundbereiche nach Augenmaß auswählen und dann versuchen musste nachzuverfolgen, welches Organoid über mehrere Tage welches war. Dieser langsame, fehleranfällige Ansatz ist für groß angelegte Wirkstoffscreenings ungeeignet. Die Autorinnen und Autoren haben eine End‑to‑End‑automatisierte Pipeline entwickelt, die drei anspruchsvolle Aufgaben übernimmt: jedes Organoid präzise vom Umfeld zu trennen, jedem eine konsistente Identität über mehrere Tage zuzuteilen und das Hintergrundsignal so zu schätzen, dass menschliche Verzerrungen vermieden werden. Sie passten ein bestehendes KI‑Werkzeug (Cellpose) so an, dass es Organoide zuverlässig erkennt, selbst wenn diese in Form, Größe und Schärfe variieren, und bauten einen Tracking‑Algorithmus, der Bilder verschiedener Tage ausrichtet und Organoide anhand von Form‑ und Lageüberlappungen zuordnet.
Fokussierung auf den aktivsten Rand
Organoide weisen verschiedene Zonen auf: einen toten oder sterbenden Kern, eine ruhige Mittenschicht und einen lebhaften äußeren Rand, an dem Zellen aktiv wachsen und oft am empfindlichsten auf Therapien reagieren. Die Pipeline schneidet automatisch diesen dünnen Außenring — die sogenannte Leading Edge — für jedes Organoid aus und berechnet dessen Redox‑Wert. Indem sie die Leading Edge desselben Organoids über drei Tage Behandlung mit unterschiedlichen Dosen des Medikaments Romidepsin verfolgt, kann die Software subtile Stoffwechselverschiebungen erkennen. Die Autorinnen und Autoren zeigen, dass dieses Organoid‑für‑Organoid‑Tracking die Variabilität verringert im Vergleich zum Zusammenfassen aller Organoide und dadurch die statistische Aussagekraft erhöht, um Arzneimittelwirkungen zu erkennen, selbst wenn die Antworten zwischen Mini‑Tumoren variieren.
Schnellere, robustere Erkenntnisse zur Arzneimittelantwort
Die Forschenden testeten ihre Pipeline an Bildern von zwei verschiedenen Mikroskopsystemen und fanden, dass die automatisierten Umrisse denen von Expertinnen und Experten sehr nahekamen und das Tracking in über 94 Prozent der Fälle mit manueller Nachverfolgung übereinstimmte. Beim Vergleich gesamter Wirkstoffantwort‑Maße erreichte die automatisierte Methode die Sensitivität des manuellen Ansatzes, während die Analysezeit um mehr als das Hundertfache reduziert wurde — von vielen Stunden menschlicher Arbeit auf nur wenige Minuten Computerverarbeitung. Für Labore, die mit patientenabgeleiteten Organoiden arbeiten, bedeutet das, dass sie realistisch große Bildbestände analysieren und herausfinden können, wie jedes Mini‑Tumor auf Behandlungen reagiert. Langfristig könnte eine solche automatisierte Analyse dazu beitragen, organoidbasierte Wirkstofftests näher an die Klinik zu bringen und eine persönlichere und effektivere Krebsbehandlung zu unterstützen.
Zitation: Hsu, A., Samimi, K., Gillette, A.A. et al. An automated image analysis pipeline for wide-field optical redox imaging of patient-derived cancer organoids. Sci Rep 16, 9757 (2026). https://doi.org/10.1038/s41598-026-40249-4
Schlüsselwörter: kolorektales Karzinom, patientenabgeleitete Organoide, optische Redoxbildgebung, automatisierte Bildanalyse, Arzneimittelantwort