Clear Sky Science · de
Molekulare Evolution und Diversität der RNA-abhängigen RNA-Polymerase von Norovirus
Warum Magen-Darm-Erkrankungen uns immer wieder überraschen
Norovirus ist das berüchtigte „Magen-Darm-Grippe“-Virus, das innerhalb weniger Tage Kreuzfahrtschiffe, Schulen und Krankenhäuser lahmlegen kann. Es breitet sich leicht aus, macht jährlich Hunderte Millionen Menschen krank und bringt ständig neue Varianten hervor. Diese Studie blickt unter die Haube dieser Evolution und konzentriert sich auf ein einzelnes virales Enzym — eine interne „Kopiermaschine“ namens RNA-Polymerase — um zu untersuchen, wie es sich im Laufe der Zeit verändert und wie stabil es wirklich ist. Das Verständnis dieses verborgenen Triebs der Veränderung könnte helfen zu erklären, warum bestimmte Norovirus-Stämme global dominieren, und die Entwicklung künftiger antiviraler Wirkstoffe leiten.
Die innere Kopiermaschine des Virus
Norovirus trägt sein genetisches Material als RNA und ist auf ein Enzym angewiesen, die RNA-abhängige RNA-Polymerase, um diese RNA innerhalb infizierter Zellen zu kopieren. Dieses Enzym, etwa 510 Bausteine lang, ähnelt einer gekrümmten Hand mit Fingern, Handfläche und Daumen und bildet einen Kanal, durch den RNA und neue Bausteine hindurchlaufen. In dieser Struktur liegen sieben winzige „Hotspots“, die über die Stämme hinweg nahezu identisch sind; diese Bereiche führen die chemische Kernarbeit des Genomkopierens aus. Weil die Polymerase für die Replikation des Virus essenziell ist, können schon kleine Störungen in diesen Hotspots katastrophal für das Virus sein, sodass die Evolution diese Regionen äußerst sorgfältig bewahrt.
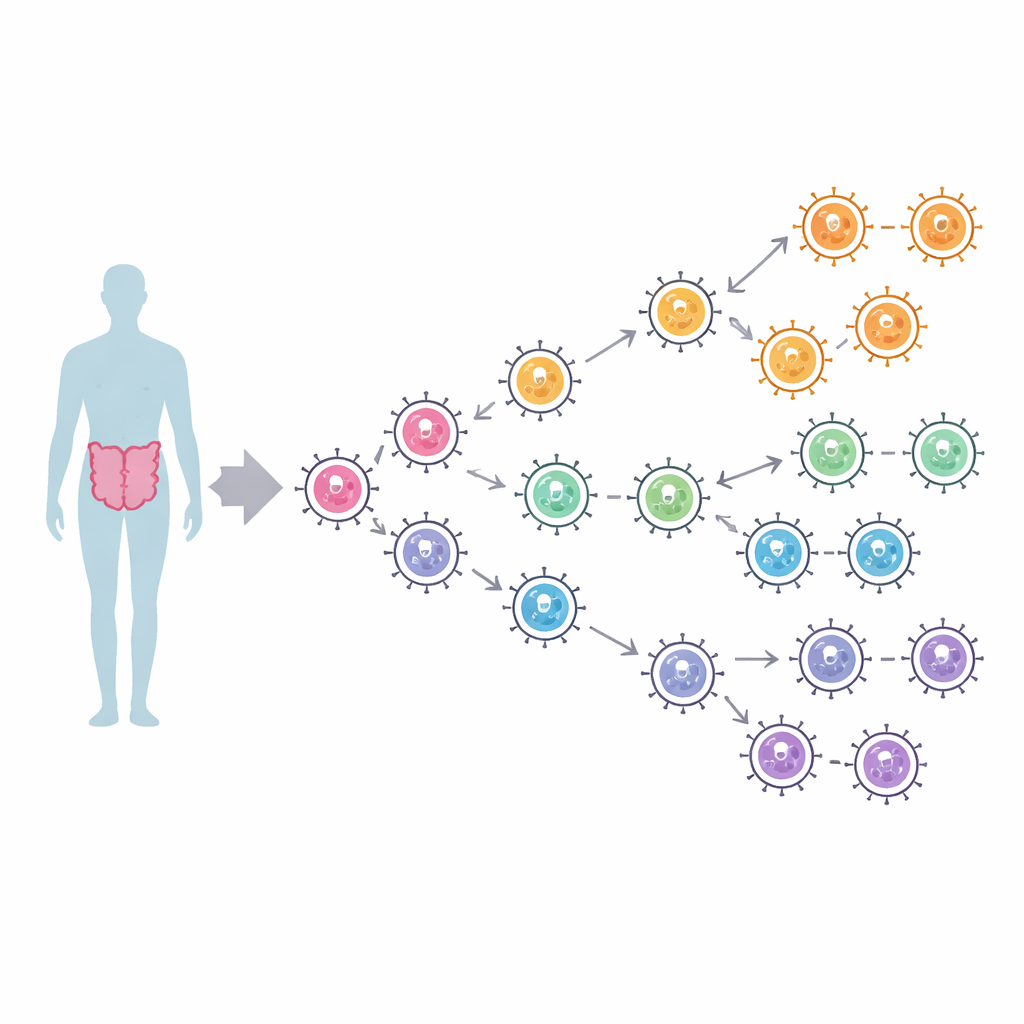
Hunderte Stämme, einige wenige Schlüssel-Familien
Die Forschenden sammelten 1.094 vollständige Polymerase-Sequenzen aus zwei großen humanen Norovirus-Gruppen, GI und GII, die weltweit zwischen 1972 und 2024 erhoben wurden. Mithilfe computergestützter Stammbaumanalysen, die Probenzeitpunkte und -orte einbeziehen, verfolgten sie, wie sich diese Enzyme über fast vier Jahrhunderte verzweigten. GI-Polymerasen gliederten sich in drei Hauptlinien, deren Aufspaltung vermutlich bereits im 17. Jahrhundert begann, während GII-Polymerasen vier Linien bildeten, darunter einen eigenen Zweig für einen Typ, der als P16 bekannt ist. Moderne Infektionen werden von zwei GII-Polymerase-Typen dominiert, P16 und P31, die historisch mit dem langanhaltenden pandemischen Kapsid-Genotyp GII.4 verknüpft sind. Trotz globaler Verbreitung zeigten die Stammbäume kaum geografische Cluster — Stämme von verschiedenen Kontinenten mischen sich — was darauf hindeutet, dass Norovirus sich schnell weltweit verbreitet, ohne auf bestimmte Regionen beschränkt zu bleiben.
Langsame, stetige Veränderungen mit gut geschützten Kernen
Durch den Vergleich der Aminosäurebausteine an jeder Position in der Polymerase katalogisierte das Team Tausende Veränderungen zwischen den Typen. Sie fanden deutlich weniger Veränderungen in GI als in GII, was teilweise die geringere Anzahl verfügbarer Sequenzen widerspiegelt, aber ein klares Muster zeigte sich: Die sieben konservierten Hotspots und die nahegelegene RNA-Bindungsstelle blieben nahezu unberührt. Wenn dort Substitutionen auftraten, handelte es sich meist um milde Austausche zwischen chemisch ähnlichen Bausteinen, was darauf hindeutet, dass das Enzym in diesen kritischen Zonen nur sehr sanfte Anpassungen toleriert. Die häufigen Veränderungen konzentrierten sich größtenteils in den „Fingern“ und anderen äußeren Regionen des Enzyms, fernab der zentralen chemischen Bereiche. Einige Positionen zeigten sogar reversible Hin- und Her-Wechsel zwischen verschiedenen Polymerase-Typen, ein Zeichen konvergenter Evolution, bei der nicht verwandte Stämme auf ähnliche Lösungen stoßen.
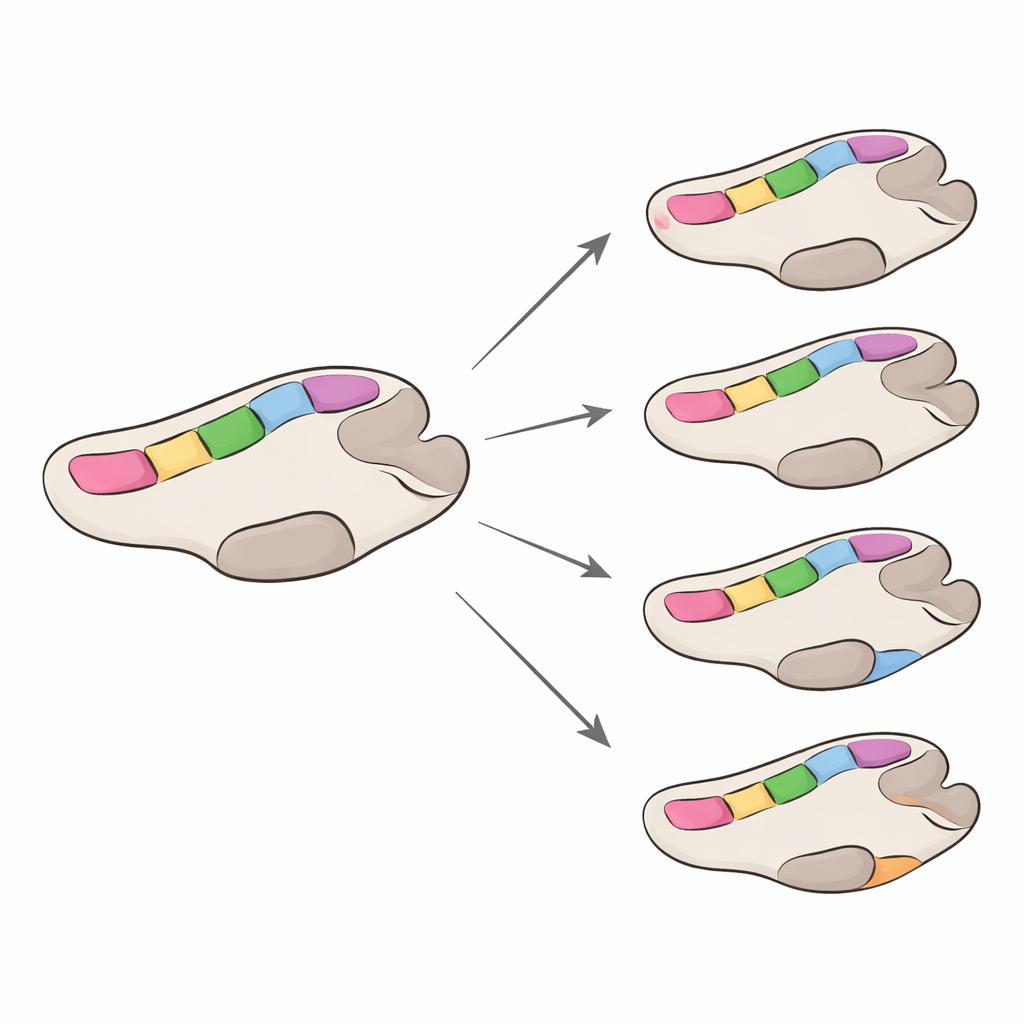
Verschiedene Geschwindigkeiten für verschiedene Virenfamilien
Das Team schätzte dann, wie schnell die Polymerase evolviert, wobei sie sich auf Veränderungen konzentrierten, die Aminosäuren verändern und daher eher die Funktion beeinflussen. Insgesamt veränderten sich GII-Polymerasen etwa viermal so schnell wie GI-Polymerasen, obwohl beide langsamer waren als das äußere Hüllprotein des Norovirus, das dafür bekannt ist, sich rasch zu verändern, um der Immunabwehr zu entgehen. Innerhalb jeder Gruppe entwickelten sich manche Polymerase-Typen etwas schneller als andere, die Unterschiede waren jedoch moderat. Wichtig ist: Die meisten Positionen im Enzym unterlagen starkem „purifizierendem“ Druck — schädliche Mutationen wurden ausgesiebt — während nur eine Handvoll Stellen Hinweise auf positive Selektion zeigte. Wenn diese positiv selektierten Stellen in dreidimensionale Modelle des Enzyms eingezeichnet wurden, lagen sie fast ausnahmslos außerhalb der am stärksten konservierten Hotspots, wenngleich einige nahe genug lagen, um die RNA-Bindung oder die Bewegungsabläufe bei der Kopie feinzujustieren.
Was das für künftige Ausbrüche und Behandlungen bedeutet
Zusammengefasst malen diese Befunde das Bild einer überraschend stabilen Polymerase-Kernstruktur, umgeben von flexibleren Regionen, die graduelle Anpassung ermöglichen. GII-Polymerasen, insbesondere jene, die mit historisch pandemischen Stämmen verbunden sind, evolvieren etwas schneller, was diesen Viren helfen könnte, mit verändernden Wirten und konkurrierenden Varianten Schritt zu halten. Dennoch spricht die tiefe Konservierung zentraler Funktionsbereiche über Jahrhunderte dafür, dass dieses Enzym ein vielversprechendes, festes Ziel für antivirale Wirkstoffe ist: Wird die Kern-Kopiermaschinerie gestört, hat das Virus kaum Spielraum zur Flucht, ohne sich selbst schwer zu schädigen. Für Nicht-Spezialisten lautet die Schlussfolgerung: Während die äußeren Flächen des Norovirus weiterhin variieren und neue Ausbrüche damit unvermeidlich bleiben, ist der innere Motor, der diese Veränderungen antreibt, sowohl eng konserviert als auch wissenschaftlich greifbar — und bietet damit ein stabiles Ziel für künftige Therapien.
Zitation: Flint, A., Jawad, M. & Nasheri, N. Molecular evolution and diversity of the norovirus RNA-dependent RNA polymerase. Sci Rep 16, 9042 (2026). https://doi.org/10.1038/s41598-026-40248-5
Schlüsselwörter: Norovirus, virale Evolution, RNA-Polymerase, antivirale Ziele, molekulare Epidemiologie