Clear Sky Science · de
Eine modulare Plattform für automatisierte Organoidkultur und Langzeitbildgebung
Mini‑Organe auf einem Chip
Stellen Sie sich vor, Sie könnten winzige, im Labor gezüchtete Versionen menschlicher Organe in Echtzeit beobachten, wie einen Zeitlupenfilm davon, wie Gewebe wachsen, krank werden oder auf Medikamente reagieren. Das ist das Versprechen von Organoiden – dreidimensionale Zellverbände, die echte Organe nachahmen. Dieser Artikel beschreibt eine neue Tischplattform, die Gehirn‑Organoide automatisch am Leben erhält, versorgt und über Tage hinweg überwacht, ohne einen sperrigen Inkubator zu benötigen. Sie öffnet die Tür zu verlässlicheren Krankheitsmodellen, intelligenteren Arzneimitteltests und schließlich zu stärker personalisierter Medizin.
Warum das Wachstum von Mini‑Organen so schwierig ist
Organoide sind starke Werkzeuge zur Erforschung von Gehirn, Darm, Niere und mehr, weil sie viele der Strukturen und Zelltypen echter Organe nachbilden. Ihre Pflege ist jedoch überraschend knifflig. Übliche Methoden beruhen darauf, dass Personen manuell die Nährflüssigkeit wechseln und Gefäße auf Schüttelplattformen in warmen, feuchten Inkubatoren platzieren. Dieses Vorgehen ist arbeitsintensiv und kann von Labor zu Labor variieren. Schlimmer noch: Die enge, feuchte Umgebung in einem Inkubator erschwert das Platzieren von Kameras und Elektronik in der Nähe, sodass Forschende normalerweise nicht kontinuierlich beobachten können, wie sich das Gewebe über die Zeit verändert. Bestehende mikrofluidische Systeme verbessern die Kontrolle der Nährflüssigkeit, befinden sich aber meist weiterhin in denselben Inkubatoren, was die Langzeitbildgebung einschränkt.
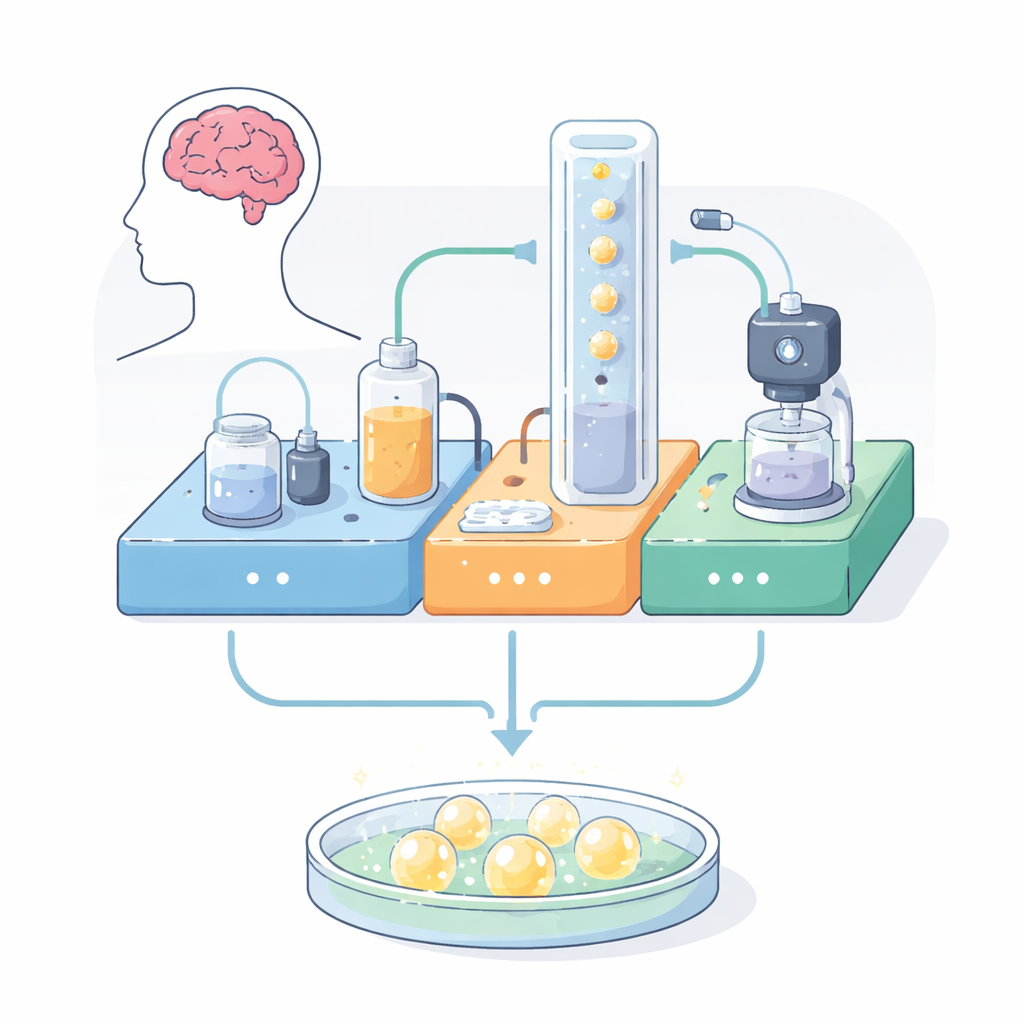
Ein autarkes Lebenserhaltungssystem
Die Autoren entwickelten eine modulare Plattform, die drei Funktionen zusammenführt, die sonst auf verschiedene Geräte verteilt sind: automatisierte Nährstoffzufuhr, Lebendbildgebung und Umweltkontrolle. Alles ist auf einer kompakten, gelochten Metallplatte montiert und nutzt 3D‑gedruckte Halter sowie handelsübliche Bauteile. Ein Modul pumpt warme Nährlösung in einem geschlossenen Kreislauf und führt sie an den Organoiden vorbei, während Verunreinigungen herausgefiltert werden. Ein zweites Modul regelt konstant Temperatur und Säuregrad und nutzt einen Heizer und kontrollierte Kohlendioxid‑Blasen, um die Bedingungen nahe an denen im Körper zu halten. Ein drittes Modul positioniert ein kleines digitales Mikroskop nahe der Kulturkammer, nimmt Hellfeld‑ und Fluoreszenzaufnahmen auf und erkennt sogar gängige grün und rot fluoreszierende Marker in den Zellen. Alle drei Module kommunizieren über einfache Elektronik miteinander, sodass lange, unbeaufsichtigte Versuchsreihen möglich sind.
Der vertikale Chip, der alles zeigt
Im Zentrum des Systems steht eine kundenspezifische Kulturkammer: ein klarer Silikonbrunnen, der auf einem Glasobjektträger aufgebracht ist. Anders als traditionelle Flachplatten ist dieser Chip vertikal montiert. Diese ungewöhnliche Ausrichtung erlaubt es Forschenden, zu beobachten, wie die Flüssigkeit tatsächlich um jedes Organoid fließt, anstatt nur eine Draufsicht zu sehen. Der Brunnen enthält Ein‑ und Auslasskanäle, die hoch genug platziert sind, um ein Auswaschen der Proben zu verhindern, und die Öffnung ist groß genug, um Organoide mit einer Standardpipette zu laden und gleichzeitig Gasaustausch zu ermöglichen. Der Chip lässt sich in weniger als einem Tag mithilfe 3D‑gedruckter Formen und günstiger Materialien herstellen und kann als einzelner großer Brunnen oder als Multiwell‑Versionen ausgeführt werden, die mehrere Organoide in Reihe oder parallel aufnehmen. Diese Flexibilität erleichtert das Hochskalieren von Experimenten oder den Vergleich unterschiedlicher Strömungsmuster.
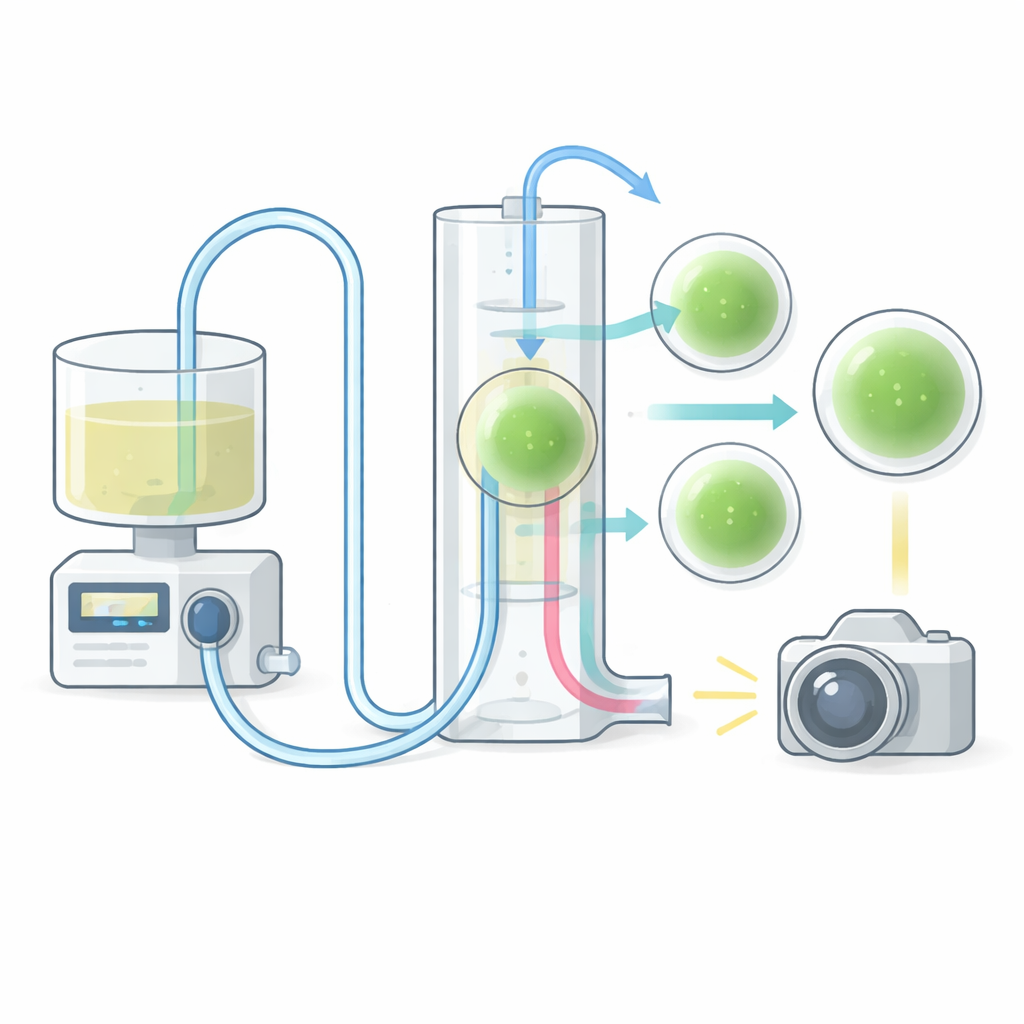
Bleiben die Mini‑Gehirne gesund?
Um zu prüfen, ob die Plattform tatsächlich lebendes Gewebe unterstützt, züchtete das Team Maus‑Gehirn‑Organoide und verteilte sie auf Standard‑Inkubatorbedingungen und das neue Gerät. Nach sechs Tagen färbten sie die Organoide mit einem Farbstoff, der intakte Zellmembranen markiert, und untersuchten ihre Struktur mit Antikörpern gegen ein neuronenspezifisches Protein. Die auf der Plattform kultivierten Organoide waren hinsichtlich Lebensfähigkeit und struktureller Organisation genauso gut wie die im Inkubator, über alle Chip‑Designs hinweg. Außerdem bestimmten sie Schlüsselnährstoffe und Salze – etwa Glukose, Natrium, Kalium, Calcium und Chlorid – in der Kulturflüssigkeit. Die Konzentrationen blieben stabil und statistisch nicht von den Inkubator‑Kontrollen zu unterscheiden, was zeigt, dass der automatisierte Fluss das Gewebe nicht belastete. Zeitrafferaufnahmen zeigten ein stetiges Wachstum der Organoidgröße, und die Multiwell‑Chips verringerten unerwünschtes Verschmelzen benachbarter Organoide, ein häufiges Problem herkömmlicher Kulturen.
Nährstoffe in Echtzeit verfolgen
Die Plattform ist nicht nur ein Lebenserhaltungssystem; sie ist auch ein Fenster dafür, wie Moleküle durch 3D‑Gewebe wandern. In einem Experiment gaben die Forschenden einen fluoreszierenden Farbstoff als Puls durch den Chip und verfolgten dessen Aufnahme in verschiedene Regionen eines Organoids über mehrere Minuten. Die resultierenden Helligkeitsmuster stimmten mit Computersimulationen von Strömung und Diffusion überein und bestätigten, dass das Gerät dynamische Transportprozesse mit feiner Auflösung erfassen kann. Diese Fähigkeit, reale Filme von Farbstoff‑ oder Arzneimittelpenetration mit Vorhersagemodellen zu verbinden, könnte helfen, die Verabreichung von Therapien und das Anlegen musterbildender Signale in entwicklungsähnlichen Experimenten zu optimieren.
Was das für die Zukunft bedeutet
Kurz gesagt liefert diese Arbeit einen kompakten, erschwinglichen „Mini‑Inkubator auf einer Platte“, der Gehirn‑Organoide automatisch wachsen lassen kann, während er sie filmt und ihre Umgebung misst. Er überwindet den üblichen Zielkonflikt zwischen dem Erhalt einer realistischen, gut kontrollierten Gewebeumgebung und der Möglichkeit, hineinzusehen. Während die aktuelle Studie sich auf Mausgewebe über etwa eine Woche konzentriert, ließe sich derselbe Ansatz auf menschliche Organoide und längere Experimente ausdehnen und so eine treuere und aufschlussreichere Testumgebung für die Erforschung der Gehirnentwicklung, neurologischer Erkrankungen und neuer Medikamente bieten.
Zitation: Torres-Montoya, S., Hernandez, S., Seiler, S.T. et al. A modular platform for automated organoid culture and longitudinal imaging. Sci Rep 16, 9717 (2026). https://doi.org/10.1038/s41598-026-40231-0
Schlüsselwörter: Organoide, Gehirnmodelle, Mikrofluidik, Lebendzell‑Bildgebung, Automatisierte Zellkultur