Clear Sky Science · de
Caveolin-1 moduliert die Notch-Transkriptionsaktivität während der in vitro Reifung respiratorischer mehrflimmeriger Zellen
Warum die winzigen Härchen in Ihren Atemwegen wichtig sind
Jeder Atemzug spült Staub, Mikroben und Schadstoffe in Ihre Atemwege. Eine dünne Zellschicht wirkt wie ein selbstreinigendes Förderband und nutzt schlagende, haarähnliche Strukturen, um Schleim und eingeschlossene Partikel aus der Lunge zu befördern. Diese Studie untersucht, wie dieses Förderband aufgebaut und erhalten wird, mit Fokus auf ein wenig bekanntes Membranprotein namens Caveolin-1 und seine Zusammenarbeit mit einem wichtigen zellulären Schicksalsumschalter. Das Verständnis dieser Partnerschaft könnte Forschern künftig helfen, bessere Therapien für chronische Lungenerkrankungen zu entwickeln, bei denen das Epithel der Atemwege geschädigt oder aus dem Gleichgewicht geraten ist.
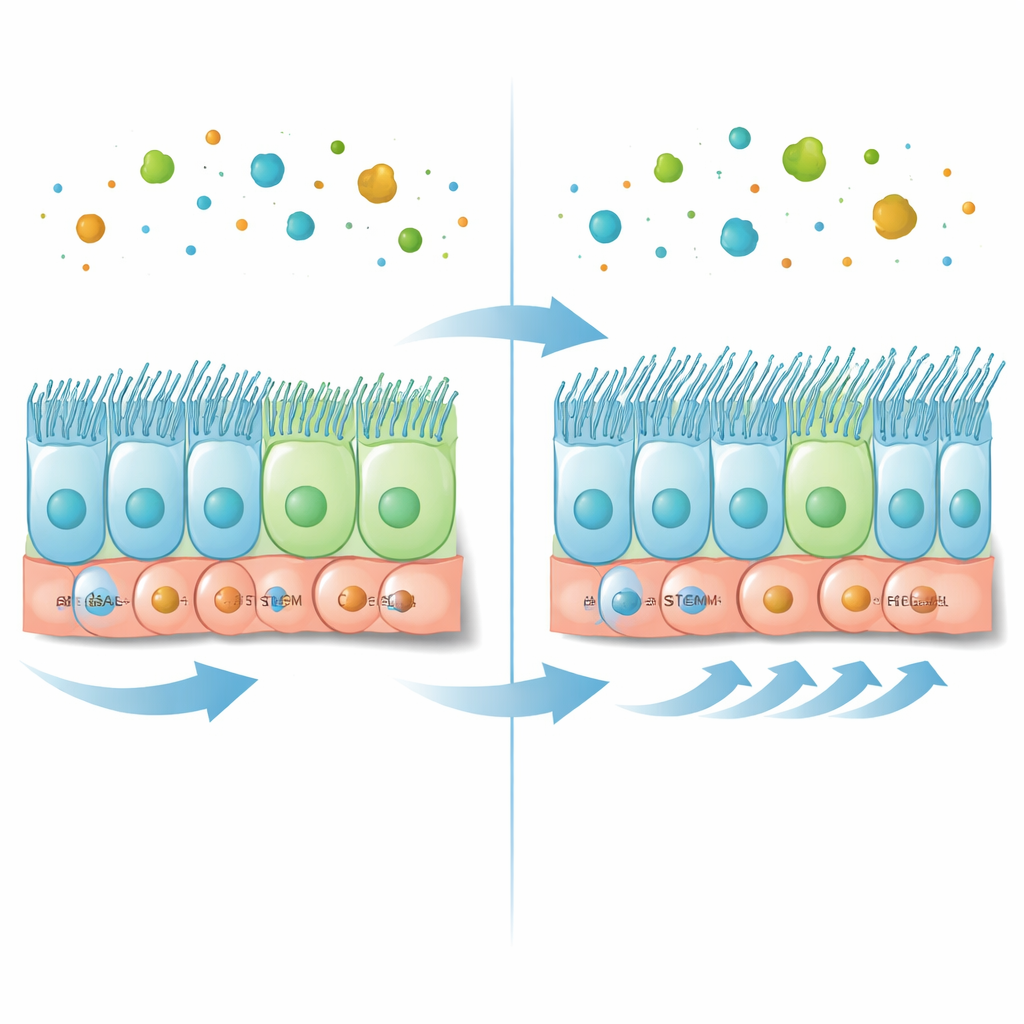
Bausteine der Reinigungsmaschine der Atemwege
Die innere Oberfläche der größeren Atemwege besteht aus einer einschichtigen Zelllage mit unterschiedlichen Zelltypen. An der Basis sitzen basale Stammzellen, ein Reservetank, der sich sowohl selbst erneuern als auch spezialisierte Zellen hervorbringen kann. Einige ihrer Nachkommen entwickeln sich zu sekretorischen Zellen, die Schleim produzieren, andere zu mehrflimmerigen Zellen, die mit vielen beweglichen Härchen besetzt sind und den Schleim Richtung Mund treiben. Das richtige Verhältnis dieser Zelltypen ist entscheidend für freie Atemwege und gesundes Atmen. In früheren Arbeiten fiel auf, dass das Protein Caveolin-1 in basalen Stammzellen und in mehrflimmerigen Zellen angereichert ist, seine genaue Rolle in diesem feinen Gleichgewicht aber unklar blieb.
Ein verborgener Ordnungsfaktor in der Epitheloberfläche aufspüren
In dieser Studie analysierten die Wissenschaftler Lungengewebe von Mäusen und im Labor kultivierte Atemwegskulturen, um zu kartieren, wo Caveolin-1 während der Reifung des Epithels vorkommt. Mithilfe hochauflösender Mikroskopie und Genexpressionsanalysen fanden sie heraus, dass Caveolin-1 am stärksten in basalen Stammzellen und in bestimmten intermediären Zellen vorkommt, die entweder zu Schleim-produzierenden oder zu mehrflimmerigen Zellen heranreifen können. Während das Gewebe in Kultur heranreift, sinken die Caveolin-1-Spiegel insgesamt, parallel zu einem Anstieg von Markern für mehrflimmerige Zellen. Dieses Muster deutete darauf hin, dass Caveolin-1 als Bremse oder Feineinstellung während des Übergangs von Stammzellen zu voll ausgereiften Flimmerzellen wirken könnte.
Was passiert, wenn die Bremse gelöst wird
Um diese Idee zu prüfen, reduzierten oder entfernten die Forschenden Caveolin-1 in Stammzellen und verfolgten die Entwicklung des Epithelgewebes in vitro. Die grundlegende Organisation und Barrierefunktion des Epithels blieb erhalten, und die Stammzellen teilten sich weiterhin normal. Gewebe ohne Caveolin-1 produzierten jedoch konsequent mehr mehrflimmerige Zellen, und diese Zellen reiften schneller heran. Zu Beginn der Differenzierung zeigten Genexpressionsprofile eine starke frühe Aktivierung von cilienbezogenen Programmen, wenn Caveolin-1 fehlte. Später zeigten mikroskopische Aufnahmen, dass die Flimmerhärchen länger waren und häufiger schlugen, was darauf hindeutet, dass nicht nur die Zahl, sondern auch die Leistungsfähigkeit der mehrflimmerigen Zellen gesteigert war.
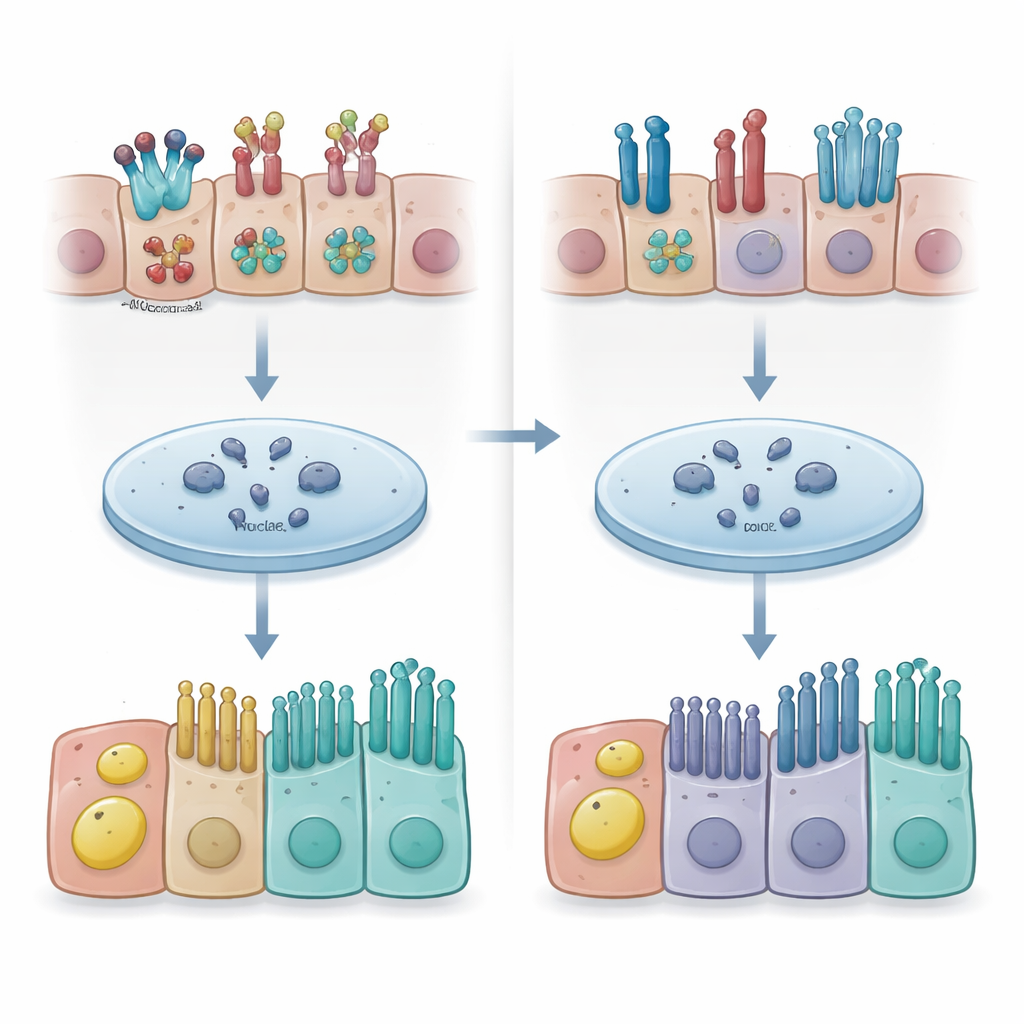
Ein Gespräch zwischen Membran und zellulärem Entscheidungsschalter
Die Forschenden fragten dann, wie Caveolin-1 so weitreichende Veränderungen der Zellschicksale beeinflussen könnte. Sie richteten ihren Blick auf die Notch-Signalgebung, einen Signalweg, der wie ein zelluläres Schaltpult wirkt: Wenn er aktiv ist, lenkt er basale Stammzellen in sekretorische Schicksale; ist er unterdrückt, begünstigt er mehrflimmerige Zellen. Notch-Rezeptoren sitzen in der Zellmembran und setzen bei Aktivierung ein intrazelluläres Fragment frei, das zum Zellkern wandert, um die Genaktivität zu steuern. Das Team fand, dass in Zellen ohne Caveolin-1 die frühe Notch-Signalausgabe reduziert war, obwohl die Gene für Rezeptoren und Liganden normal exprimiert wurden. Chromatinbindungsstudien zeigten, dass das aktive Notch-Fragment an deutlich weniger Stellen der DNA gebunden war, wenn Caveolin-1 reduziert war. Weitere biochemische Analysen deuteten darauf hin, dass Caveolin-1 dabei hilft, die Verarbeitung der Notch1- und Notch2-Rezeptoren zu organisieren und wie effektiv deren aktive Fragmente das Genom erreichen und binden.
Warum das für gesunde und kranke Lungen wichtig ist
Zusammen deuten diese Befunde darauf hin, dass Caveolin-1 ein zentraler Koordinator dafür ist, wie Atemwegsstammzellen ihr Schicksal bestimmen. Statt die Teilungsrate der Stammzellen direkt zu verändern, justiert Caveolin-1 die Stärke der Notch-Signalgebung zu Beginn der Differenzierung, was wiederum festlegt, wie viele Zellen mehrflimmerig werden und wie schnell ihre Flimmerhärchen ausreifen. Fehlt Caveolin-1 oder ist es reduziert, schwächt sich der Einfluss von Notch ab, wodurch das Gleichgewicht zugunsten von mehr und aktiveren mehrflimmerigen Zellen verschoben wird. Praktisch gesehen offenbart diese Arbeit einen molekularen Hebel, der eines Tages gezielt werden könnte, um das gesunde Epithel der Atemwege bei Erkrankungen wie Asthma, chronisch obstruktiver Lungenerkrankung oder Mukoviszidose wiederherzustellen, in denen die Reinigungsmechanik der Lunge oft gestört ist.
Zitation: Olivera-Gómez, M., Cumplido-Laso, G., Benitez, D.A. et al. Caveolin-1 modulates Notch transcriptional activity during in vitro respiratory multiciliated cell maturation. Sci Rep 16, 9165 (2026). https://doi.org/10.1038/s41598-026-40201-6
Schlüsselwörter: Atemwegsepithelium, mehrflimmerige Zellen, Caveolin-1, Notch-Signalgebung, Lungenregeneration