Clear Sky Science · de
Multimodale Charakterisierung der strömungsinduzierten Bildung und des Wachstums von Thromben in der extrakorporalen Membranoxygenierung
Warum Blutgerinnsel in lebenserhaltenden Maschinen wichtig sind
Die extrakorporale Membranoxygenierung, kurz ECMO, ist eine Form der Herz‑Lungen‑Bypassunterstützung, die kritisch kranke Patienten am Leben halten kann, während sich ihre Organe erholen. Wird Blut jedoch durch Pumpen und Kunststoffschläuche geleitet, ist es mechanischen Belastungen ausgesetzt, für die der Körper nicht ausgelegt ist. Diese Kräfte können gefährliche Blutgerinnsel im Kreislauf auslösen, die wiederum das Risiko für Schlaganfall, Organschäden oder Maschinenversagen erhöhen. Diese Studie hatte zum Ziel, genau zu verstehen, wie die Strömung des Bluts durch eine ECMO‑Pumpe die Entstehung und das Wachstum solcher Thromben beeinflusst, mit dem langfristigen Ziel, ECMO sicherer und wirksamer zu machen.
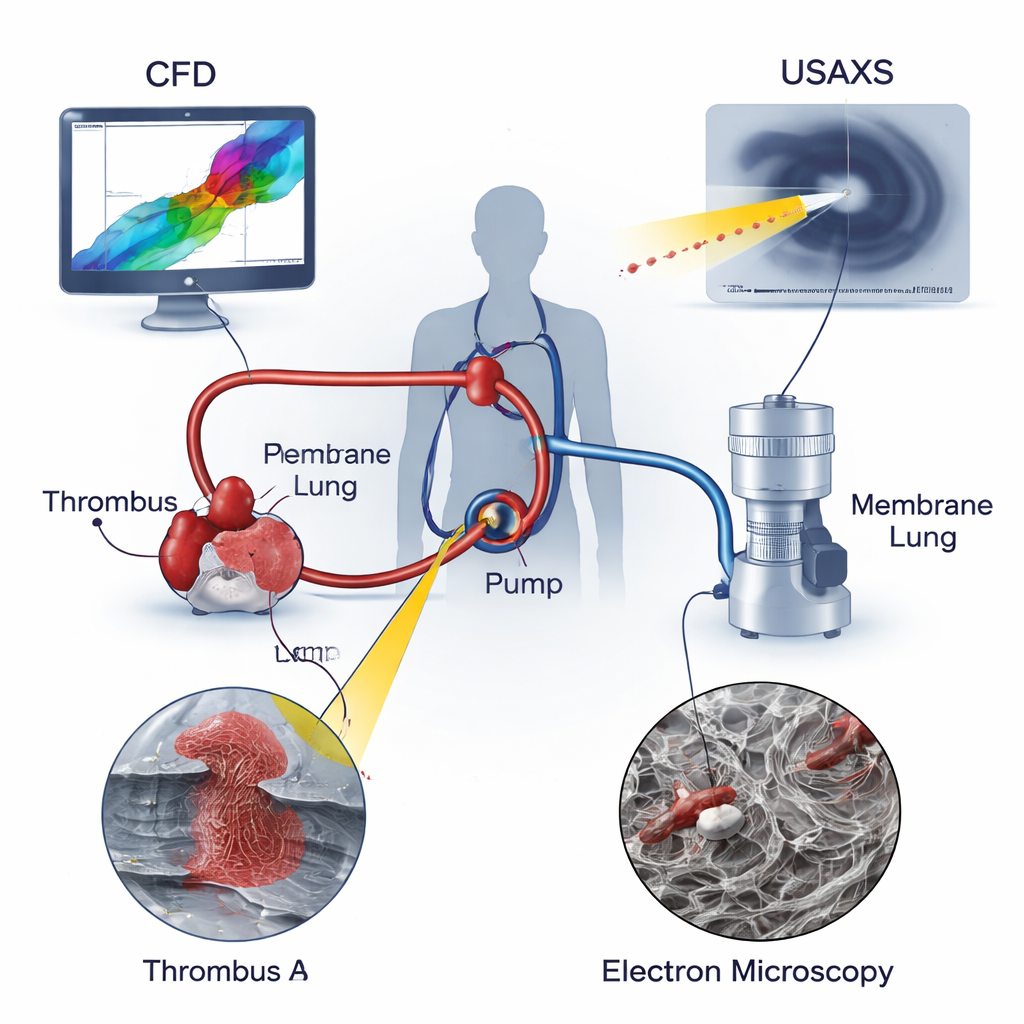
Wie ECMO Patienten am Leben hält
Bei der ECMO wird Blut aus einer großen Vene oder Arterie entnommen, von einer Zentrifugalpumpe durch eine „Membran‑Lunge“ gepumpt, die Sauerstoff zuführt und Kohlendioxid entfernt, und dann zum Patienten zurückgeführt. Anders als der gleichmäßige Fluss in natürlichen Gefäßen weist die Strömung im ECMO‑Kreislauf extreme Bedingungen auf: sehr schnelle Ströme, scharfe Richtungswechsel und nahezu stagnierende Bereiche, in denen Blut verweilt. Diese Umgebungen können Blutzellen schädigen und die Gerinnung fördern. Klassische medizinische Modelle konzentrieren sich auf langsame oder blockierte Gefäßströmungen, erfassen jedoch nicht vollständig das intensive Scheren und Dehnen, dem Blut in einer rotierenden Pumpe ausgesetzt ist. Die Autoren argumentieren, dass man zur vollständigen Einschätzung des Thromboserisikos in der ECMO sowohl die mechanischen Kräfte im Gerät als auch die mikroskopische Struktur der entstehenden Thromben untersuchen muss.
Thromben aus drei Blickwinkeln betrachten
Die Forscher kombinierten drei leistungsfähige Methoden, um zwei echte Thromben aus in der Pädiatrie eingesetzten ECMO‑Kreisläufen zu analysieren: einen Thrombus am Pumpeneinlass (Thrombus A) und einen weiteren im Schlauch unmittelbar stromabwärts der Pumpe (Thrombus B). Computational Fluid Dynamics (CFD) simulierte die Blutströmung durch die Pumpe und zeigte Bereiche mit Rezirkulation und wirbelförmiger Strömung sowie Stellen, an denen Scher‑ und Dehnungskräfte ihren Höhepunkt erreichten. Ultra‑Small‑Angle X‑Ray Scattering (USAXS) drang tief in jeden Thrombus ein und maß, wie dicht gepackt und wie stark gerichtet das Fibringerüst — das Proteinnetz, das Thromben zusammenhält — im gesamten Probenvolumen war. Die Rasterelektronenmikroskopie (SEM) lieferte stark vergrößerte Bilder der Thrombusoberflächen und zeigte die Formen roter und weißer Blutkörperchen, von Thrombozyten und die umgebenden Fibrinfibrillen. Durch das Überlagern dieser drei Perspektiven konnten die Autoren lokale Strömungsbedingungen mit der inneren Architektur jedes Thrombus verknüpfen.
Eine Rezirkulationszone bildet einen steifen, ausgerichteten Thrombus
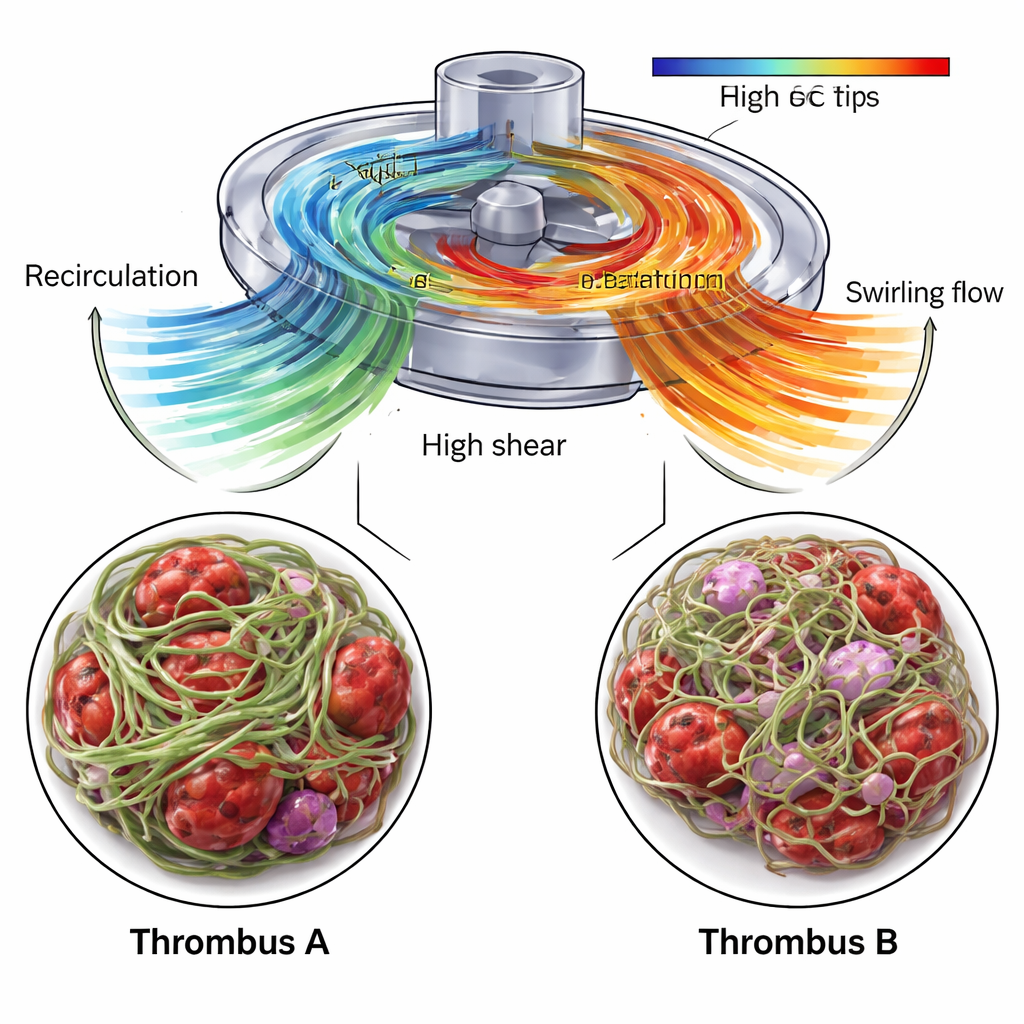
CFD zeigte, dass sich in der Nähe des Pumpeneinlasses, wo Thrombus A entstand, eine Rezirkulationszone befand: Blut wurde rückwärts und aufwärts entlang des Gehäuses gedrückt, bevor es wieder in den Hauptstrom eintrat. Diese Region erlaubte es Blutbestandteilen, länger zu verweilen, während gleichzeitig scharfe Geschwindigkeitsunterschiede an der Grenze zwischen rezirkulierender und einströmender Strömung auftraten. Innerhalb von Thrombus A wies USAXS einen hohen Fibrinanteil — mindestens 70 Prozent — und eine starke Gesamtalignment der Fasern in einer bevorzugten Richtung nach, was auf ein dichtes, steifes Gerüst hindeutet. SEM‑Bilder bestätigten ein eng gewebtes Fibrinnetz, durchsetzt mit auffällig verformten Erythrozyten und Thrombozytenfragmenten. Die Autoren schlagen vor, dass die Kombination aus langen Verweilzeiten und starken lokalen Scherkräften das Wachstum eines kompakten, hoch organisierten Thrombus begünstigte, der den mechanischen Belastungen der Pumpe standhalten kann.
Wirbelnde Ausströmung formt einen lockereren, verdrehten Thrombus
Im Gegensatz dazu wuchs Thrombus B, entnommen aus dem Schlauch nach der Pumpe, in einer Region, die von wirbelnder Ausströmung dominiert war. CFD zeigte rotierende, spiralähnliche Strömungsstrukturen, die aus dem Pumpenausgang austreten, und die USAXS‑Daten ergaben ein weiterhin dominantes, jedoch weniger dichtes und insgesamt weniger stark ausgerichtetes Fibrinnetz. Die Hauptorientierung der Fibrinfasern änderte sich allmählich über den Thrombus hinweg, von einem Neigungswinkel zu einem anderen, was das verdrehte Strömungsmuster widerspiegelt. SEM‑Bilder zeigten Fibrinfäden unterschiedlicher Dicke und zahlreiche eingeschlossene rote und weiße Blutkörperchen, einschließlich Hinweise auf Zellschädigung und Entzündung. Wichtig ist, dass die Simulationen auch kleine, aber signifikante Volumenbereiche in der Pumpe identifizierten, in denen Dehnungskräfte groß genug waren, um den von Willebrand‑Faktor zu entfalten — ein zentrales Blutprotein, das unter Stress klebrig wird und schnell Thrombozyten anziehen kann. Diese Zonen konzentrierten sich in der Nähe der Laufradblätter und des Auslasses und sind daher wahrscheinliche Orte für die initialen Aktivierungsereignisse, die zu Thrombus B führten.
Auf dem Weg zu sichereren lebenserhaltenden Geräten
Indem detaillierte Strömungssimulationen des Bluts mit Röntgen‑ und Elektronenmikroskopmessungen realer ECMO‑Thromben zusammengeführt wurden, zeigt diese Arbeit, dass die innere „Struktur“ und Dichte eines Thrombus das mechanische Umfeld widerspiegelt, in dem er entstanden ist. Rezirkulierende Strömung nahe dem Pumpeneinlass wurde mit einem dichten, stark ausgerichteten Fibringerüst in Verbindung gebracht, während wirbelnde Ausströmung mit einem verdrehteren, offeneren Netzwerk assoziiert war, das dennoch viele Blut‑ und Immunzellen einschloss. Diese Erkenntnisse heben konkrete Bereiche in ECMO‑Pumpen und Schläuchen hervor, in denen konstruktive Änderungen oder gezielte Anpassungen der Antikoagulation am wirkungsvollsten das Thromboserisiko verringern könnten. Langfristig könnte eine solche multiskalige Kartierung — von der Pumpengeometrie und den Strömungsmustern bis zur Proteinordnung — sichere Gerätekonzepte leiten und Klinikern helfen, die beiden Gefahren von Blutungen und Thrombose während lebensrettender ECMO‑Therapie besser abzuwägen.
Zitation: Nilsson, F., Sochor, B., Henriksson, S. et al. Multimodal characterization of flow-induced thrombus initiation and growth in extracorporeal membrane oxygenation. Sci Rep 16, 7166 (2026). https://doi.org/10.1038/s41598-026-40177-3
Schlüsselwörter: ECMO, Blutgerinnung, Scherkräfte, Zentrifugalblutpumpe, Fibrinstruktur