Clear Sky Science · de
Müller-Glia- und Mikroglia-Antworten gekoppelt an die Erholung von Zapfen-Photorezeptoren nach begrenzter Zapfen-Ablation in der Netzhaut von Zebrafingen
Warum die Heilung von Fischaugen wichtig ist
Der hintere Teil des Auges, die Netzhaut, verwandelt Licht in Seheindruck. Beim Menschen wachsen diese lichtempfindlichen Zellen nach schweren Schäden nur selten wieder nach, was zu dauerhaftem Sehverlust führen kann. Zebrafische sind anders: Sie können Teile ihrer Netzhaut auf natürliche Weise reparieren. Diese Studie untersucht, was passiert, wenn nur ein kleiner Bruchteil der farbempfindlichen Zellen der Zebrafische kurzzeitig gestresst oder verloren geht, und zeigt, wie Stützzellen und Immunzellen aktiv werden, um der Netzhaut bei der Erholung zu helfen. Das Verständnis dieses Zusammenspiels könnte eines Tages neue Wege inspirieren, das menschliche Sehen zu schützen oder zu reparieren.
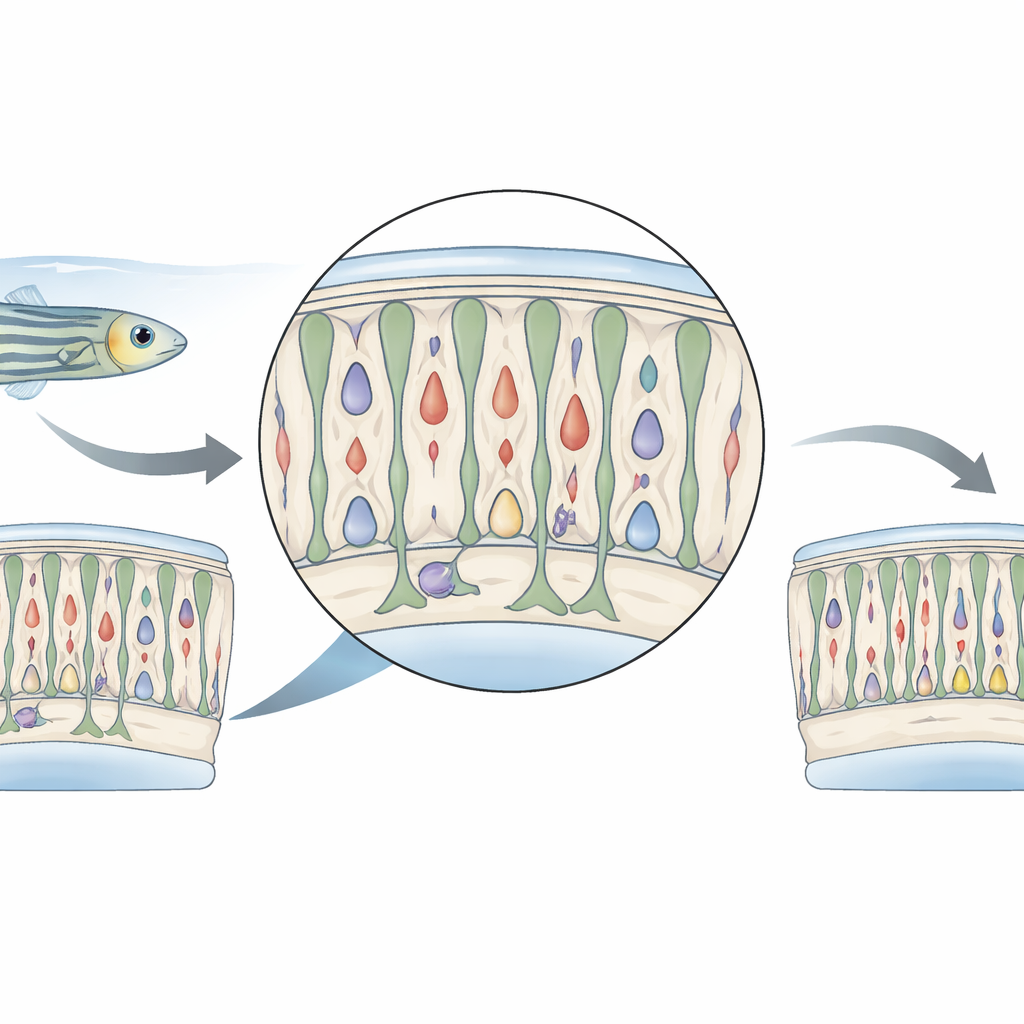
Ein sanfter Anschub fürs Auge
Die Forschenden arbeiteten mit gentechnisch veränderten Zebrafischen, deren Zapfen-Photorezeptoren — die Zellen, die Farbe und Tageslicht detektieren — ein Enzym tragen, das ein harmloses Medikament nur in diesen Zapfen in ein Gift umwandeln kann. Erwachsene Tiere wurden 24 Stunden lang in das Medikament Metronidazol getaucht und dann in sauberes Wasser zurückgebracht. Anstatt große Mengen an Zapfen zu vernichten, tötete diese Behandlung nur eine kleine Untergruppe. Die meisten Zapfen überlebten, zeigten jedoch Anzeichen vorübergehender Schädigung: ihr Erscheinungsbild veränderte sich, ihr fluoreszierendes Signal schwächte sich ab und ein wichtiges Zapfen-Gen, gnat2, wurde herunterreguliert. Die Fische verhielten sich kurz nach der Behandlung, als sei ihr Sehvermögen gedämpft, doch diese Probleme klangen innerhalb weniger Tage ab, als die Netzhaut zu regenerieren begann.
Farbzellen unter Stress
Um zu sehen, was in einzelnen Zellen vor sich ging, nutzte das Team Einzelzell-RNA-Sequenzierung, die abliest, welche Gene in tausenden Einzelzellen gleichzeitig aktiviert sind. Sie konzentrierten sich auf zwei bis fünf Tage nach Entfernen des Medikaments, ein Zeitfenster, in dem die Zapfen eher zu genesen als zu sterben schienen. Überlebende Zapfen reduzierten die Expression vieler Gene, die für Lichtwahrnehmung und Signalverarbeitung zuständig sind, was darauf hindeutet, dass sie vorübergehend ihre visuelle Maschinerie „herunterfahren“. Gleichzeitig erhöhten sie Gene, die mit dem Umgang mit schädlichen Sauerstoffnebenprodukten und der Erhaltung der Proteinqualität verbunden sind. Dieses Muster weist auf einen Stressreaktionsmodus hin, in dem Zapfen Schadenskontrolle und Wiederherstellung priorisieren anstatt maximale Sehfunktion.
Stützzellen schalten in den Reparaturmodus
Die wichtigsten Stützzellen der Netzhaut, die sogenannten Müller-Gliazellen, reagierten stark, obwohl nur ein begrenzter Zapfenverlust festgestellt wurde. Diese Gliazellen erstrecken sich von der unteren bis zur oberen Schicht der Netzhaut, berühren direkt die lichtempfindlichen Zellen und sind bei Zebrafisch bekannt dafür, nach Verletzung als Quelle neuer Neuronen zu dienen. In dieser Studie fuhren Müller-Glia Gene hoch, die typischerweise mit Reaktivität und Gewebsumgestaltung assoziiert sind, und viele von ihnen traten wieder in den Zellzyklus ein, ein Zeichen dafür, dass sie sich zu teilen begannen. Die Autor*innen beobachteten neue progenitorähnliche Zellen, die in der mittleren Schicht der Netzhaut erschienen und dann zur äußeren Schicht wanderten, die die Photorezeptoren beherbergt. Einige dieser Reparaturantworten gingen mit Umschaltungen in Genen einher, die normalerweise in Stammzellen aktiv sind, was darauf hindeutet, dass Müller-Glia teilweise in einen flexibleren, regenerativen Zustand zurückkehrten, obwohl der tatsächliche Zellverlust nur gering war.
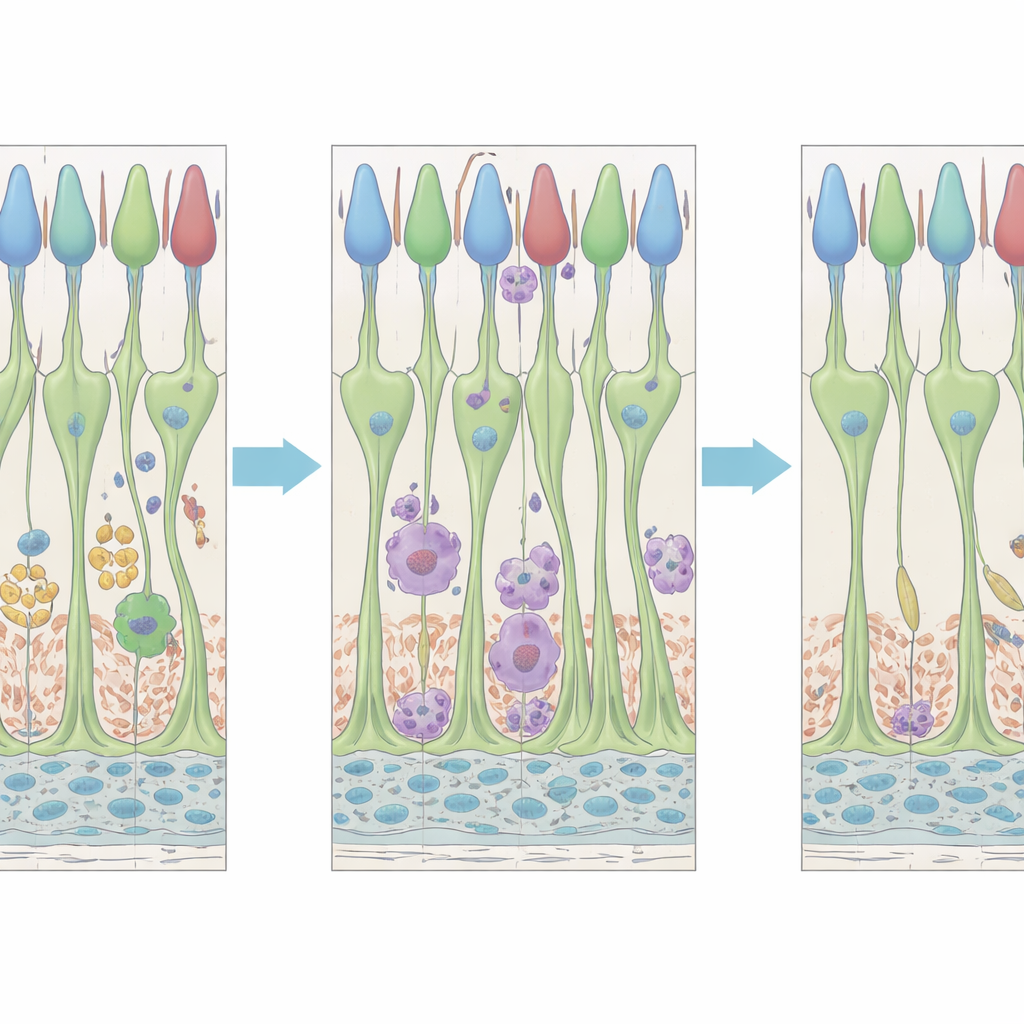
Immunzellen mit zwei Wellen des Handelns
Die im Auge ansässigen Immunzellen, die Mikroglia und andere eng verwandte myeloische Zellen, zeigten ebenfalls eine zweistufige Reaktion. Innerhalb von etwa zwei Tagen nach der Behandlung veränderten Mikroglia ihre Form, sammelten sich um sterbende Zapfen und halfen wahrscheinlich, Trümmer zu beseitigen. Später, etwa vier bis fünf Tage nach der Behandlung, trat eine zweite Welle veränderter mikroglialer Aktivität auf: Zellen erschienen in der Nähe der äußeren Segmente der Zapfen und im Raum nahe der pigmentierten Schicht hinter der Netzhaut, zu einer Zeit, in der die Zapfen eindeutige Zeichen der Erholung zeigten. Die Genexpressionsmuster deuteten darauf hin, dass es mindestens zwei unterschiedliche mikrogliaähnliche Subpopulationen mit verschiedenen molekularen Signaturen gibt, was nahelegt, dass einige Immunzellen auf das Aufräumen sterbender Zellen spezialisiert sein könnten, während andere eher Stressed, aber überlebende Neurone unterstützen.
Was das für den Schutz des Sehens bedeutet
Diese Arbeit zeigt, dass in Zebrafischen schon eine begrenzte und kurzzeitige Störung der farbempfindlichen Zellen ausreicht, um eine koordinierte Antwort von Stützzellen und Immunzellen zu mobilisieren. Zapfen drosseln vorübergehend ihre visuelle Funktion, während sie interne Reparaturprogramme anschalten. Müller-Glia werden reaktiv, teilen sich und erzeugen Progenitorzellen, und Mikroglia reagieren in zeitlich abgestimmten Wellen, die zuerst mit Zellsterben und später mit Stresswiederherstellung verbunden sind. Gemeinsam scheinen diese Reaktionen der Netzhaut zu helfen, Struktur und Funktion nach einer milden Schädigung wiederherzustellen. Für menschliche Augenkrankheiten, die eher durch langsame, chronische Schädigung als durch plötzliche Verletzung gekennzeichnet sind, könnte das Verständnis, wie Zebrafische Glia und Immunzellen bei sublethalen Stressreaktionen mobilisieren, Hinweise auf Therapien geben, die die körpereigenen Fähigkeiten des Auges stärken, gefährdete Photorezeptoren zu stabilisieren oder sogar wiederaufzubauen.
Zitation: Weimar, H.V., Farre, A.A., Rumford, J.E. et al. Müller glial and microglial responses coupled to recovery of cone photoreceptors following limited cone ablation in zebrafish retina. Sci Rep 16, 9058 (2026). https://doi.org/10.1038/s41598-026-40141-1
Schlüsselwörter: Zebrafisch-Netzhaut, Zapfen-Photorezeptoren, Müller-Glia, Mikroglia, Retinale Regeneration