Clear Sky Science · de
Machine-Learning-gestützte transkriptomische Integration identifiziert GFM1 als mit Lactylierung verbundenen Kandidaten-Biomarker bei Aortendissektion
Warum diese verborgene Gefahr in der Aorta zählt
Eine Aortendissektion ist ein medizinischer Notfall, bei dem ein Riss in der Hauptschlagader zu binnen Stunden lebensbedrohlichen inneren Blutungen führen kann. Ärztinnen und Ärzte können Patientinnen und Patienten oft mit einer dringenden Operation retten, doch es gibt noch keinen verlässlichen Bluttest, der früh vor der Gefahr warnt, und keine Medikamente, die den Krankheitsverlauf definitiv verlangsamen. Diese Studie untersucht, ob subtile Veränderungen in der Energie- und Signalverarbeitung von Gefäßzellen neue Warnhinweise liefern könnten. Im Fokus steht ein wenig bekanntes Gen namens GFM1, das möglicherweise den Stoffwechsel der Zelle mit der Schwächung der Aortenwand verbindet.
Den Code eines gefährlichen Risses knacken
Bei einer Aortendissektion dringt Blut in die Wand der Aorta ein und trennt deren Schichten. Warum die Aorta mancher Menschen auf diese Weise versagt, ist noch nicht vollständig geklärt. Die Autorinnen und Autoren analysierten Muster der Genaktivität in Proben von Betroffenen mit Aortendissektion und von Personen mit gesunden Aorten. Besonderes Augenmerk legten sie auf Gene, die mit „Lactylierung“ in Verbindung stehen — einer kürzlich entdeckten Modifikation, bei der Zellen Laktat — bekannt aus Muskelermüdung — nutzen, um Proteine und Genregulation zu beeinflussen. Da Lactylierung mit Entzündungen und Gewebeumbau in Verbindung gebracht wurde, vermutete das Team, dass laktatbezogene Gene auch an der Schädigung der Aortenwand beteiligt sein könnten.
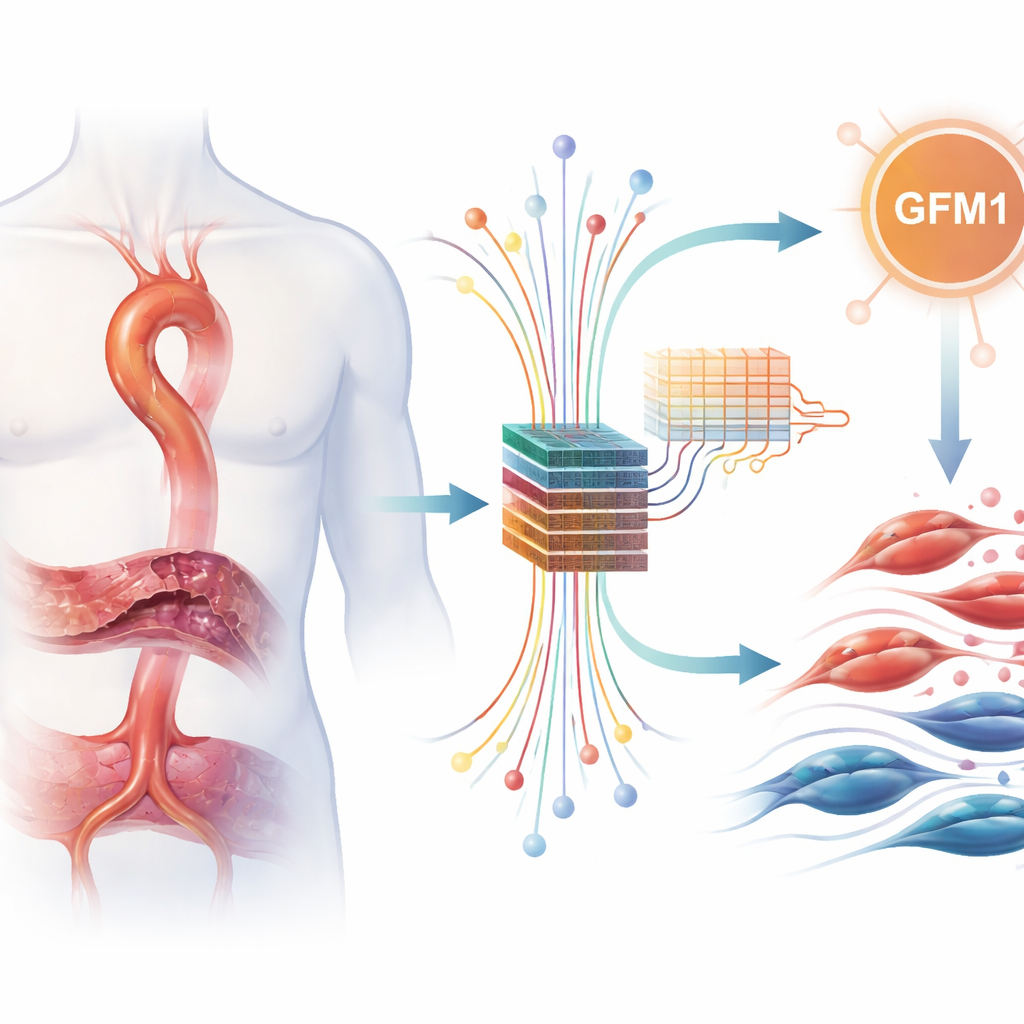
Große Datensätze mit intelligenten Algorithmen auswerten
Um diese Idee zu prüfen, bündelten die Forschenden mehrere öffentlich zugängliche Datensätze, die aufzeichnen, welche Gene im Aorten-Gewebe hoch- oder herunterreguliert sind. Sie korrigierten sorgfältig für technische Unterschiede zwischen den Studien und suchten dann nach Genen, deren Aktivität in kranken und gesunden Proben konsistent unterschiedlich war. Von Tausenden Genen identifizierten sie 217 mit deutlichen Veränderungen, viele davon mit Hinweisen auf Immunreaktionen und Umbau der Gewebsstruktur, die die Aorta stützt. Anschließend konzentrierten sie sich auf eine kuratierte Liste von Genen, die mit Laktatverarbeitung und Lactylierung zusammenhängen, und fanden 11 Gene, die sowohl bei der Aortendissektion verändert waren als auch Teil dieser laktatbezogenen Programme sind.
Die Maschine abstimmen lassen: ein Schlüsselverdächtiger
Elf interessante Gene waren noch zu viele, um sie alle im Labor eingehend zu untersuchen. Daher nutzte das Team Machine-Learning-Methoden als objektives „Abstimmungssystem“. Sie speisten die Daten dieser Gene in drei verschiedene Modelle — LASSO, Random Forest und XGBoost — ein, die häufig verwendet werden, um Muster zu finden, die Patientinnen und Patienten von Kontrollen unterscheiden. Jede Methode hob eigene Favoriten hervor, aber nur ein Gen, GFM1, wurde von allen drei zuverlässig und stark ausgewählt. Dieser Kreuzvergleich machte GFM1 als besonders robusten Kandidaten sichtbar, wobei die Modelle zur Rangfolge dienten, nicht zur Erstellung eines sofort einsatzbereiten Diagnosetests.
Fokus auf Gefäßmuskelzellen
GFM1 hilft zu steuern, wie Mitochondrien — die Energiequellen der Zelle — ihre eigenen Proteine herstellen. Da das Energiegleichgewicht entscheidend für das Verhalten der Zellen in der Aortenwand ist, untersuchten die Autorinnen und Autoren GFM1 näher. Sie bestätigten, dass die GFM1-Spiegel in Gewebe von Patientinnen und Patienten mit Aortendissektion höher waren als in nicht erkrankten Aorten. Dann verwendeten sie ein kontrolliertes Zellkultursystem mit Maus-gefäßglatten Muskelzellen — den muskelähnlichen Zellen, die der Aorta Festigkeit verleihen. Wurden diese Zellen mit Angiotensin II stimuliert, einem Hormon, das mit Bluthochdruck und Gefäßstress verbunden ist, neigten sie stärker zur Proliferation und Migration, was schädliche Veränderungen nachahmt, wie sie in erkrankten Arterien beobachtet werden. Senkten die Forscher mittels small interfering RNA die GFM1-Expression in diesen Zellen, waren das angiotensinvermittelte Wachstum und die Migration deutlich reduziert, was darauf hindeutet, dass GFM1 diese riskanten Verhaltensweisen fördert.
Was das bedeutet — und was noch nicht bewiesen ist
Insgesamt deuten die Ergebnisse darauf hin, dass GFM1 eine Brücke zwischen verändertem Zellstoffwechsel und dem aggressiven Verhalten der Zellen der Aortenwand bei Aortendissektion schlagen könnte. Einfach gesagt scheint höhere GFM1-Aktivität mit einer instabileren, schädigungsanfälligeren Aorta einherzugehen, und das Herunterregeln von GFM1 in Laborzellen macht diese weniger proliferativ und weniger migrierend. Die Autorinnen und Autoren betonen jedoch, dass diese Arbeit noch in einer frühen, hypothesenbildenden Phase ist. Sie haben in den Geweben nicht direkt Lactylierung gemessen und auch nicht nachgewiesen, dass GFM1 selbst chemisch in dieser Weise modifiziert ist; die Vorhersagekraft der Modelle wurde nicht in unabhängigen Patientengruppen geprüft. Zukünftige Studien müssen diese Ergebnisse in größeren Kohorten bestätigen und genau untersuchen, wie GFM1 und verwandte metabolische Veränderungen die Aortenwand schwächen. Gelingt dies, könnten GFM1 oder seine Signalwege schließlich Zielstrukturen für neue Bluttests oder Therapien werden, die diese oft tödliche Ruptur verhindern sollen.
Zitation: Chen, J., Jiang, N., Guo, Z. et al. Machine-learning–guided transcriptomic integration identifies GFM1 as a lactylation-related candidate biomarker in aortic dissection. Sci Rep 16, 9033 (2026). https://doi.org/10.1038/s41598-026-40139-9
Schlüsselwörter: Aortendissektion, gefäßglatte Muskelzellen, Laktatstoffwechsel, Mitochondrienfunktion, Biomarker-Entdeckung