Clear Sky Science · de
Bewertung der Wirksamkeit von Bakteriophagen gegen Pseudomonas aeruginosa in ex vivo- und in vitro-Hautsystemen des Hundes
Warum Hautinfektionen neue Lösungen brauchen
Hartnäckige Hautinfektionen sind nicht nur lästig für Haustiere und ihre Besitzer — sie können zu langanhaltenden, schmerzhaften Problemen werden, die auf Standardantibiotika nicht ansprechen. Ein häufiger Verursacher ist Pseudomonas aeruginosa, ein schwer zu bekämpfendes Bakterium, das in schleimigen Biofilmen auf Wunden gedeiht. Diese Studie untersucht, ob Viren, die Bakterien infizieren — sogenannte Bakteriophagen oder kurz Phagen — diese Infektionen in Hundenhautmodellen sicher beseitigen können und damit neue Optionen aufzeigen, die eines Tages sowohl Tieren als auch Menschen helfen könnten.
Ein zäher Keim, der Schleim liebt
Pseudomonas aeruginosa ist ein opportunistischer Erreger, der zuschlägt, wenn die Abwehr geschwächt ist, und schwere Lungen-, Blut- und Wundinfektionen in Krankenhäusern und Tierkliniken verursacht. Er wächst häufig in Biofilmen — dünnen, klebrigen Schichten von Bakterien, die durch eine schützende Matrix zusammengehalten werden. Innerhalb dieser Filme sind die Mikroben deutlich schwerer mit Antibiotika zu erreichen und können dem Immunsystem besser entgehen, wodurch behandelbare Infektionen chronisch werden. Da multiresistente Pseudomonas-Arten inzwischen auf der Liste der höchsten Priorität der Weltgesundheitsorganisation stehen, suchen Forscher dringend nach Alternativen zu herkömmlichen Arzneien.
Viren, die Bakterien jagen
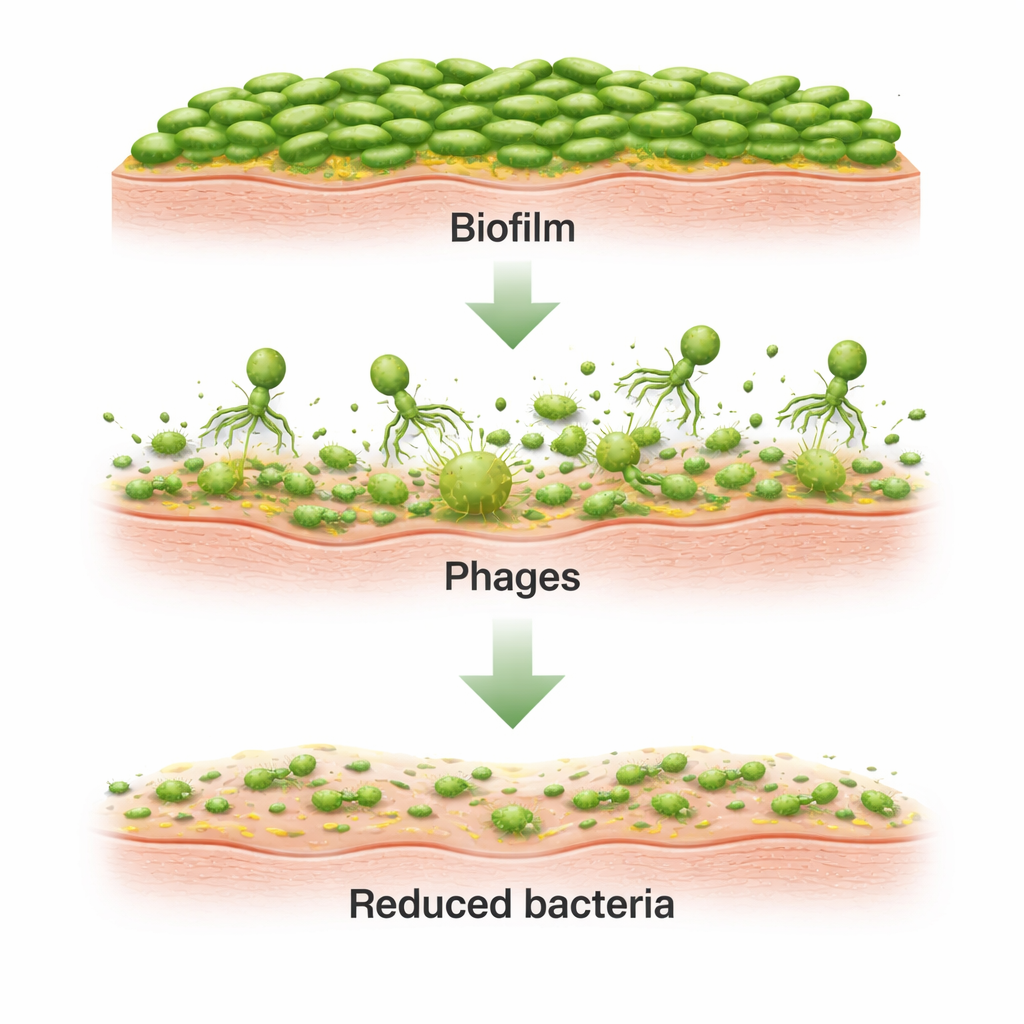
Bakteriophagen sind natürlich vorkommende Viren, die Bakterien infizieren und abtöten, ohne tierische oder menschliche Zellen zu schädigen. Das Team konzentrierte sich auf zwei gut charakterisierte Phagen, JG003 und PTLAW1, die ausgewählt wurden, weil sie stark lytisch sind und Gene tragen, die beim Abbau von Biofilmen helfen könnten. Zunächst testeten die Forschenden diese Phagen an im Labor gezüchteten Pseudomonas-Biofilmen, die auf Kunststoffplatten entstanden waren. Mithilfe fluoreszierender Farbstoffe und 3D-Konfokalmikroskopie zeigten sie, dass jeder Phage allein — und besonders das Paar zusammen — das gesamte Biofilmvolumen deutlich verringerte und den Anteil geschädigter bakterieller Membranen erhöhte, was einen effektiven Angriff auf die bakterielle Gemeinschaft signalisiert.
Phagen auf echter Hundehaut anwenden
Biofilme auf Kunststoff sind weitaus einfacher aufgebaut als echte Haut, die Schichten, Haarfollikel, Drüsen und eine widerstandsfähige äußere Barriere besitzt. Um realistischere Bedingungen nachzubilden, nutzten die Forschenden zwei canine Hautsysteme. In einem ex vivo-Ansatz wurden dünne Hautscheiben von Hunden in Franz-ähnliche Diffusionszellen montiert — Glaskonstruktionen mit einer Donorkammer oberhalb und einer Empfängerkammer unterhalb der Haut. Nachdem die Oberfläche 16 Stunden lang mit Pseudomonas infiziert worden war, trugen sie ein Gemisch der beiden Phagen auf. Im Verlauf der nächsten acht Stunden sanken die bakteriellen Zählzahlen in der Haut um etwa vier Größenordnungen im Vergleich zu unbehandelten Proben. Mikroskopische Untersuchungen bestätigten, dass dichte Bakteriencluster und Biofilmmatrix auf der Hautoberfläche nach Phagenexposition weitgehend aufgelöst waren, während die Phagen selbst aktiv blieben, jedoch nicht in die untere Kammer durchtraten.
Ein lebendes Hautmodell, das Entzündungen abbilden kann
Anschließend züchteten die Wissenschaftler ein lebendes „Epidermisäquivalent“ aus Hundezellen auf durchlässigen Einsätzen, das die äußeren Hautschichten einschließlich einer ordentlichen verhornten Oberfläche nachahmt. Dies ermöglichte nicht nur die Messung des bakteriellen Überlebens, sondern auch die Verfolgung entzündlicher Signale. Wurden diese Hautäquivalente mit einer geringen Zahl von Pseudomonas-Zellen infiziert und drei Stunden später mit dem Phagen-Cocktail behandelt, fielen die Bakterienkonzentrationen drastisch — in den meisten behandelten Proben waren keine Bakterien mehr nachweisbar. Gleichzeitig sanken die Werte des proinflammatorischen Botenstoffs CXCL8, der bei Infektionen stark ansteigt, sowohl auf Gen- als auch auf Proteinebene wieder in Richtung Normalwerte. Wichtig: Die Phagenexposition allein schadete den Hautzellen nicht und störte die Barrierestruktur nicht.
Was das für die zukünftige Wundversorgung bedeutet
Insgesamt zeigen diese Experimente, dass sorgfältig ausgewählte Phagen Pseudomonas-Biofilme merklich angreifen, die bakterielle Belastung verringern und frühe Entzündungen in realistischen Hundenhautmodellen dämpfen können, ohne erkennbare Nebenwirkungen. Zwar sterilisierten die Behandlungen stark infizierte Hautproben nicht vollständig und wurden hauptsächlich an frühen Biofilmen getestet, doch die Arbeit liefert einen reproduzierbaren präklinischen Rahmen, um Phagendosen, Zeitpunkte und Kombinationen — möglicherweise zusammen mit Antibiotika — zu verfeinern. Für Tierärzte, die schwierige Wunden beim Hund behandeln, und für Ärzte, die ähnlichen Infektionen beim Menschen gegenüberstehen, könnten phagenbasierte Sprays oder Cremes schließlich eine gezielte Möglichkeit bieten, biofilmgetriebene Infektionen anzugehen, die auf Standardmedikamente nicht mehr ansprechen.
Zitation: Dalponte, A., Filor, V., Nerlich, A. et al. Evaluation of bacteriophage efficacy against Pseudomonas aeruginosa in ex vivo and in vitro canine skin systems. Sci Rep 16, 7167 (2026). https://doi.org/10.1038/s41598-026-40091-8
Schlüsselwörter: Bakteriophagentherapie, Pseudomonas-Hautinfektion, Biofilm, canines Wundmodell, Antibiotikaresistenz