Clear Sky Science · de
Der antitumorale Wirkmechanismus von Oclacitinib bei hundlichem Lymphom
Warum das für Hunde und ihre Familien wichtig ist
Lymphom ist eine der häufigsten Krebsarten bei Haushunden. Chemotherapie kann vielen Patient:innen helfen, wirkt aber nicht immer und kann erhebliche Nebenwirkungen verursachen. Oclacitinib, eine Tablette, die bereits weit verbreitet gegen Juckreiz bei allergischer Hautkrankheit verschrieben wird, zeigte kürzlich überraschende Vorteile bei einigen Hunden mit Hautlymphom. Diese Studie stellt eine einfache, aber wichtige Frage: Wie genau kann dieses alltägliche Allergiemedikament gegen Krebszellen wirken, und lässt sich vorhersagen, welche Hunde am ehesten davon profitieren?
Von der Allergiemedizin zum Krebsbekämpfer
Oclacitinib wurde entwickelt, um überaktive Immunsignale zu dämpfen, die atopische Dermatitis antreiben. Es wirkt, indem es eine Familie molekularer Schalter blockiert, die JAKs genannt werden, insbesondere JAK1, die Botschaften von entzündlichen Molekülen an der Zelloberfläche zum Zellkern weiterleiten. Tierärzt:innen bemerkten, dass sich einige Hunde mit einer Form von Hautlymphom verbesserten, wenn sie Oclacitinib erhielten, doch die Gründe dafür waren unklar und die Ansprechraten uneinheitlich. Die Forscher:innen gingen dem kontrolliert nach, indem sie im Labor gezüchtete Lymphomzellen von Hunden sowie Proben aus echten Patienten verwendeten, um zu untersuchen, wann und wie Oclacitinib tatsächlich Krebszellen abtöten kann, statt nur die Haut zu beruhigen. 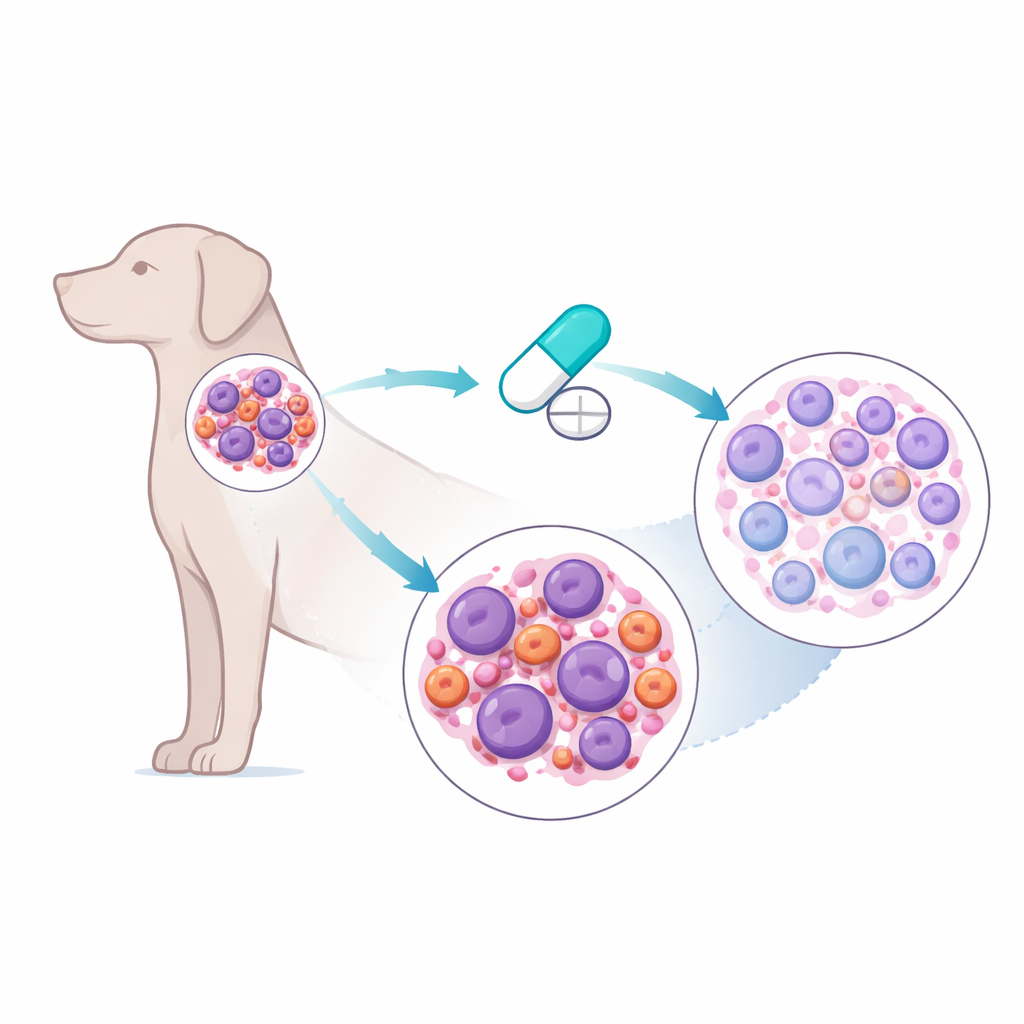
Untersuchung von Lymphomzellen im Labor
Das Team untersuchte eine canine kutane (Haut-)Lymphom-Zelllinie und acht weitere hochgradige Lymphomzelllinien, die sowohl T-Zell- als auch B-Zell-Tumoren repräsentieren. Bei Exposition dieser Zellen gegenüber Oclacitinib in Konzentrationen, die denen behandfter Hunde ähneln, zeigten etwa die Hälfte der Zelllinien deutlich verlangsamtes Wachstum, und mehrere durchliefen Zelltod. Empfindliche Zellen sammelten sich in einer Ruhestellung des Zellzyklus an und zeigten Kennzeichen des programmierten Zelltods, einschließlich Aktivierung eines Ausführerproteins namens Caspase‑3. Im Gegensatz dazu reagierten andere Lymphomlinien innerhalb des gleichen Konzentrationsbereichs kaum, was unterstreicht, dass Lymphom bei Hunden keine einheitliche Erkrankung, sondern eine Gruppe biologisch unterschiedlicher Tumoren ist.
Fokussierung auf einen verwundbaren Signalweg
Um herauszufinden, was sensible von resistenten Tumoren trennte, konzentrierten sich die Wissenschaftler:innen auf den JAK/STAT-Signalweg, einen häufigen Überlebensweg in vielen Blutkrebserkrankungen. Sie fanden heraus, dass nur die Lymphomzelllinien, die auf Oclacitinib ansprachen, eine starke Grundaktivierung zweier Schlüsselfaktoren zeigten: JAK1 und STAT5. Wenn diese sensiblen Zellen mit Oclacitinib behandelt wurden, sank die Aktivität von STAT5 stark, während die Gesamtmengen der Proteine gleich blieben. Ein zweites, in der Humanmedizin eingesetztes JAK1‑blockierendes Medikament, Filgotinib, zeigte ein ähnliches Muster aus Wachstumshemmung und Abschaltung von STAT5. Tiefe Genaktivitätsprofile zeigten, dass Oclacitinib Genprogramme dämpfte, die mit JAK/STAT-Signalgebung verbunden sind, und die Expression von c‑Myc verringerte, einem zentralen Wachstumsregulator, der in Krebszellen häufig missbraucht wird. Das hilft, den beobachteten Zellzyklusstopp und Zelltod zu erklären. 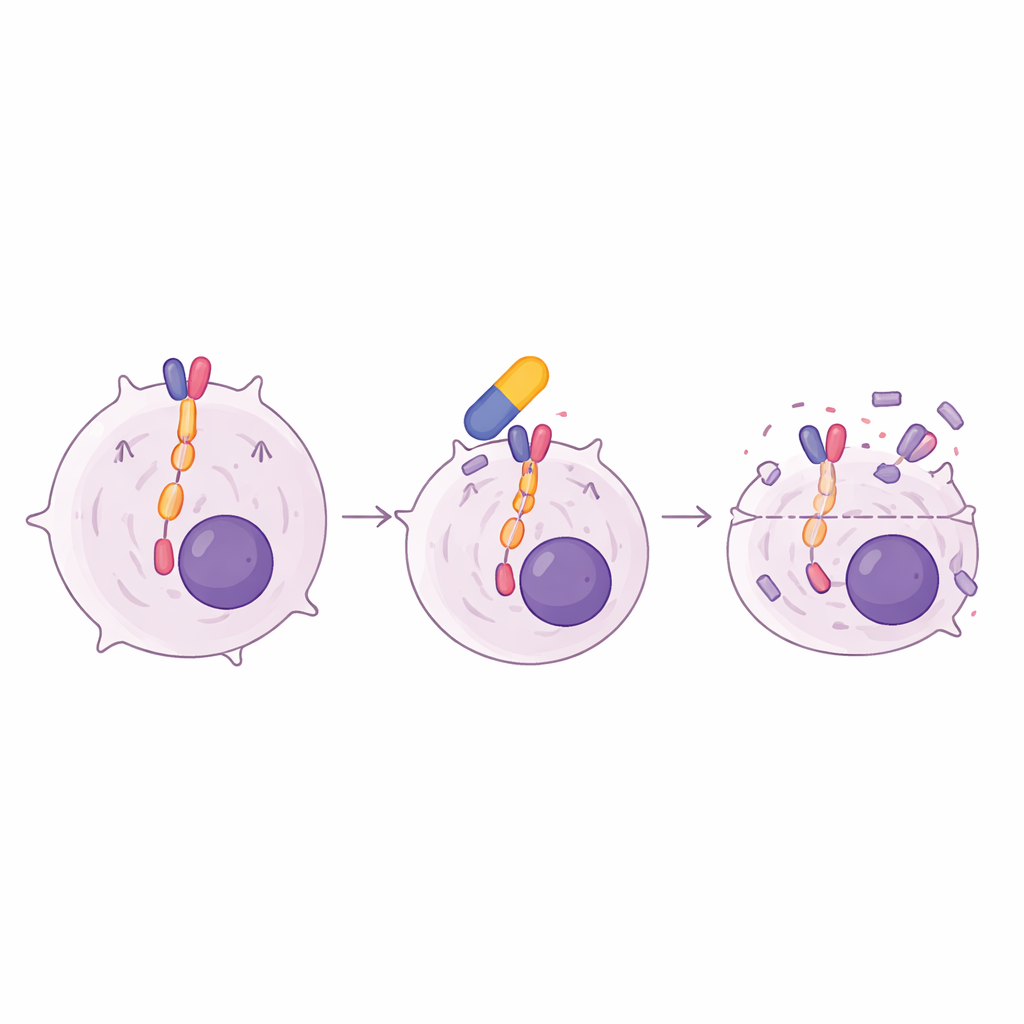
Verknüpfung von Laborergebnissen mit echten Patienten
Die Forschenden wandten sich dann Biopsieproben von Hunden mit kutanem Lymphom zu, die klinisch mit Oclacitinib behandelt worden waren. Mithilfe von Färbemethoden, die aktivierte Proteine sichtbar machen, stellten sie fest, dass Hunde, deren Tumoren aktiviertes JAK1 und STAT5 zeigten, eher partielle oder vollständige Ansprechen auf das Medikament hatten. Einige Nichtansprecher zeigten diese Signale dennoch, was darauf hindeutet, dass zusätzliche Umgehungswege bestimmte Tumoren erhalten können; insgesamt zeigte sich jedoch ein starker Zusammenhang. Wichtig ist, dass viele Lymphknoten‑ und Darmlymphomproben anderer Hunde dasselbe Aktivierungsmuster von JAK1/STAT5 aufwiesen, was die Möglichkeit nahelegt, dass Oclacitinib über das Hautlymphom hinaus bei einem breiteren Spektrum aggressiver hundlicher Lymphome Nutzen bringen könnte.
Was das für künftige Behandlungen bedeuten könnte
Zusammengefasst zeigt die Arbeit, dass Oclacitinib bestimmte hundliche Lymphomzellen direkt hemmen und manchmal abtöten kann, indem es einen zentralen Überlebensweg um JAK1 und STAT5 ausschaltet und die Aktivität wachstumsfördernder Gene wie c‑Myc senkt. Normale Lymphozyten gesunder Hunde waren bei klinisch relevanten Dosen deutlich weniger betroffen, wenngleich hohe Konzentrationen die Vermehrung aktivierter Immunzellen verlangsamten — ein Hinweis darauf, dass antitumorale Effekte gegen mögliche Immunsuppressionsrisiken abgewogen werden müssen. Die Studie legt nahe, dass das Testen von Tumoren auf aktiviertes JAK1 und STAT5 Tierärzt:innen helfen könnte, Hunde zu identifizieren, die am ehesten von Oclacitinib und ähnlichen Wirkstoffen profitieren. Obwohl weitere klinische Studien erforderlich sind, könnte dieses breit verfügbare Allergiemedikament Teil eines gezielten Behandlungsrepertoires für hundliche Lymphome werden, gesteuert durch einfache molekulare Marker.
Zitation: Harada, M., Inanaga, S., Sakurai, M. et al. The antitumor mechanism of oclacitinib in canine lymphoma. Sci Rep 16, 8427 (2026). https://doi.org/10.1038/s41598-026-40066-9
Schlüsselwörter: hundliches Lymphom, Oclacitinib, JAK1-STAT5-Signalweg, gezielte Krebstherapie, veterinäronkologie