Clear Sky Science · de
Tribolium castaneum mit längerer Dauer der tonischen Immobilität weist mehr Variationen im entsprechenden Genomabschnitt für die menschliche Parkinson-Krankheit auf
Warum ein winziger Käfer für Hirnerkrankungen wichtig ist
Parkinson-Krankheit ist vor allem für Zittern und Bewegungsstörungen bekannt, im Kern handelt es sich jedoch um eine Störung der Gehirnzellen, die den Neurotransmitter Dopamin nutzen. Diese Studie zeigt, dass ein häufiger Vorratsschädling, der rote Mehlkäfer, nach mehreren Zuchtgenerationen für eine ungewöhnliche anti‑räuberische Taktik — Totstellen — Merkmale entwickeln kann, die an Parkinson erinnern. Indem dieses auffällige Verhalten mit spezifischen Genveränderungen verknüpft wird, die denen in der Nähe menschlicher Parkinson‑Gene ähneln, legt die Arbeit nahe, dass selbst ein kleiner Käfer helfen kann, eine wichtige menschliche Hirnerkrankung besser zu verstehen.
Ein Käfer, der den Tod durch Stillstehen „betrügt”
Wenn sie von Fressfeinden angegriffen werden, lassen sich manche rote Mehlkäfer regungslos fallen und „spielen tot“ in einem Zustand, der tonische Immobilität genannt wird. Die Forscher züchteten zuvor zwei Stämme: einen, der lange regungslos bleibt (L‑Stamm), und einen, der schnell wieder zu sich kommt (S‑Stamm). Frühere Arbeiten zeigten, dass die lang totstellenden Käfer langsamer laufen, auffällige Gangmuster haben und geringere Dopaminspiegel im Gehirn tragen. Die Verabreichung von Dopamin oder sogar Koffein verkürzt ihre Totstellphasen. In der Natur überleben die langsam, lange totstellenden Käfer gegen bestimmte Spinnen und Raubwanzen besser, weil Bewegungsstillstand sie schwerer fassbar macht. So führt eine Überlebensstrategie in freier Wildbahn zu Käfern, die im Labor in ihrem Bewegungsverhalten überraschende Ähnlichkeiten mit Parkinson‑Patienten zeigen.
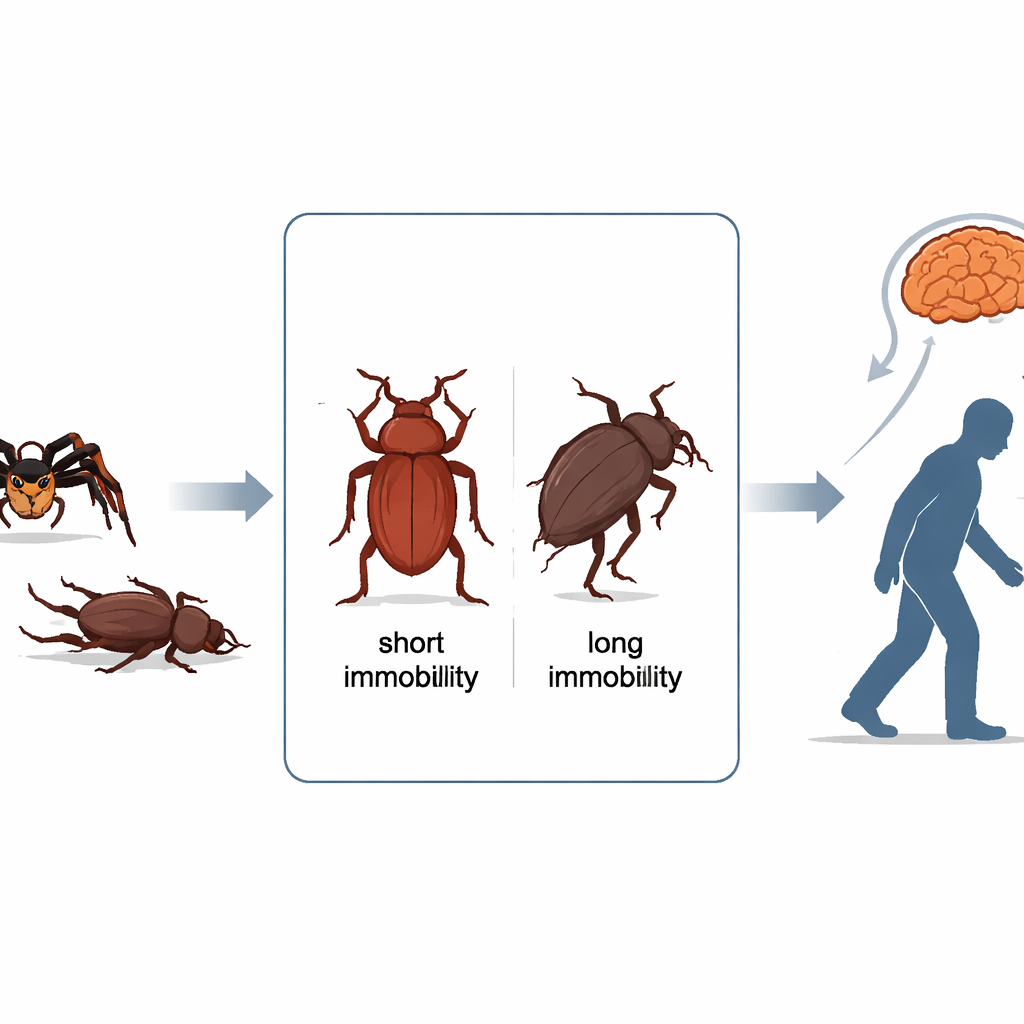
Das Käfer‑Genom nach Parkinson‑Echos absuchen
Um herauszufinden, ob diese Parkinson‑ähnlichen Merkmale mit genetischen Veränderungen zusammenhängen, die denen beim Menschen ähneln, verglich das Team die vollständigen DNA‑Sequenzen der lang‑ und kurz totstellenden Stämme. Sie suchten nach kleinen Änderungen im genetischen Code, größeren Einfügungen und Deletionen sowie Veränderungen in der Genkopienzahl. Anschließend fragten sie, welche dieser veränderten Käfergene eng mit menschlichen Genen übereinstimmen, die bereits mit Parkinson oder dem Dopaminsystem in Verbindung gebracht werden. Die Antwort war eindrücklich: Der lang totstellende Stamm trug deutlich mehr Mutationen in Käferversionen menschlicher Parkinson‑assoziierter Gene als der kurz totstellende Stamm. Dazu gehörten Gene, die an stressreaktiven „Chaperon“‑Proteinen beteiligt sind, und Gene der energieproduzierenden Maschinerie der Mitochondrien — beides zentrale Verdächtige bei der menschlichen Parkinson‑Erkrankung.
Von Genen zu Dopamin und Bewegung
Die Studie ging über rohe DNA‑Sequenzen hinaus und untersuchte, wie stark verschiedene Gene im Käferkörper ein- oder ausgeschaltet sind. Mithilfe früherer RNA‑Sequenzierungsdaten verbanden die Autoren Dutzende von Genen, die zwischen den Stämmen unterschiedlich waren, mit menschlichen Signalwegen für Monoamin‑Signalisierung — einer Familie von Botenstoffen, zu der auch Dopamin gehört. Bei den lang totstellenden Käfern zeigten Enzyme, die die Aminosäure Tyrosin in Dopamin umwandeln, veränderte Expressionsmuster und trugen subtile Sequenzveränderungen. Das deutet darauf hin, dass Dopamin in diesen Tieren anders produziert und verarbeitet wird. Außerdem entdeckten sie Unterschiede in Käfergenen, die mit Insulin und Zuckerstoffwechsel zusammenhängen und mit menschlichen und Fruchtfliegen‑Genen übereinstimmen, die mit Parkinson und Diabetes verknüpft sind — zwei Erkrankungen, die beim Menschen bereits als miteinander beeinflusst bekannt sind.
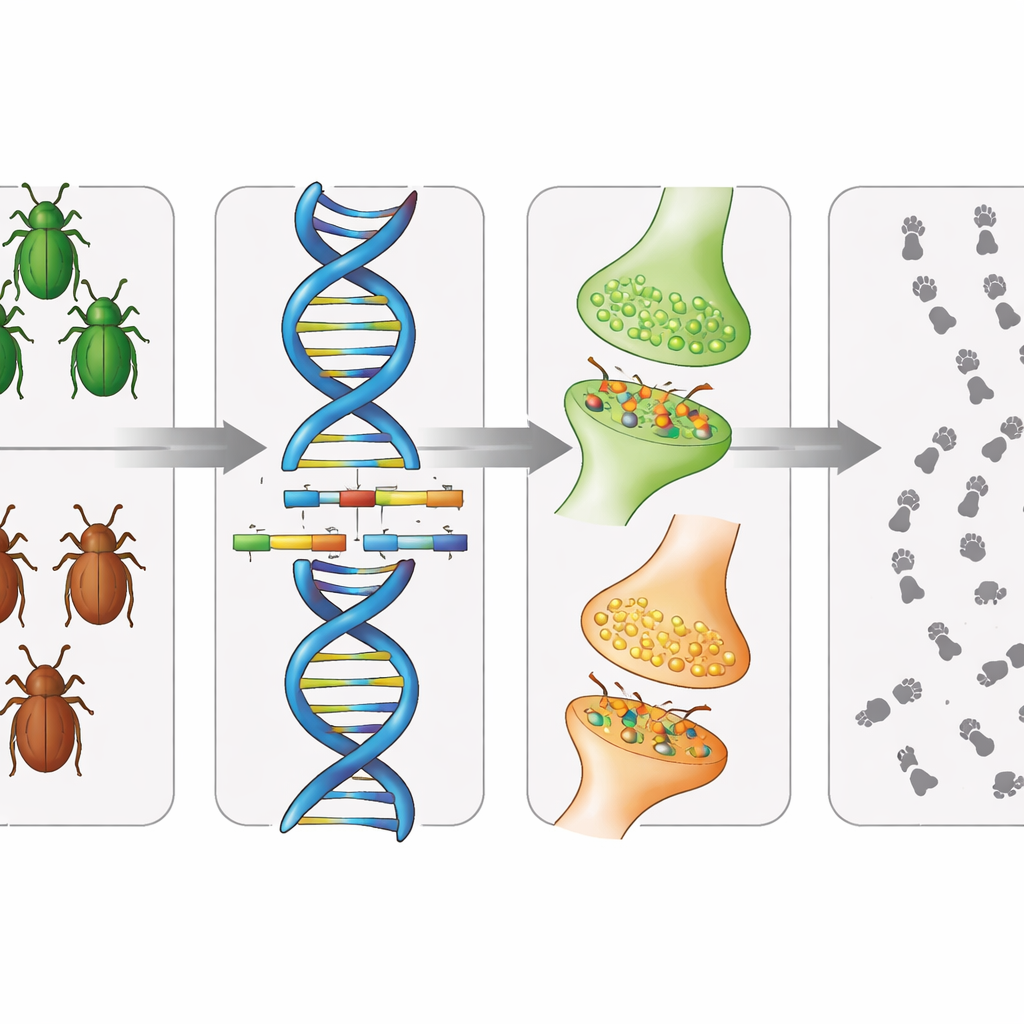
Ein Netzwerk von Signalen, kein einzelnes „Parkinson‑Gen”
Wichtig ist, dass die klassischen menschlichen Parkinson‑Gene wie LRRK2 und PINK1 bei diesen Käfern keine offensichtlichen Mutationen zeigten. Stattdessen scheint der lang totstellende Stamm eine Ansammlung von Veränderungen über viele Gene hinweg anzusammeln, die in die Dopamin‑Signalgebung, die mitochondriale Gesundheit, Stressantworten und Insulinwege hineinwirken. Netzwerk‑Analysen zeigten, dass diese Käfergene auf menschliche Signalwege abgebildet werden, die als verschiedene Parkinson‑Subtypen bezeichnet sind. Die Autoren argumentieren, dass dies die menschliche Situation widerspiegelt, in der Parkinson besser als ein Syndrom zu verstehen ist, das aus gestörten Netzwerken von Genen und zellulären Systemen entsteht, und nicht als Folge eines einzigen defekten Schalters.
Was das für Menschen und für Räuber bedeutet
Für Nicht‑Spezialisten lautet die Kernbotschaft: Ein durch Evolution geformtes Verhalten zur List gegenüber Fressfeinden kann unbeabsichtigt Merkmale einer menschlichen Hirnerkrankung nachbilden. Durch die Auswahl von Käfern nach der Dauer ihres „Totstellens“ erhielten Wissenschaftler Tiere, deren Gene und Hirnchemie wichtige Aspekte von Parkinson widerspiegeln — darunter niedrige Dopaminwerte, steife und veränderte Fortbewegung sowie Störungen in Energie‑ und Insulinsignalwegen. Obwohl diese Käfer nicht „an Parkinson leiden“, bieten sie ein einfaches, genetisch zugängliches Modell, um zu untersuchen, wie Veränderungen über viele Signalwege hinweg kombiniert werden, um Bewegung zu stören. Solche Modelle können Forschern helfen, Hypothesen zu testen, wie Stress, Stoffwechsel und Dopamin im menschlichen Gehirn interagieren, und letztlich neue Ansätze zur Vorbeugung oder Behandlung Parkinson‑ähnlicher Störungen informieren.
Zitation: Tanaka, K., Sasaki, K., Yajima, S. et al. Tribolium castaneum with longer duration of tonic immobility have more variations corresponding to the human Parkinson’s disease genomic region. Sci Rep 16, 8840 (2026). https://doi.org/10.1038/s41598-026-40050-3
Schlüsselwörter: Parkinson-Krankheit, Dopamin, Mehlkäfer (rote Mehlkäfer), tonische Immobilität, Insulinsignalisierung