Clear Sky Science · de
MyoFuse ist ein vollständig KI‑basiertes Workflow zur automatisierten Quantifizierung der Fusion von Skelettmuskelzellen in vitro
Warum das Zählen von Muskelzellen wichtig ist
Beim Sport, bei der Erholung nach Verletzungen oder bei Erkrankungen wie Diabetes remodeln sich unsere Skelettmuskeln ständig. Im Labor ahmen Forschende diesen Prozess nach, indem sie Muskelzellen in einer Schale wachsen lassen und beobachten, wie einzelne Zellen zu langen, mehrkernigen Fasern verschmelzen. Eine einfache Kennzahl, der Fusionsindex, sagt aus, wie gut diese Fusion verläuft. Heute wird diese Zahl meist dadurch ermittelt, dass Menschen per Hand tausende winziger Zellkerne auf dem Bildschirm zählen – eine langsame Arbeit, die uneinheitlich und fehleranfällig sein kann. Diese Studie stellt MyoFuse vor, einen vollständig KI‑gestützten Workflow, der diese Zählaufgabe automatisiert und darauf abzielt, die Muskel‑Forschung schneller, verlässlicher und weniger voreingenommen zu machen.
Die Herausforderung: wirklich sehen, was da ist
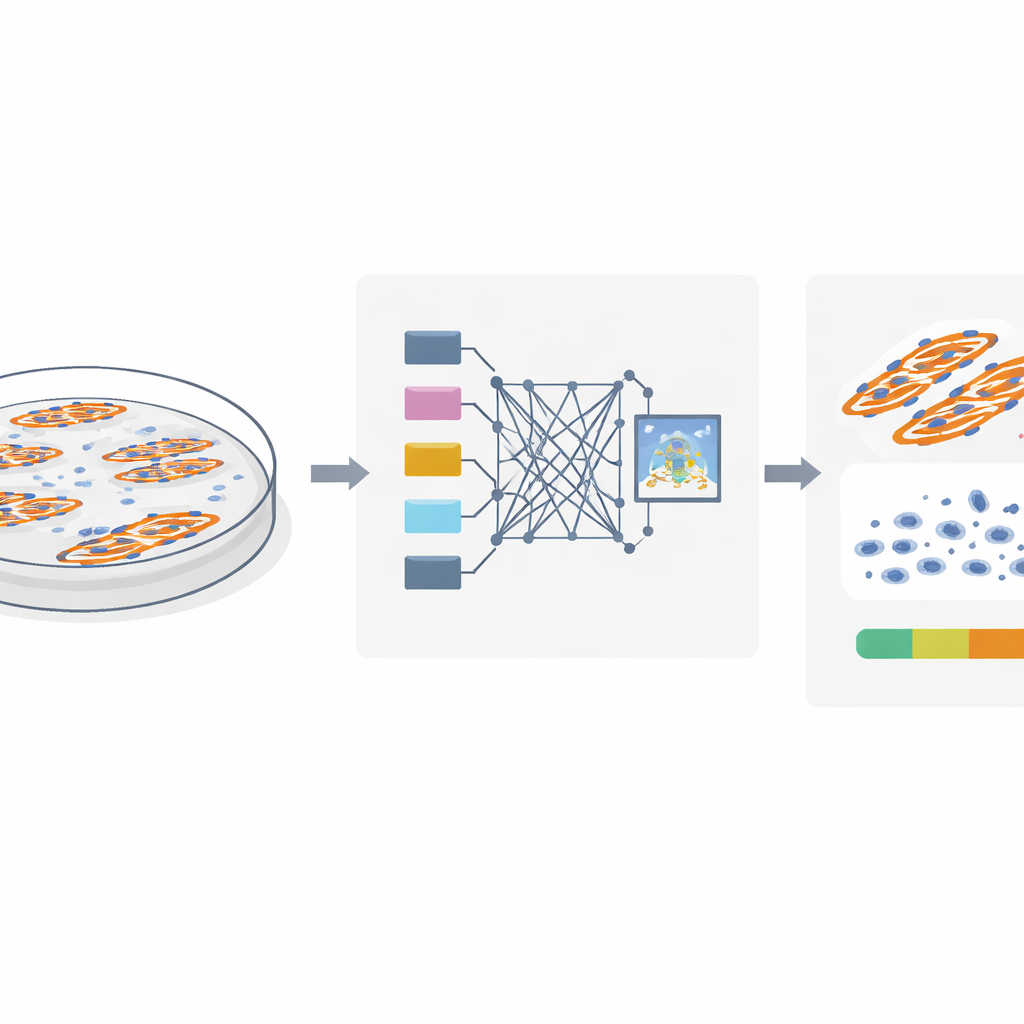
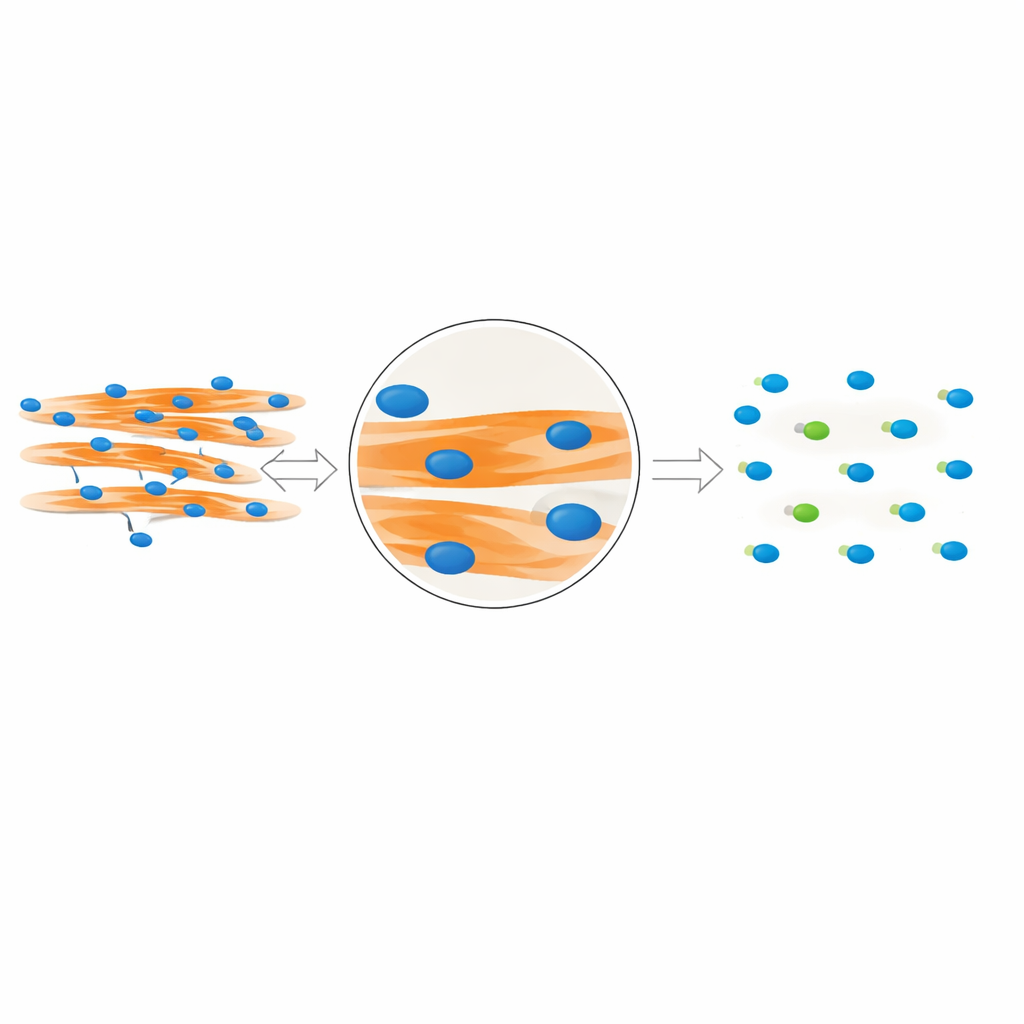
Um die Fusion von Muskelzellen zu untersuchen, färben Forschende Zellkerne und Muskelfasern mit fluoreszierenden Farbstoffen und erstellen Mikroskopaufnahmen. Die entscheidende Frage ist, welche Kerne tatsächlich innerhalb verschmolzener Muskelfasern liegen und welche zu unverschmolzenen Zellen in der Nähe gehören. Traditionelle Methoden gehen oft davon aus, dass ein Kern, der in einem zweidimensionalen Bild mit einer Muskelfaser überlappt, zwangsläufig Teil dieser Faser sein muss. Zellen wachsen jedoch in drei Dimensionen: Ein Kern kann oberhalb oder unterhalb einer Faser liegen und in der Aufnahme dennoch überlappend erscheinen. Die Autorinnen und Autoren zeigen mithilfe detaillierter konfokaler Bilder von Maus‑ und humanen Muskelzellen, dass dieser Überlappungs‑Trick irreführend sein kann und viele nahegelegene Kerne fälschlich als Bestandteil verschmolzener Fasern zählt, wodurch der Fusionsindex aufgebläht wird.
Ein klügerer Weg, fluoreszierende Bilder zu lesen
Das Team erkannte, dass echte „in‑Faser“‑Kerne einen charakteristischen visuellen Fingerabdruck hinterlassen. Weil diese Kerne physisch Raum innerhalb der Faser einnehmen, erzeugen sie kleine dunkle Lücken im Fluoreszenzsignal, das für das Muskelprotein MyHC markiert ist. Im Gegensatz dazu stören Kerne, die oberhalb oder unterhalb einer Faser liegen, dieses Signal nicht. Aufbauend auf dieser Erkenntnis entwickelten die Autorinnen und Autoren MyoFuse, einen zweistufigen KI‑Workflow. Zuerst umreißt ein spezialisiertes Segmentierungsmodell (angepasst aus dem Open‑Source‑Tool Cellpose) einzelne Kerne präzise, selbst wenn sie dicht zu Clustern gepackt sind. Anschließend prüft ein leichtgewichtiges neuronales Netz für jeden Kern das umgebende MyHC‑Signal und entscheidet, ob er sich innerhalb einer Muskelfaser befindet oder außerhalb — basierend ausschließlich auf diesem lokalen Muster statt auf einfacher Überlappung.
Wie gut die KI mit menschlichen Expertinnen und Experten übereinstimmt
Die Forschenden testeten MyoFuse rigoros an Bildern von Maus‑C2C12‑Muskelzellen und primären humanen Muskelzellen aus verschiedenen Muskeln. Für beide Spezies stimmten die KI‑Zählung der Gesamtkerne und der berechnete Fusionsindex sehr gut mit sorgfältigen manuellen Annotationen durch Expertinnen und Experten überein, mit nahezu perfekten Korrelationen. Auf der Ebene einzelner Kerne unterschied der Klassifikator in mehr als 90 % der Fälle korrekt zwischen Kernen innerhalb und außerhalb von Fasern in den untersuchten Datensätzen und erreichte Leistungskennwerte, die an menschliches Niveau heranreichen. Wichtig ist, dass MyoFuse auch bei einer separaten Gruppe menschlicher Zellen, die nie im Training verwendet wurden, gut funktionierte — ein Hinweis darauf, dass der Ansatz auf neue Proben generalisieren kann und nicht nur die Trainingsbilder auswendig lernt.
Verborgene Verzerrungen gängiger Methoden offenlegen
Über seine Genauigkeit hinaus deckte MyoFuse systematische Probleme in weit verbreiteten maskenbasierten Methoden auf, die auf einfacher Überlappung von Kern‑ und Fasernsiganlen beruhen. Beim Vergleich der Fusionsindizes von MyoFuse mit denen einer verfeinerten Maskenmethode auf denselben Bildern überschätzte die Maskenmethode konstant die Fusion, insbesondere in Bereichen, in denen Muskelfasern einen größeren Anteil der Fläche bedeckten. Eine Anpassung der Erkennungs‑Schwellen veränderte zwar die Zahlen, beseitigte aber nicht diese zugrunde liegende Verzerrung; scheinbare Verbesserungen ergaben sich oft dadurch, dass sich Fehler gegenseitig aufhoben, statt dass die Biologie besser abgebildet wurde. Das Team zeigte außerdem, dass die Fusionsschätzungen innerhalb unterschiedlicher Regionen einer einzigen Vertiefung stark schwanken können, was verdeutlicht, dass die Analyse nur einiger handverlesener Felder ein verzerrtes Bild davon liefern kann, wie gut die Zellen tatsächlich verschmelzen.
Was das für die zukünftige Muskel‑Forschung bedeutet
MyoFuse bietet Muskelbiologinnen und ‑biologen eine Möglichkeit, die Zellfusion schneller und treuer zu messen gegenüber dem, was wirklich in der Schale passiert. Durch die Kombination automatisierter Mikroskopie mit einer KI, die hunderte von tausenden Kernen in Minuten segmentieren und klassifizieren kann, reduziert der Workflow die menschliche Arbeitslast, minimiert subjektive Entscheidungen darüber, wo man hinschaut und wie man Bilder schwellenwertet, und vermeidet das Zählen benachbarter Zellen als verschmolzene Muskulatur. Die Autorinnen und Autoren räumen ein, dass extrem ungewöhnliche Bildbedingungen oder stark abweichende Färbeprotokolle ein Retraining erforderlich machen könnten, aber die Methode ist offen verfügbar und darauf ausgelegt, anpassbar zu sein. Für Labore, die Muskelentwicklung, Alterung, Regeneration oder stoffwechselbedingte Erkrankungen untersuchen, verspricht MyoFuse robustere Fusionsmessungen — und damit verlässlichere Schlussfolgerungen darüber, wie Muskeln wachsen und sich verändern.
Zitation: Lair, B., Cazorla, C., Lobeto, A. et al. MyoFuse is a fully AI-based workflow for automated quantification of skeletal muscle cell fusion in vitro. Sci Rep 16, 9387 (2026). https://doi.org/10.1038/s41598-026-40047-y
Schlüsselwörter: Skelettmuskel, Zellfusion, künstliche Intelligenz, Bildanalyse, Myogenese