Clear Sky Science · de
Hochleistungs-Au–MoS₂–Graphen-Mehrschicht-SPR-Biosensor mit überlegener Empfindlichkeit und Präzision
Warum dieser winzige Sensor wichtig ist
Ärztinnen und Ärzte, Umweltwissenschaftler und auch Lebensmittelkontrolleure benötigen Werkzeuge, die winzige Mengen an Chemikalien oder Biomolekülen schnell und zuverlässig nachweisen können. Diese Arbeit stellt einen neuen optischen Sensor vor, der aus ultradünnen Schichten Gold und fortschrittlichen 2D‑Materialien aufgebaut ist und extrem kleine Änderungen in flüssigen Proben wie Blut, Zuckerlösungen oder wässerigen Pufferlösungen detektieren kann. Indem Licht in einen Nanometerbereich an einer Metalloberfläche gedrückt wird, verspricht das Gerät schnellere und präzisere Tests für Krankheitsmarker und Schadstoffe.
Dem Licht an einer Oberfläche lauschen
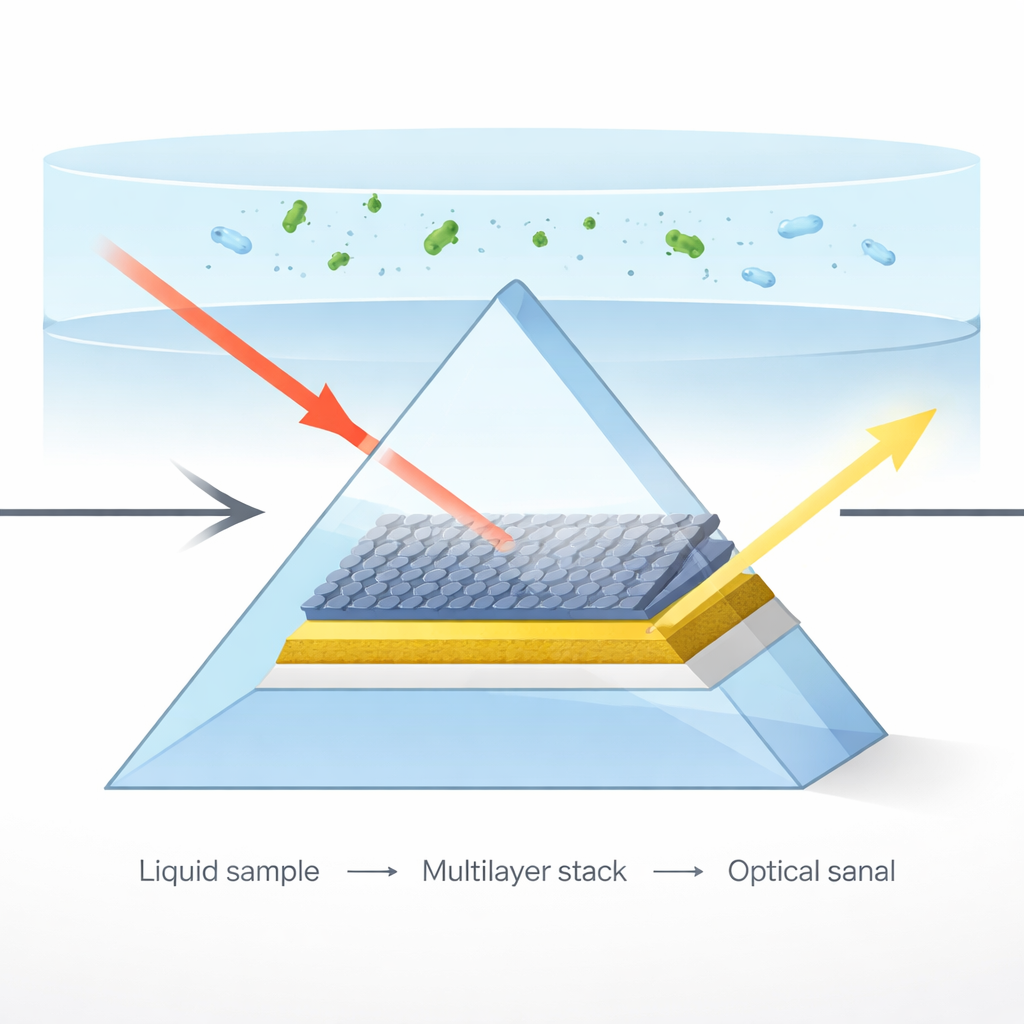
Der Sensor beruht auf dem Phänomen der Oberflächenplasmonresonanz, bei dem Licht an einer Metalloberfläche entlangschreitet und sich mit Elektronenwellen an dieser Grenze koppelt. Sobald eine Flüssigkeitsprobe diese Oberfläche berührt, verschiebt bereits eine winzige Änderung der optischen Eigenschaften der Flüssigkeit den Winkel, bei dem die Resonanz auftritt. Durch das Durchscheinen eines Lasers durch ein Glasprisma auf einen dünnen Goldfilm und das Beobachten des reflektierten Lichts kann das Gerät diese Verschiebungen in Informationen darüber übersetzen, was in der Flüssigkeit gelöst ist, etwa die Zuckerkonzentration oder Veränderungen in der Blutzusammensetzung.
Smartes Materialstapeln für stärkere Signale
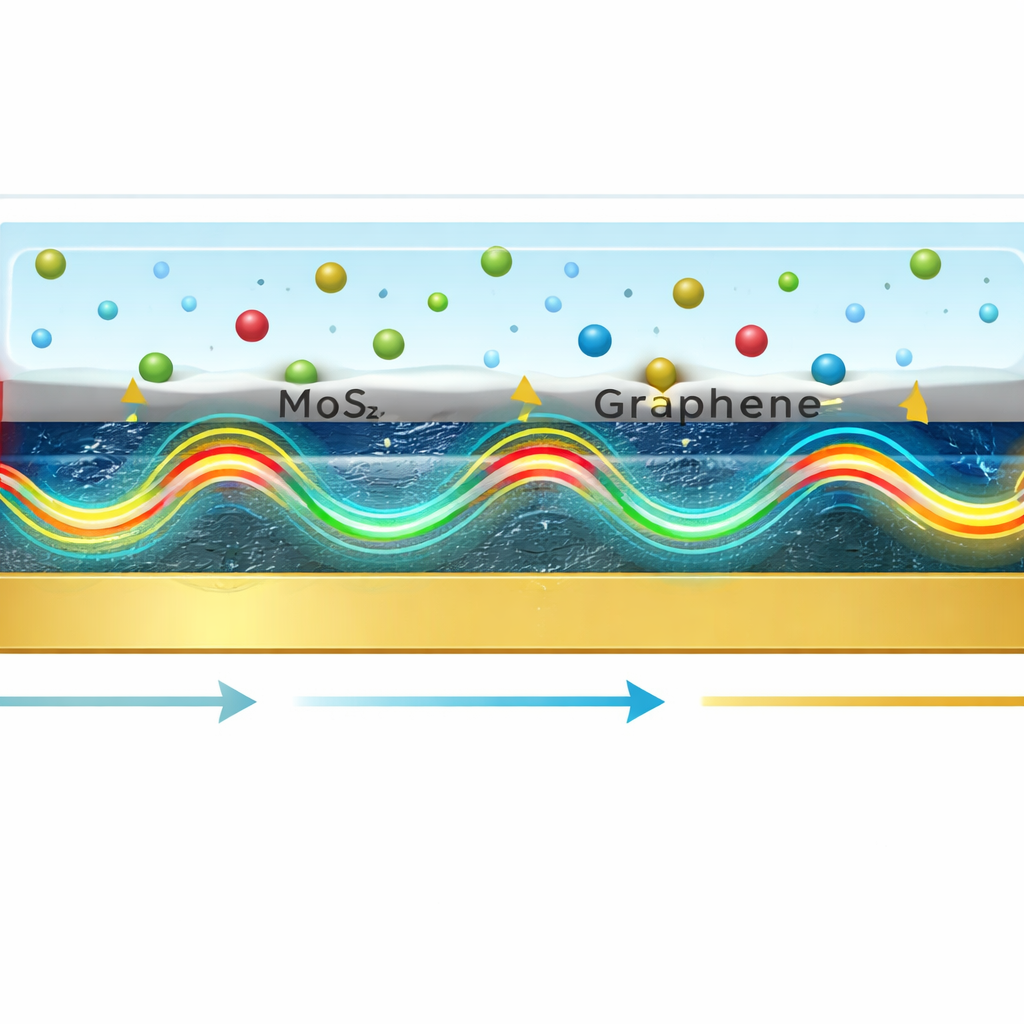
Statt nur blankes Gold zu verwenden, entwarfen die Forschenden einen Mehrschichtaufbau: ein Glasprisma, ein Goldfilm, einige atomare Schichten Molybdändisulfid (MoS₂) und drei Graphenlagen, wobei die Prüf‑Flüssigkeit obenauf liegt. Jedes Material erfüllt eine bestimmte Aufgabe. Gold startet effizient die Oberflächen‑Elektronenwellen. MoS₂ mit seiner hohen optischen Dichte und starken Lichtwechselwirkung komprimiert und konzentriert das elektromagnetische Feld nahe der Oberfläche. Graphen bietet eine enorme Oberfläche, an der Moleküle haften können, sowie ausgezeichnete elektrische und optische Eigenschaften, die die Licht‑Materie‑Wechselwirkung weiter verstärken. Computersimulationen zeigten, dass eine Anordnung mit fünf MoS₂‑Schichten und drei Graphenlagen das intensivste und am schärfsten begrenzte Feld an der Sensoroberfläche erzeugte.
Winzige Änderungen in klare Messergebnisse verwandeln
Um die Leistung zu bewerten, simulierte das Team, wie sich der reflektierte Lichtwinkel verschiebt, wenn der Sensor verschiedenen Flüssigkeiten ausgesetzt ist: Standardlaborpuffer (PBS), Saccharoselösung, Blut und Glycerin. Sie berechneten mehrere Kennzahlen, die zusammen beschreiben, wie gut der Sensor arbeitet—wie groß die Winkelverschiebung für eine gegebene Änderung im Medium ist, wie schmal und scharf der Resonanzdip erscheint und wie präzise kleine Verschiebungen unterschieden werden können. Über alle getesteten Proben erreichte der Sensor Empfindlichkeiten nahe 80 Grad pro Brechungsindex‑Einheit, mit besonders hoher Präzision bei Saccharose und Glycerin, wo die Resonanzmerkmale sehr eng waren. Diese Werte entsprechen vielen zuvor berichteten Mehrschichtsensoren oder übertreffen sie und zeigen, dass der Drei‑Material‑Aufbau reale Vorteile in Empfindlichkeit und Messklarheit bietet.
Die Schichten für beste Leistung abstimmen
Die Autorinnen und Autoren untersuchten außerdem, wie sich die Dicke der Graphen‑ und MoS₂‑Schichten auf das Signal auswirkt. Sehr dünnes Graphen bringt das begrenzte Lichtfeld nahe an die Flüssigkeit und erhöht die Empfindlichkeit, während zu dickes Graphen das Feld nach innen verschiebt und die Antwort abschwächt. Ein ähnliches Gleichgewicht gilt für MoS₂: Einige zusätzliche Schichten verstärken die Feldkonfinierung, aber jenseits einer optimalen Dicke dämpft zusätzliche Absorption die Resonanz und verbreitert das Signal. Die Simulationen betrachteten außerdem, wie unterschiedliche Einfallswinkel und Wellenlängen die Empfindlichkeit beeinflussen, und identifizierten Bereiche, in denen das Gerät am stärksten auf kleine Änderungen in der Probe reagiert.
Vom Computermodell zu Tests in der Praxis
Obwohl diese Arbeit auf numerischen Modellen basiert, diskutieren die Autorinnen und Autoren realistische Fertigungswege unter Verwendung standardisierter Techniken zum Aufbringen von Gold sowie zum Wachsen oder Übertragen von MoS₂ und Graphen. Sie heben praktische Herausforderungen hervor—etwa die extrem glatte Oberflächengestaltung, die Kontrolle der Schichtdicken im Nanometerbereich und das Vermeiden von Falten, Oxidation oder Ablösung der empfindlichen 2D‑Materialien. Mit sorgfältiger Kontrolle dieser Schritte und der Integration in mikrofluidische Kanäle zur Handhabung winziger Flüssigkeitsvolumina argumentieren sie, dass der Mehrschichtsensor im Labor hergestellt und eingesetzt werden könnte.
Was das für den Alltag bedeutet
Kurz gesagt zeigt diese Studie, wie das sorgfältige Stapeln dreier fortschrittlicher Materialien einen bekannten optischen Effekt in ein leistungsfähiges chemisches „Ohr“ verwandeln kann, das leise Signale von Veränderungen in komplexen Flüssigkeiten wahrnimmt. Die Goldschicht startet das Signal, MoS₂ verstärkt und fokussiert es, und Graphen bietet eine geeignete Oberfläche für Zielmoleküle; zusammen liefern sie schärfere, empfindlichere Messungen als viele frühere Designs. Wenn solche Sensoren experimentell realisiert werden, könnten sie Ärzten helfen, Krankheitsmarker früher zu erkennen, schnellere Qualitätskontrollen in der Lebensmittel‑ und Pharmaindustrie ermöglichen und tragbare Systeme zur Überwachung von Wasserverunreinigungen bereitstellen—alles durch Beobachtung, wie ein schmaler Lichtstrahl von einer konstruierten Oberfläche reflektiert wird, die nur wenige Nanometer dick ist.
Zitation: Bahmani, E., Kaatuzian, H. & Shafagh, S.G. High-performance Au–MoS₂–graphene multilayer SPR biosensor with superior sensitivity and precision. Sci Rep 16, 8428 (2026). https://doi.org/10.1038/s41598-026-39993-4
Schlüsselwörter: Oberflächenplasmonresonanz, Biosensor, Graphen, MoS2, Brechungsindex-Sensorik