Clear Sky Science · de
Caldesmon-1–vermittelte Aktin-Dynamik ist essentiell für die osteogene Differenzierung von Aortenklappen-interstitiellen Zellen
Warum die Versteifung der Herzklappe wichtig ist
Mit dem Alter kann eines der Haupttore des Herzens – die Aortenklappe – allmählich steif und nahezu steinartig werden. Dieser Zustand, Aortenstenose genannt, zwingt das Herz zu stärkerer Pumparbeit und kann zu Herzversagen führen. Gegenwärtig sind chirurgische oder katheterbasierte Klappenersatzverfahren die einzigen verlässlichen Behandlungen. Die hier zusammengefasste Studie stellt eine grundlegende, aber entscheidende Frage: Was lässt das weiche, flexible Gewebe der Klappe schrittweise in knochenähnliches Material übergehen? Indem sie einen zentralen molekularen Akteur in diesem Prozess aufdeckt, weist die Forschung in Richtung zukünftiger Medikamente, die das Fortschreiten der Klappenverkalkung verlangsamen oder verhindern könnten, statt die geschädigte Klappe nur zu ersetzen.
Ein genauerer Blick auf die verborgenen Helfer der Klappe
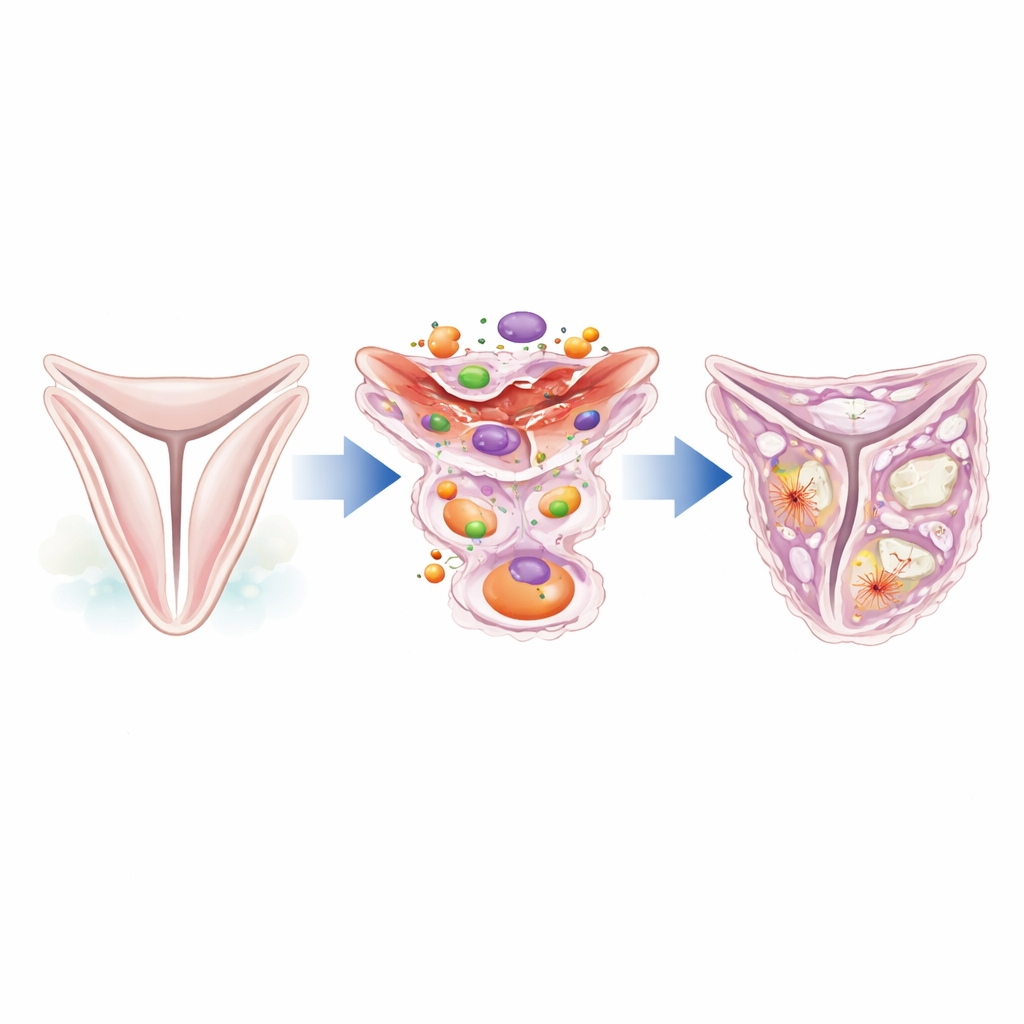
Die Segel der Aortenklappe werden von einer dünnen Schicht spezialisierter Stützzellen getragen, die als Klappen-interstitielle Zellen bekannt sind. In einer gesunden Klappe bleiben diese Zellen ruhig und tragen zur Erhaltung der Gewebestruktur bei. Unter Stress oder nach Verletzung können sie jedoch ihre Identität ändern und sich wie narbenbildende Zellen oder sogar wie knochenbildende Zellen verhalten. Die Autorinnen und Autoren konzentrierten sich auf ein Protein namens Caldesmon-1, das die interne Zellgerüste aus Aktinfilamenten mitsteuert. Durch Auswertung vorhandener Einzelzell-RNA-Sequenzierungsdaten aus menschlichen Klappen fanden sie, dass Caldesmon-1 in Klappen von Patienten mit Aortenstenose deutlich erhöht ist im Vergleich zu normalen Klappen, insbesondere in interstitiellen Zellen, die in verdickten, fibrotischen Regionen vorkommen.
Vom flexiblen Gewebe zu fibrotischen und knochenähnlichen Bereichen
Mikroskopische Untersuchungen menschlicher Klappenproben zeigten, dass Caldesmon-1-Protein in erkrankten Segeln reichlich vorhanden ist und mit Markern aktivierter, kontraktiler Zellen sowie fibroblastähnlicher Zellen, die Kollagen produzieren, übereinstimmt. Diese Caldesmon-1‑reichen Zellen gruppieren sich um Bereiche von Fibrose und frühen Verkalkungen, was darauf hindeutet, dass sie beim Aufbau der zusätzlichen Matrix mitwirken, die die Klappe verdickt. Weitere Analysen zeigten, dass diese Zellen Gene exprimieren, die typisch sind für glattmuskelähnliche und knochengeneigte Zelltypen, und dass sie Hauptproduzenten von Strukturproteinen wie Typ‑I‑Kollagen sind. Anders gesagt: Wo immer die Klappe versteift und vernarbt, sind Caldesmon-1-positive interstitielle Zellen vor Ort.
Wie ein formgebendes Protein Zellen in Richtung Knochen treibt
Um Ursache und Wirkung zu klären, isolierte das Team menschliche klappen-interstitielle Zellen und setzte small interfering RNA ein, um Caldesmon-1 herunterzuregulieren. Ohne dieses Protein verloren die Zellen ihre längliche, spindelförmige Gestalt und wurden runder. Ihre inneren Aktinfilamente wurden dünner, und ihre Fähigkeit zur Teilung sowie zur gerichteten Bewegung nahm ab. Unter einem osteogenen, also knochenfördernden Kulturmedium bildeten normale Zellen problemlos Kalziumablagerungen, während Caldesmon-1‑reduzierte Zellen deutlich weniger Mineralisierung zeigten. Umfangreiche RNA-Sequenzierungen bestätigten, dass viele Gene, die an der Knochenbildung und Gewebsremodellierung beteiligt sind, darunter bekannte osteogene Treiber wie RUNX2 und alkalische Phosphatase, unter osteogenen Bedingungen stark hochreguliert wurden, aber nicht anstiegen, wenn Caldesmon-1 abgeschwächt war.
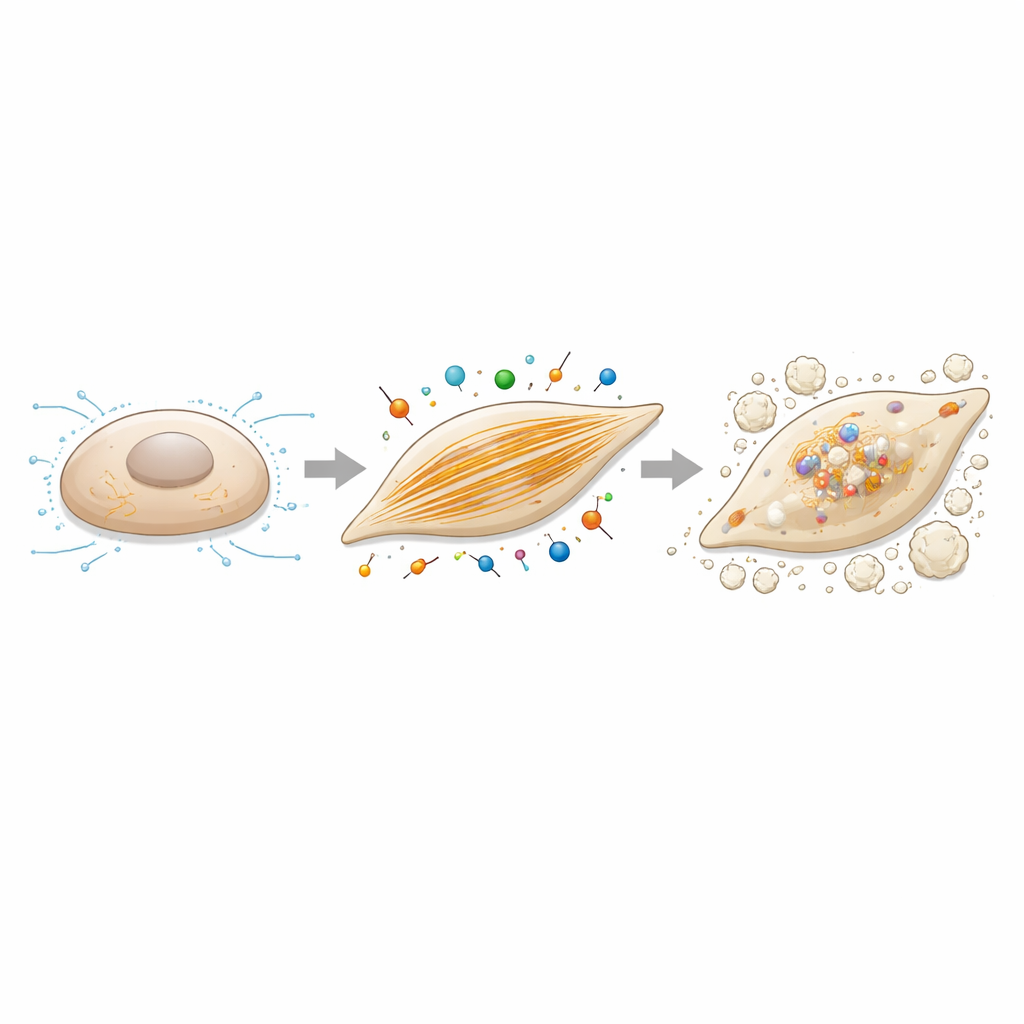
Aktinfilamente als Steuerhebel für Verkalkung
Da Caldesmon-1 ein Aktinregulator ist, untersuchten die Autorinnen und Autoren, ob eine Veränderung der Aktinmontage selbst die Neigung der Zellen zur Verkalkung beeinflusst. Sie behandelten die klappen-interstitiellen Zellen mit Cytochalasin B, einer Verbindung, die das Wachstum von Aktinfilamenten schonend stört, während sie die gleichen knochenfördernden Kulturbedingungen anwandten. In Dosen, die das Überleben der Zellen nicht ernsthaft beeinträchtigten, reduzierte diese Behandlung die Kalziumablagerungen stark und senkte die Expression knochenbildungsbezogener Gene, einschließlich Caldesmon-1 und RUNX2. Zusammen mit den Knockdown-Experimenten ergibt sich ein stimmiges Bild: Robuste Aktinfilament-Netzwerke und die von ihnen getragenen kontraktilen Kräfte sind nicht bloße Zuschauer – sie treiben aktiv den Wechsel von ruhenden Stützzellen zu knochenbildenden Zellen in der Klappe voran.
Was das für künftige Therapien bedeutet
Für Laien lautet die Kernbotschaft, dass die Versteifung der Aortenklappe ein aktiver, regulierter Prozess ist und kein bloßer „Verschleiß“. Diese Studie identifiziert Caldesmon-1 als zentralen Koordinator, der das innere Gerüst der Zelle mit dem genetischen Programm für die Bildung knochenähnlichen Gewebes verknüpft. Indem Caldesmon-1 den klappen-interstitiellen Zellen hilft, eine kontraktile, fibrotische und letztlich osteogene Identität anzunehmen, trägt es direkt zum Aufbau harter Ablagerungen bei, die die Klappe verengen. Obwohl jede Therapie, die dieses Protein oder die Aktin-Dynamik anvisiert, sorgfältig geprüft werden muss, um unerwünschte Effekte in anderen Geweben zu vermeiden, heben Caldesmon-1-vermittelte Wege nun vielversprechende Kandidaten für Medikamente hervor, die die Klappenverkalkung verlangsamen oder stoppen könnten, bevor ein chirurgischer Eingriff notwendig wird.
Zitation: Komoda, M., Sakaue, T., Nakao, Y. et al. Caldesmon-1–mediated actin dynamics is essential for osteogenic differentiation of aortic valve interstitial cells. Sci Rep 16, 9385 (2026). https://doi.org/10.1038/s41598-026-39938-x
Schlüsselwörter: Aortenklappenverkalkung, Caldesmon-1, Klappen-interstitielle Zellen, Aktin-Zytoskelett, osteogene Differenzierung