Clear Sky Science · de
RBP4 wirkt der Progression von Plattenepithelkarzinom der Zunge entgegen, indem es den PI3K/AKT-Signalweg hemmt und die M1-Polarisation von Makrophagen fördert
Warum Zungenkrebs neue Ansätze braucht
Zungenkrebs kann Menschen die Fähigkeit zu sprechen, zu essen und zu schmecken rauben, und trotz Operation, Chemotherapie und Bestrahlung bleiben die Langzeitüberlebensraten häufig enttäuschend. Diese Studie untersucht einen unerwarteten Helfer im Blut, ein Vitamin‑A‑transportierendes Protein namens RBP4, und zeigt, wie es sowohl das Wachstum von Zungentumoren verlangsamen als auch die körpereigenen Immunverteidiger mobilisieren kann. Indem die Forscher aufdecken, wie dieses Molekül innerhalb von Krebszellen und in den umgebenden Immunzellen wirkt, weisen die Ergebnisse auf neue Strategien hin, die eines Tages Behandlungen wirksamer und weniger schädlich machen könnten.
Ein verborgenes Protein in Zungentumoren
Die Forschenden begannen damit, große Krebsgen‑Datenbanken zu durchforsten, um zu ermitteln, welche immunbezogenen Gene vorhersagen könnten, wie Patienten mit Plattenepithelkarzinom der Zunge langfristig abschneiden. Unter Hunderten von Kandidaten erwies sich RBP4, ein Protein, das vor allem für den Transport von Vitamin A im Blut bekannt ist, als besonders interessant. Beim Vergleich von Tumorproben mit nahegelegenem gesundem Zungengewebe fanden sie, dass die RBP4‑Spiegel im Krebs durchgängig deutlich niedriger waren. Dieses Muster bestätigte sich in mehreren unabhängigen Datensätzen und in Gewebeproben von 20 Patientinnen und Patienten, was darauf hindeutet, dass der Verlust von RBP4 ein häufiges Merkmal dieser Erkrankung ist.
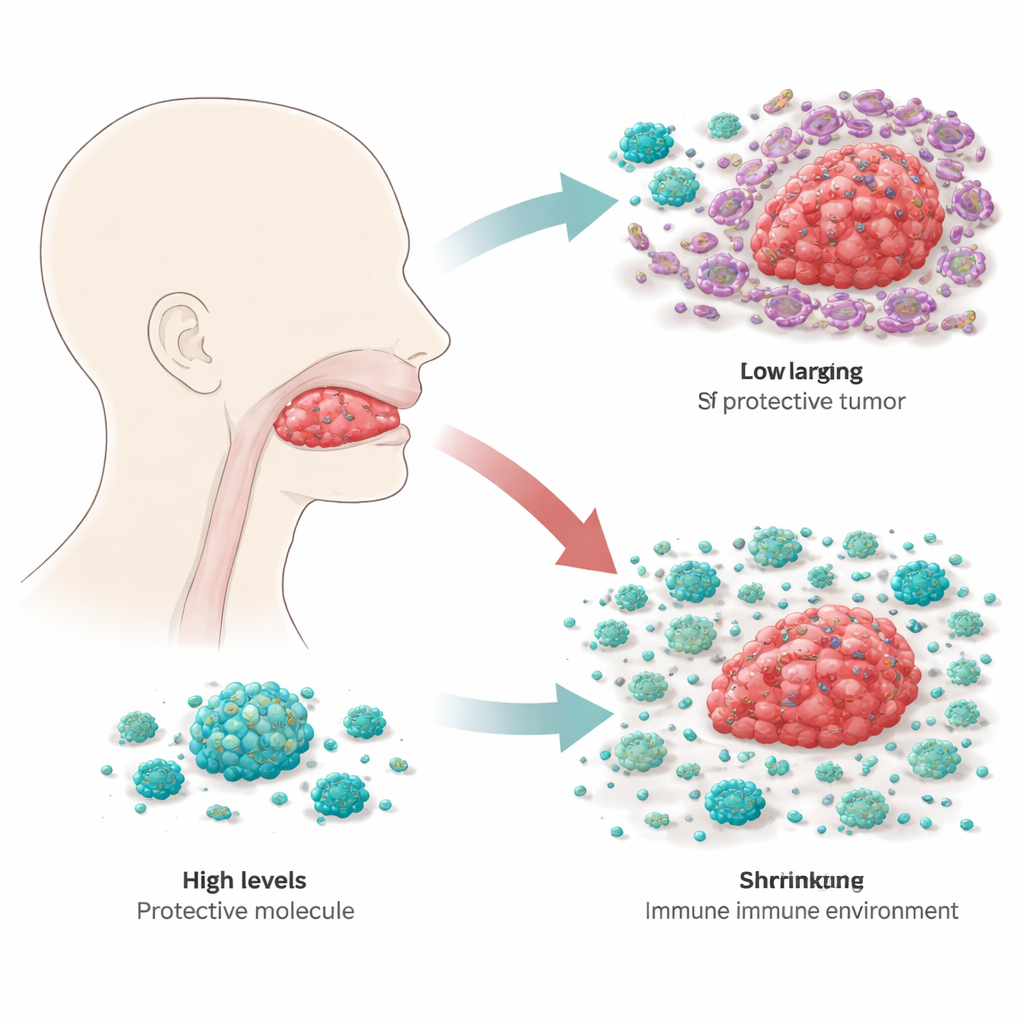
Wachstumshemmung von innen
Um herauszufinden, was RBP4 in Zungenkrebszellen tatsächlich bewirkt, veränderten die Wissenschaftler Tumorzelllinien so, dass sie entweder zusätzliches RBP4 produzieren oder deutlich weniger davon herstellen. In Zellkultur wuchsen Zellen mit erhöhtem RBP4 langsamer, während solche mit reduziertem RBP4 schneller teilten und sich besser bewegten sowie in künstlichen Membranen eindrangen—Verhalten, das mit Metastasierung und Rückfällen in Verbindung steht. Wurden diese veränderten Zellen in Mäuse implantiert, blieben Tumoren mit zusätzlichem RBP4 kleiner, während Tumoren mit reduziertem RBP4 aggressiver wuchsen. Durch die Verfolgung zentraler Wachstumssteuerungs‑Schalter innerhalb der Zellen zeigte das Team, dass RBP4 einen wichtigen Wachstumsweg namens PI3K–AKT–mTOR dämpft, auf den sich viele Krebsarten als inneren Beschleuniger stützen. Bei hohem RBP4 ist dieser Weg leiser, und Tumorzellen sind weniger fähig, den flexiblen, mobilen Zustand anzunehmen, der ihnen die Migration erleichtert.
Immunzellen zu Tumorkämpfern machen
Krebs wächst nicht isoliert; er lebt in einer Nachbarschaft aus Immunzellen, Blutgefäßen und Stützgewebe, der sogenannten Tumormikroumgebung. Hier spielen Makrophagen—große Immunzellen, die entweder Tumore angreifen oder unterstützen können—eine zentrale Rolle. Die Forschenden bemerkten, dass Tumoren mit mehr RBP4 auch tendenziell mehr Makrophagen des Typs „M1“ enthielten, die mit Entzündung und Tumorzellabtötung assoziiert sind, statt des „M2“-Typs, der häufig das Tumorwachstum fördert. In Zellkultur verschoben sich Makrophagen, die entweder zu reinem RBP4 ausgesetzt wurden oder mit Zungenkrebszellen kultiviert wurden, die mehr RBP4 sezernierten, hin zu diesem M1‑, tumorbekämpfenden Zustand. Wurde RBP4 in den Krebszellen reduziert, neigten die Makrophagen stattdessen zu einem tumorfreundlicheren Profil.
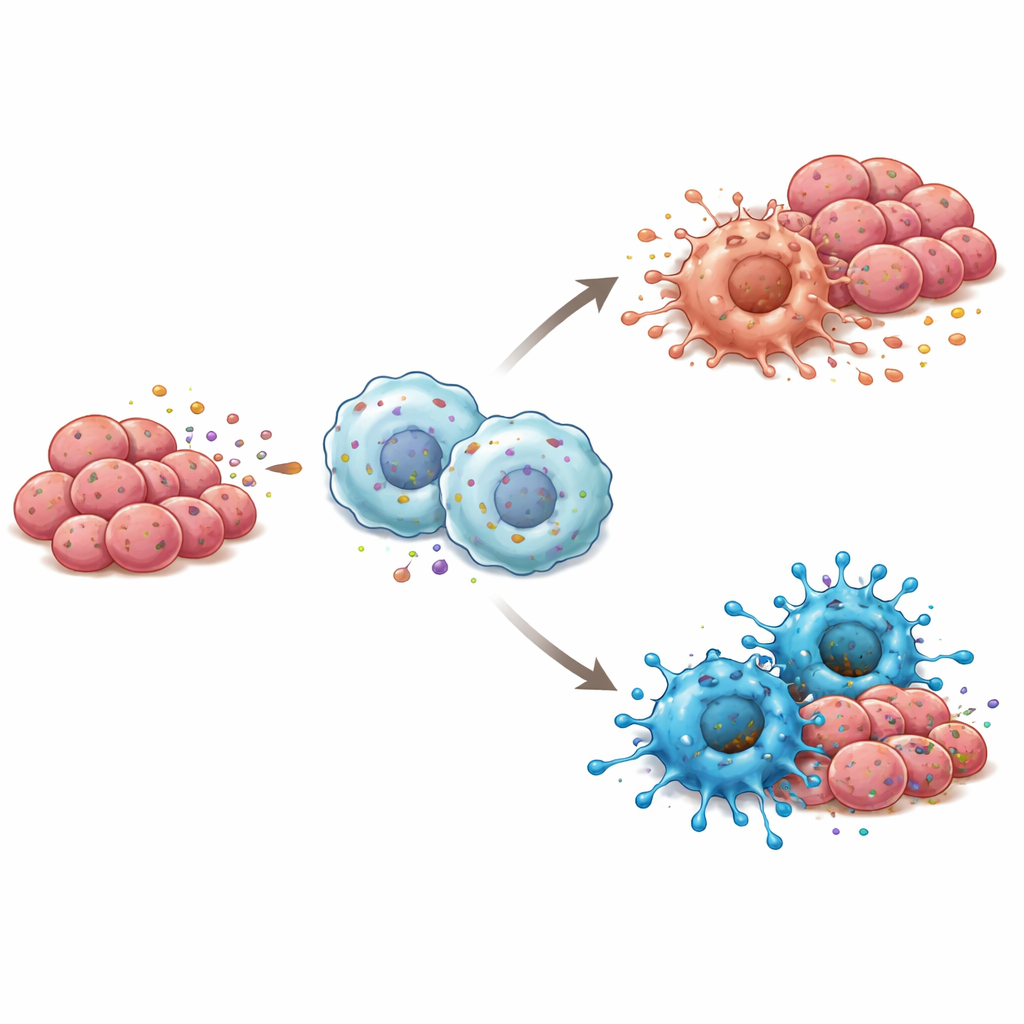
Signalwege hinter der Immunumstellung
Um zu verstehen, wie RBP4 Makrophagen in eine feindlichere Haltung gegenüber Tumoren drängt, untersuchten die Forscher, welche internen Alarmwege in diesen Immunzellen aktiviert wurden. Sie fanden heraus, dass RBP4 einen Sensor namens TLR4 auf der Makrophagenoberfläche stimulierte und damit wiederum NF‑κB aktivierte, einen zentralen Schalter, der Entzündungsreaktionen antreibt. Die Blockade von TLR4 mit einem chemischen Inhibitor unterbrach diese Kaskade und verhinderte, dass Makrophagen den M1‑Zustand annahmen, selbst in Anwesenheit von RBP4. In Mäusen wuchsen Tumoren, die aus RBP4‑reichen Zungenkrebszellen und Makrophagen gebildet wurden, langsamer und enthielten mehr M1‑Zellen sowie stärkere TLR4‑ und NF‑κB‑Aktivität, was die Vorstellung stützt, dass dieser Weg entscheidend für die immunologischen Effekte von RBP4 ist.
Was das für zukünftige Therapien bedeuten könnte
In der Gesamtschau zeichnet die Arbeit RBP4 als doppelt wirkende Bremse gegen Zungenkrebs: innerhalb der Tumorzellen dämpft es einen überaktiven Wachstums‑Kreislauf, und in der Tumornachbarschaft hilft es, Makrophagen in wachsame Verteidiger zu verwandeln. Obwohl viele Fragen offen bleiben—etwa wie RBP4 genau mit seinen Zielstrukturen interagiert und wie man es am besten und sichersten steigern könnte—legt die Studie nahe, dass die Wiederherstellung oder Nachahmung von RBP4‑Funktionen sowohl das Tumorwachstum verlangsamen als auch den körpereigenen Immunangriff auf den Krebs verstärken könnte. Für Patientinnen und Patienten eröffnet das die Aussicht auf zukünftige Therapien, die Tumore nicht nur entfernen, sondern auch deren innere Verschaltung und das lokale „Ökosystem“ so umgestalten, dass Rückfälle unwahrscheinlicher werden.
Zitation: Yan, Y., Miao, N. & Wang, X. RBP4 interferes with tongue squamous cell carcinoma progression by inhibiting the PI3K/AKT signaling pathway and promoting macrophage M1-type polarization. Sci Rep 16, 9375 (2026). https://doi.org/10.1038/s41598-026-39915-4
Schlüsselwörter: Zungenkrebs, RBP4, Tumormikroumgebung, Makrophagen, PI3K AKT Signalweg