Clear Sky Science · de
Ein intelligentes Gesundheitsrahmenwerk zur Diagnose des hepatozellulären Karzinoms basierend auf aggregierten Lernenden aus biomedizinischen Daten unter Nutzung erklärbarer künstlicher Intelligenz
Warum schlauere Leberkrebskontrollen wichtig sind
Leberkrebs, insbesondere eine häufige Form namens hepatozelluläres Karzinom, wächst oft still, bis er schwer behandelbar ist. Ärztinnen und Ärzte sammeln bereits viele Routinewerte von Patientinnen und Patienten, aber all diese Zahlen in frühzeitige Warnsignale zu verwandeln ist schwierig. Diese Studie untersucht, wie fortgeschrittene Computerprogramme Alltagsdaten aus dem Gesundheitswesen durchsuchen können, um zu erkennen, welche Patienten ein hohes Risiko tragen, und gleichzeitig ihre Entscheidungswege so zu erklären, dass Ärztinnen und Ärzte ihnen vertrauen können.
Routinewerte in Frühwarnungen verwandeln
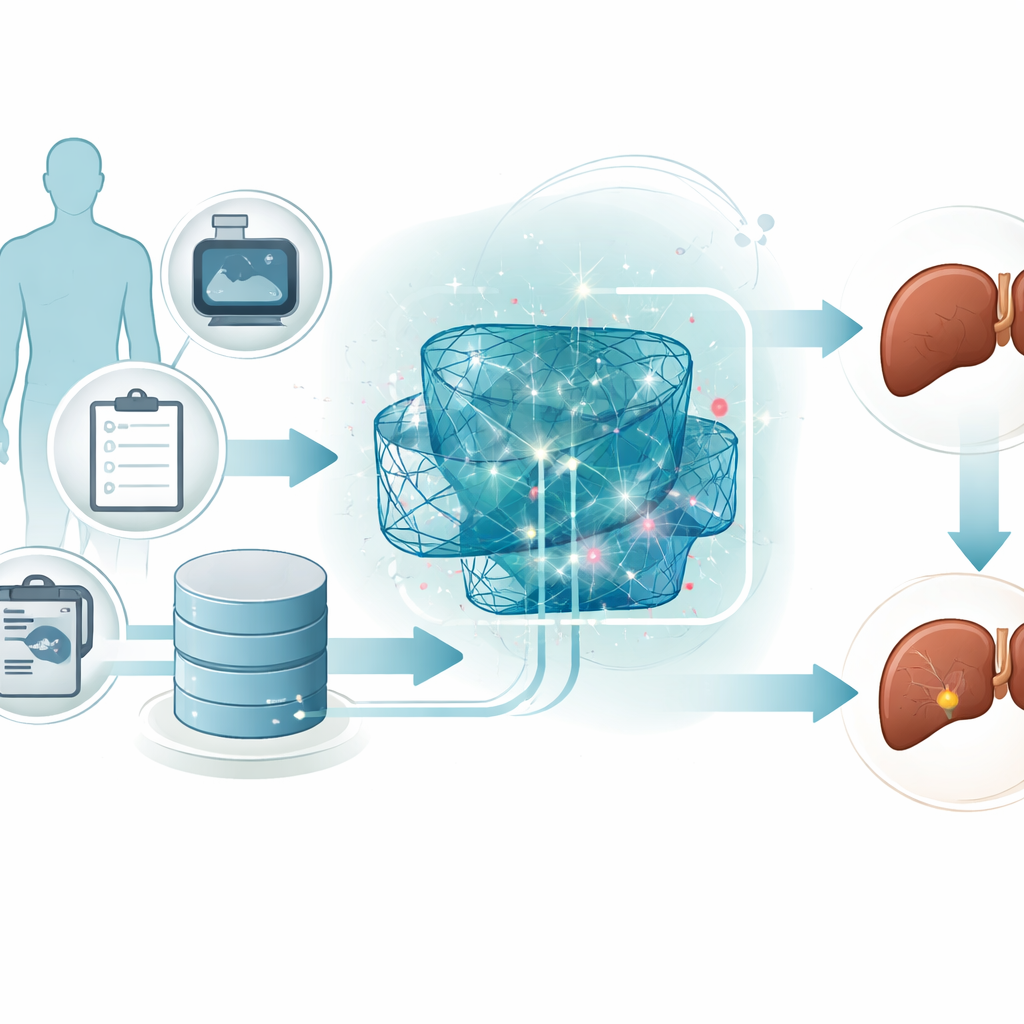
Die Forschenden konzentrieren sich auf Patientinnen und Patienten mit chronischen Lebererkrankungen, die ein höheres Risiko für die Entwicklung eines schweren Leberkrebses haben. Anstatt auf teure Bildgebungen oder komplexe Gentests zu setzen, nutzen sie standardmäßige klinische Messwerte – etwa Blutchemie, Leberenzyme und grundlegende Gesundheitsinformationen. Diese Messwerte werden zunächst sorgfältig reskaliert, sodass alle Merkmale in denselben numerischen Bereich fallen. Dieser einfache, aber wichtige Bereinigungsschritt hilft Computermodellen, Muster zuverlässiger zu lernen, und verhindert, dass ein einzelner ungewöhnlich großer Wert die Vorhersagen dominiert.
Viele digitale „Zweitmeinungen“, die zusammenarbeiten
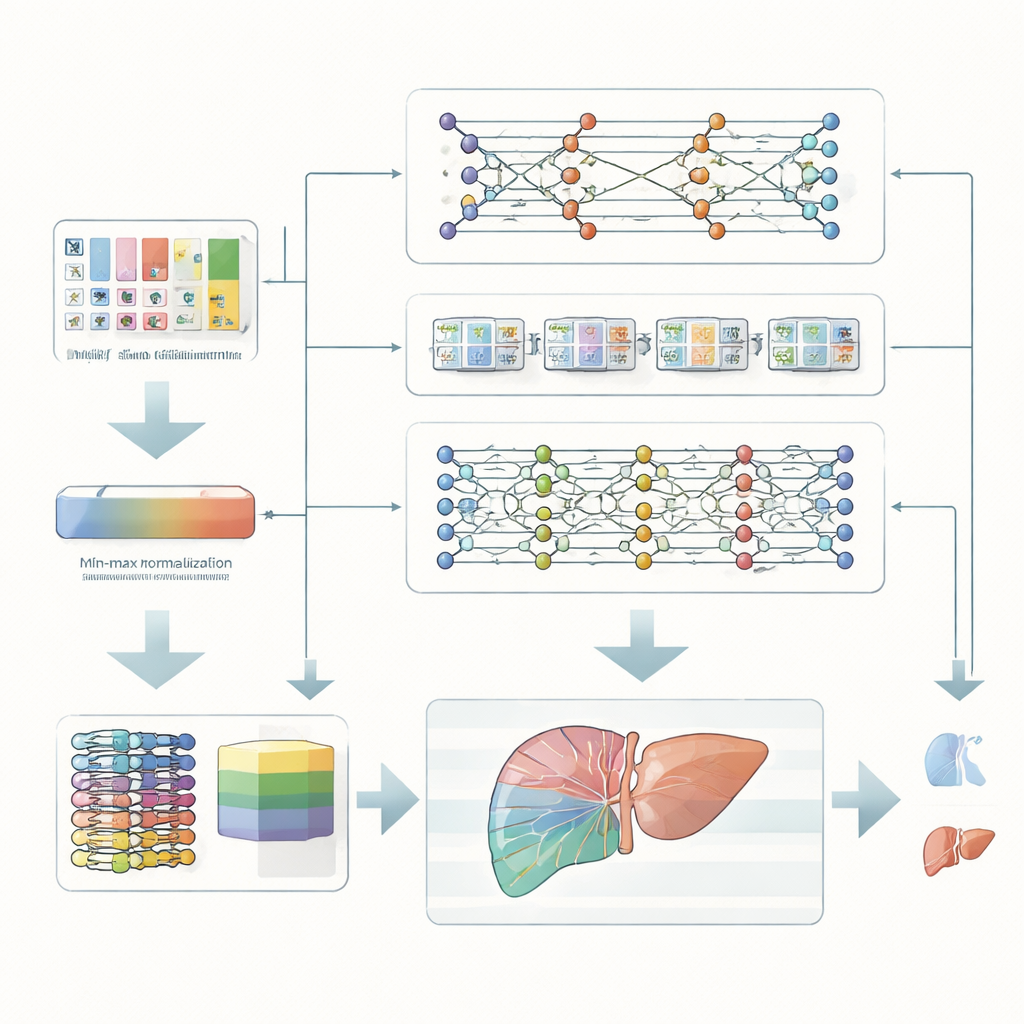
Statt sich auf einen einzelnen Algorithmus zu verlassen, baut das Team ein Ensemble, also ein Team, aus drei verschiedenen tiefen Lernmodellen. Ein Modell komprimiert die Daten, um die informativsten Merkmalskombinationen zu entdecken. Ein zweites Modell ist so ausgelegt, Muster zu erkennen, die sich wie Sequenzen entfalten, und einfängt, wie mehrere Messwerte zusammen auf ein Risiko hindeuten können. Ein drittes Modell stapelt mehrere einfache Schichten, um komplexe, nichtlineare Beziehungen in den Daten zu erfassen. Jedes Modell gibt eine eigene Einschätzung ab, ob ein Patient zur Hochrisiko- oder Niedrigrisikogruppe gehört, und ein höherstufiger Kombinator gewichtet und verschmilzt diese Einschätzungen zu einer endgültigen Entscheidung.
Die Blackbox für Ärztinnen und Ärzte öffnen
So mächtig sie auch sind, werden Deep‑Learning‑Systeme oft dafür kritisiert, wie geheimnisvolle „Blackboxes“ zu agieren. Um dem entgegenzuwirken, fügen die Autorinnen und Autoren eine Schicht erklärbarer künstlicher Intelligenz hinzu, die auf einer Methode namens SHAP basiert. Diese Technik schätzt ab, wie stark jedes Eingangsmerkmal eine einzelne Vorhersage in Richtung eines sichereren oder riskanteren Ergebnisses drückt. Beispielsweise erweisen sich bestimmte Leberenzymwerte, Marker der Leberfunktion und Hinweise auf Außerausbreitung der Erkrankung als besonders einflussreich. Ärztinnen und Ärzte sehen nicht nur, dass das System einen Patienten als Hochrisiko einstuft, sondern auch, welche konkreten Messwerte diese Entscheidung in welche Richtung beeinflusst haben, wodurch eine transparentere Partnerschaft zwischen Klinikpersonal und Maschine entsteht.
Wie gut funktioniert der Ansatz?
Das Team testet sein Rahmenwerk an einem öffentlichen Datensatz mit 165 Patientinnen und Patienten, die mindestens ein Jahr lang verfolgt wurden und jeweils als überlebend oder nicht überlebend gekennzeichnet sind. Trotz der bescheidenen Datensatzgröße lernt das kombinierte Modell, Hochrisiko- von Niedrigrisikopatienten mit auffallender Genauigkeit zu trennen: In den finalen Trainingsphasen klassifiziert es etwa 98 von 100 Fällen korrekt. Im Vergleich mit einer Reihe bestehender Methoden – einschließlich klassischer statistischer Modelle und mehrerer moderner neuronaler Netze – erreicht dieser Ansatz nicht nur ähnliche oder bessere Werte bei Genauigkeit, Präzision und dem Gleichgewicht zwischen Fehlalarmen und verpassten Fällen, sondern das bei relativ niedrigen Rechenzeiten. Eine Ablationsstudie, bei der die drei Teilmodelle einzeln getestet werden, zeigt, dass jedes für sich einen Beitrag liefert, ihre Kombination jedoch am besten abschneidet.
Was das für die Patientenversorgung bedeuten könnte
Für die tägliche medizinische Praxis weist diese Arbeit auf Entscheidungswerkzeuge hin, die sowohl präzise als auch nachvollziehbar sind. Ein System nach diesem Prinzip könnte helfen, Leberpatientinnen und -patienten zu identifizieren, die sich lange vor dem Auftreten von Symptomen heimlich in eine Gefahrenzone bewegen, und zwar mit Daten, die bereits in vielen Kliniken erhoben werden. Gleichzeitig könnten seine Erklärungen – die hervorheben, welche Testergebnisse und klinischen Zeichen für eine bestimmte Person am wichtigsten sind – Ärztinnen und Ärzten dabei helfen, Behandlungspläne zu verfeinern und Risiken mit Patientinnen und Patienten zu besprechen. Auch wenn die Studie noch auf einem relativ kleinen, einheitlichen Datensatz basiert und Bild- sowie genetische Daten unberücksichtigt lässt, bietet sie eine Roadmap für intelligentere, transparentere Krebsrisikomodelle, die mit größeren und vielfältigeren Daten eines Tages zu routinemäßigen Partnern im Kampf gegen Leberkrebs werden könnten.
Zitation: Alqaralleh, B.A.Y., Alksasbeh, M.Z., Kulakli, A. et al. An intelligent healthcare framework for hepatocellular carcinoma diagnosis based on aggregated learners from biomedical data utilising explainable artificial intelligence. Sci Rep 16, 9357 (2026). https://doi.org/10.1038/s41598-026-39871-z
Schlüsselwörter: Leberkrebs, medizinische KI, Früherkennung, erklärbare KI, klinische Entscheidungsunterstützung