Clear Sky Science · de
Rheologische Modulation und Wirkstofffreisetzungseffizienz von mit Kohlenstoffnanoröhren verstärkten Guar-Gummi-Hydrogelen
Warum ein intelligenteres Pflaster wichtig ist
Stellen Sie sich ein Pflaster vor, das nicht nur eine Wunde abdeckt, sondern über Stunden still und zuverlässig Antibiotika in gleichmäßigem Tempo abgibt, ohne gewechselt oder nachgefüllt werden zu müssen. Das ist das Versprechen dieser Forschung. Die Autor*innen arbeiteten mit einem natürlich gewonnenen Gel aus Guar-Gummi – einem häufigen pflanzlichen Verdickungsmittel in Lebensmitteln – und verstärkten es mit winzigen Kohlenstoffnanoröhren. Durch das Feinabstimmen der inneren Struktur des Materials gelang es ihnen, die Freisetzung eines Antibiotikums zu verlangsamen und zu glätten, sodass aus einem einfachen Gel eine intelligentere Wirkstoffabgabplattform wurde.
Vom Küchenverdicker zum medizinischen Gel
Guar-Gummi stammt aus den Samen einer bohnenähnlichen Pflanze und wird weit verbreitet zum Andicken von Soßen und Eiscreme verwendet. In der Medizin erlaubt dieselbe Eigenschaft, dass Guar-Gummi weiche, wasserreiche Gele – sogenannte Hydrogele – bildet, die Wirkstoffe halten und freisetzen können. Diese Gele sind körperverträglich und können große Mengen an Flüssigkeit aufnehmen, weshalb sie sich gut für Wundauflagen und lokal begrenzte Therapien eignen. In ihrer reinen Form sind sie jedoch mechanisch schwach und neigen dazu, die meisten Wirkstoffe zu schnell freizugeben – ein „Burst-Effekt“, der die Behandlungsdauer verkürzt und Medizin verschwenden kann. Die Herausforderung besteht darin, das Gel widerstandsfähiger und kontrollierter zu machen, ohne seine natürlichen Vorteile zu opfern.
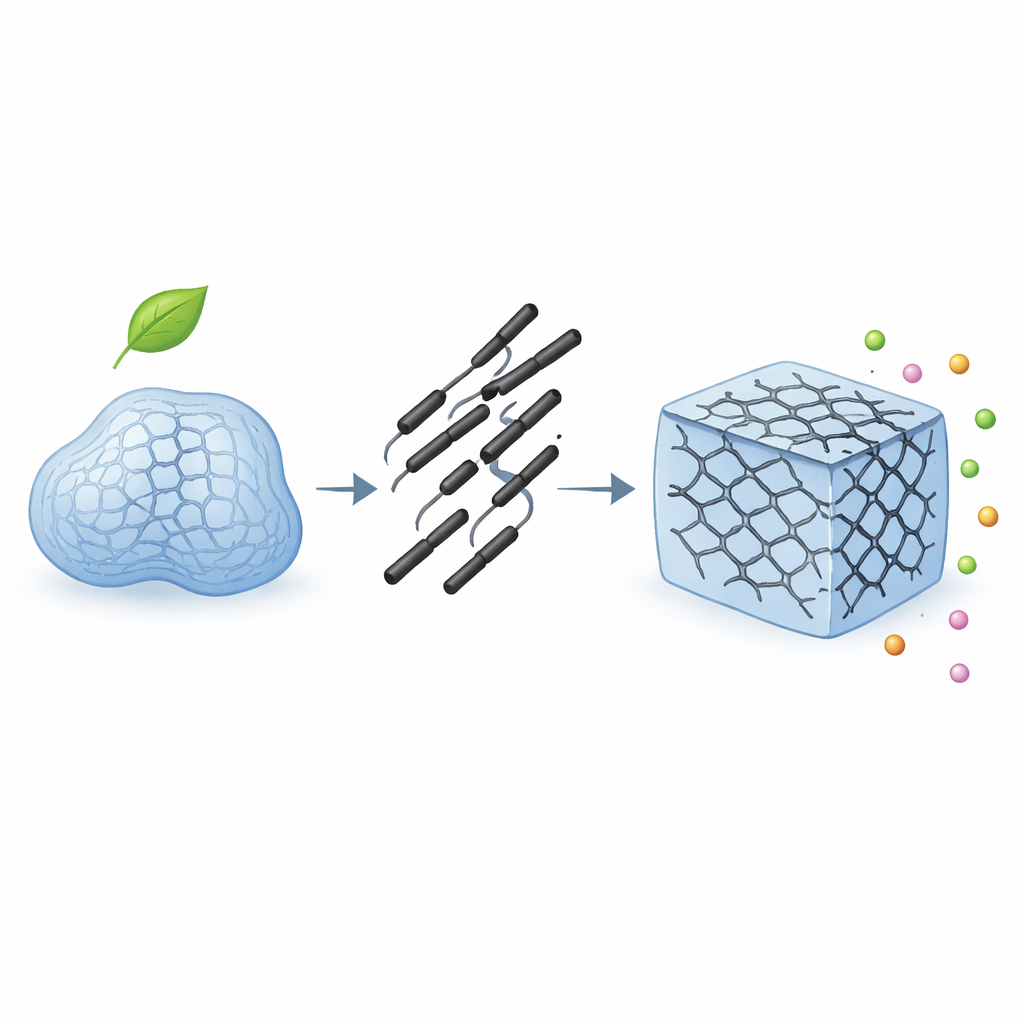
Verstärkung des Gels mit winzigen Röhrchen
Um das Problem zu lösen, mischten die Forschenden sehr geringe Mengen an mehrwandigen Kohlenstoffnanoröhren in das Guar-Gummi-Gel. Diese Nanoröhren sind extrem dünne, hohle Zylinder aus Kohlenstoff, die für ihre Festigkeit und Steifigkeit bekannt sind. Wenn sie in Wasser dispergiert und dann mit heißer Guar-Gummi-Lösung kombiniert werden, verlaufen sie durch das dreidimensionale Netzwerk des Gels. Feine Anziehungskräfte zwischen den Röhrchen und den Polymerketten wirken wie zusätzliche physikalische Verbindungen, die die Struktur zusammenziehen und verstärken. Messungen des Verhaltens des Gels bei leichter Verformung zeigten, dass sein „federähnliches“ Verhalten bereits bei nur 0,2 Prozent Nanoröhrengehalt mehr als verzehnfacht wurde, was auf ein deutlich stabileres und stärker stoffähnliches Netzwerk hindeutet, das dem Auseinanderbrechen besser widersteht.
Wie die Struktur Schwellung und Wasseraufnahme steuert
Die Art und Weise, wie das Gel in Wasser quillt, ist entscheidend, weil das Quellen Kanäle öffnet, über die Wirkstoffe entweichen. Das Team untersuchte, wie viel Wasser die verstärkten Gele unter sauren, neutralen und basischen Bedingungen aufnahmen. Alle Proben quollen zunächst schnell und verlangsamten sich dann, als sie eine stabile Größe erreichten. Gele mit weniger Nanoröhren quollen stärker – unter sauren Bedingungen auf das mehr als Zehnfache ihres Trockengewichts –, während Gele mit mehr Nanoröhren weniger quollen. Dieses Verhalten zeigt, dass das Hinzufügen von Nanoröhren das Netzwerk enger zusammenpackt und weniger freien Raum für Wasser lässt. Dennoch blieben die Gele stark hydratisiert und stabil, was bedeutet, dass sie in verschiedenen körperähnlichen Umgebungen intakt und feucht bleiben können und gleichzeitig eine feinere Kontrolle darüber bieten, wie schnell Substanzen durch sie hindurchwandern.
Die Wirkstofffreisetzung glätten
Um die praktische Leistungsfähigkeit zu testen, luden die Forschenden die Hydrogele mit dem Antibiotikum Levofloxacin und verfolgten, wie es in einer Kochsalzlösung ähnlich der Körperflüssigkeiten über die Zeit freigesetzt wurde. Ein schwächeres, leicht verstärktes Gel setzte etwa 90 Prozent des Wirkstoffs innerhalb von ungefähr 6 bis 8 Stunden frei und zeigte damit ein schnelles Ausstoßverhalten. Im Gegensatz dazu setzte ein Gel mit höherem Nanoröhrengehalt eine ähnliche Gesamtmenge – etwa 96 bis 97 Prozent – frei, zog diesen Prozess jedoch über rund 28 Stunden hinweg und zeigte ein deutlich lineareres, gleichmäßigeres Muster. Das dichtere Netzwerk und das Vorhandensein der Nanoröhren zwingen die Wirkstoffmoleküle, komplexere, hindernisreiche Pfade zu folgen, wodurch ihr Austreten verlangsamt, aber nicht dauerhaft blockiert wird. Diese Kombination aus Festigkeit und kontrollierter Freisetzung macht das Material besonders vielversprechend für langanhaltende Antibiotikatherapien.
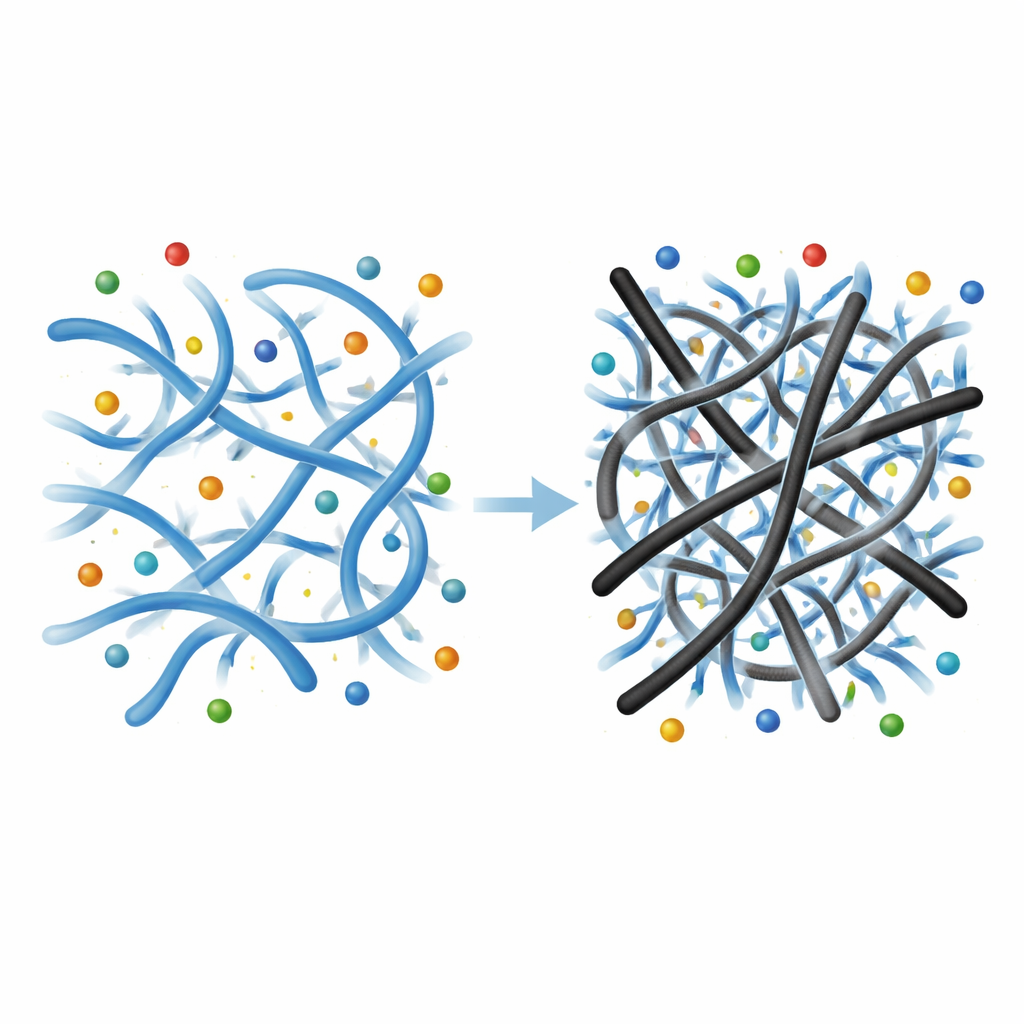
Was das für zukünftige Behandlungen bedeuten könnte
Vereinfacht gesagt zeigt diese Arbeit, wie die Kombination eines vertrauten pflanzenbasierten Verdickungsmittels mit einer winzigen Menge eines fortschrittlichen Kohlenstoffmaterials ein fragiles, schnell freisetzendes Gel in ein robustes Depot für eine langsame und gleichmäßige Wirkstoffabgabe verwandeln kann. Die verstärkten Guar-Gummi-Hydrogele behalten ihre Form, nehmen Wasser kontrolliert auf und geben Medizin über viele Stunden statt auf einen Schlag frei. Während weitere Studien nötig sind, um Langzeitsicherheit und Leistung in lebenden Systemen zu bestätigen, weist der Ansatz in Richtung intelligenter Pflaster, injizierbarer Depots und lokalisierter Behandlungen, die mit minimalem Nanomaterial die richtige Dosis zur richtigen Zeit liefern.
Zitation: Sharma, S., Mulwani, P. Rheological modulation and drug delivery efficiency of carbon nanotube-integrated guar gum hydrogels. Sci Rep 16, 9298 (2026). https://doi.org/10.1038/s41598-026-39858-w
Schlüsselwörter: Hydrogel-Wirkstofffreisetzung, Guar-Gummi, Kohlenstoffnanoröhren, kontrollierte Freisetzung, Antibiotika-Freisetzung