Clear Sky Science · de
Kandidaten-Biomarker zur Identifizierung von Mesotheliom-Patienten mit Risiko für venöse Thromboembolien nach Operation
Warum diese Forschung für Patienten und Familien wichtig ist
Menschen mit pleuralem Mesotheliom, einer Krebserkrankung der Lungenhaut, sehen sich nach einer Operation oft einer verborgenen Gefahr gegenüber: schweren Blutgerinnseln in Beinen oder Lunge. Diese Gefäßverschlüsse, medizinisch als venöse Thromboembolie bezeichnet, können innerhalb weniger Wochen nach einem Eingriff lebensbedrohlich sein. Bisher verfügen Ärztinnen und Ärzte nur über grobe Werkzeuge, um einzuschätzen, wer das höchste Risiko hat. Diese Studie ist ein wichtiger erster Schritt in Richtung eines einfachen Bluttests, der vor der Operation gefährdete Patientinnen und Patienten kennzeichnen könnte, sodass Behandlungsteams sie mit intensiverer Überwachung und gezielten Maßnahmen schützen können.
Eine stille Bedrohung nach lebensrettender Operation
In den Vereinigten Staaten erhalten jährlich einige tausend Menschen die Diagnose pleurales Mesotheliom, und für manche bietet eine große Operation zur Tumorentfernung die beste Chance auf längeres Überleben. Dennoch sterben bis zu etwa einer von zehn Patientinnen bzw. Patienten möglicherweise innerhalb eines Monats nach dem Eingriff, häufig infolge von Blutgerinnseln, die sich in tiefen Venen bilden und in die Lunge wandern können. Standard-Labortests und einfache Indikatoren wie Thrombozytenzahlen oder ein häufig verwendeter Gerinnungstest namens D‑Dimer sind nicht spezifisch genug, um vorherzusagen, welche Mesotheliom-Patienten tatsächlich Thrombosen entwickeln. Daher erhalten viele dieselben vorbeugenden Maßnahmen, obwohl nur ein Teil tatsächlich ein hohes Risiko hat. Ein genauerer Prädiktor könnte helfen, die Versorgung zu individualisieren und sowohl gefährliche Gerinnsel als auch unnötige Behandlungen zu vermeiden.
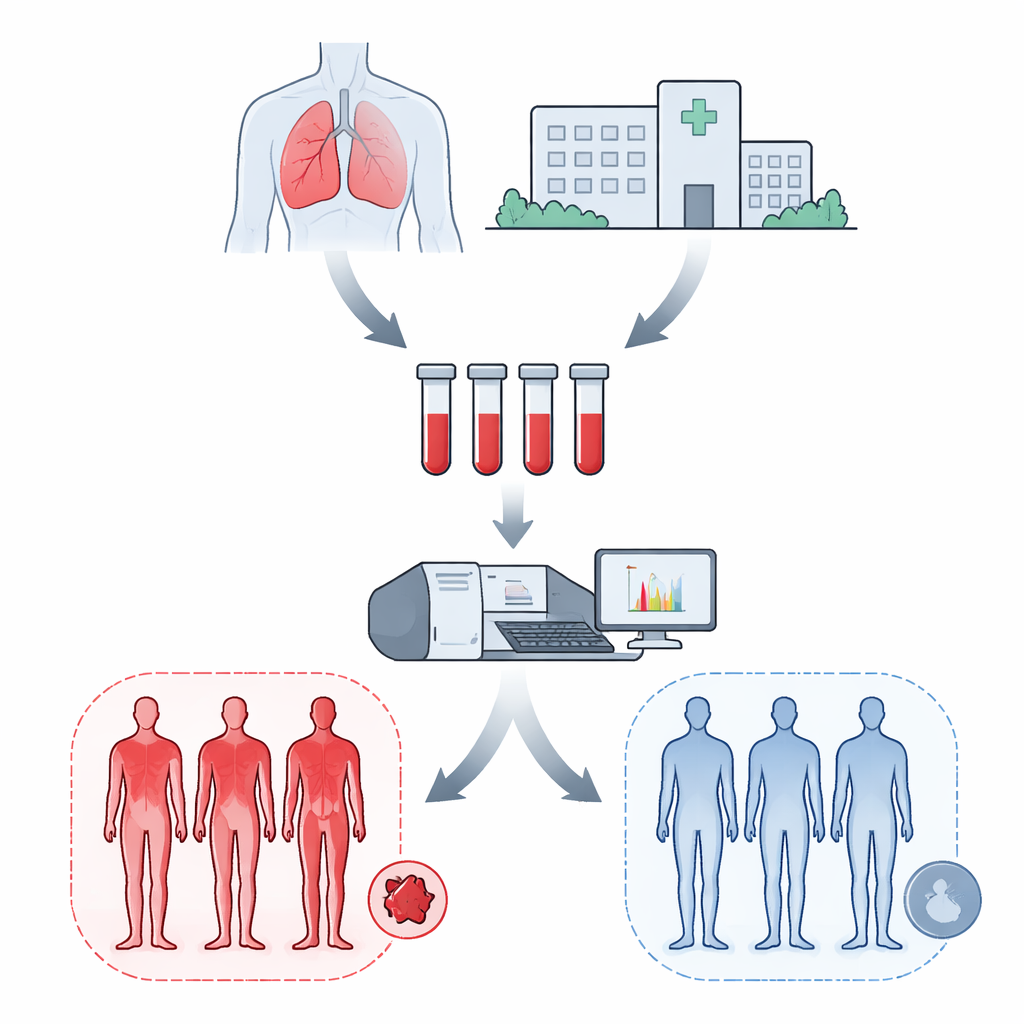
Auf der Suche nach Warnsignalen in Blutproteinen
Die Forschenden konzentrierten sich auf im Blut zirkulierende Proteine, die sich auf subtile, aber aussagekräftige Weise verändern könnten, bevor Gerinnsel auftreten. Untersucht wurden Plasma-Proben von nur 18 Personen: sechs Mesotheliom-Patientinnen bzw. -Patienten, die nach der Operation später Gerinnsel entwickelten, sechs Mesotheliom-Patienten, die dies nicht taten, und sechs Lungenkrebspatienten, bei denen ebenfalls keine Gerinnsel auftraten. Alle Proben wurden vor der Operation gewonnen, also bevor irgendwelche thrombosebezogenen Symptome oder Therapien eintraten. Mithilfe hochentwickelter Massenspektrometrie, einer Technik, die tausende Proteine gleichzeitig trennen und messen kann, erstellte das Team ein detailliertes Abbild der Proteine, die in den Patientengruppen stärker oder schwächer vertreten waren. Eine maßgeschneiderte Analyse-Pipeline namens WASP half dabei, diese komplexen Proteinprofile auch mit einer so kleinen Patientenzahl zu bereinigen, zu normalisieren und zu vergleichen.
Die vielversprechendsten Hinweise eingrenzen
Aus nahezu 600 detektierten Proteinen verglichen die Forschenden drei zentrale Gruppen: Mesotheliom-Patienten mit und ohne spätere Gerinnsel sowie beide diese Gruppen je gegen Lungenkrebspatienten ohne Gerinnsel. Durch sorgfältiges Überschneiden dieser Vergleiche identifizierten sie eine Shortlist von 33 Proteinen, die ausschließlich bei den Patientinnen und Patienten auftraten, die später Blutgerinnsel entwickelten, und in beiden Kontrollgruppen fehlten. Anschließend führten sie eine zweite Analyseschicht durch und prüften für jeden Kandidaten drei Fragen: Interagieren diese Proteine miteinander in bekannten biologischen Netzwerken? Sind sie an Wegen beteiligt, die mit Gerinnung und Entzündung verknüpft sind? Und sind ihre Spiegel vom Fortschreiten des Mesothelioms abhängig oder bleiben sie relativ stabil über die Tumorstadien hinweg?
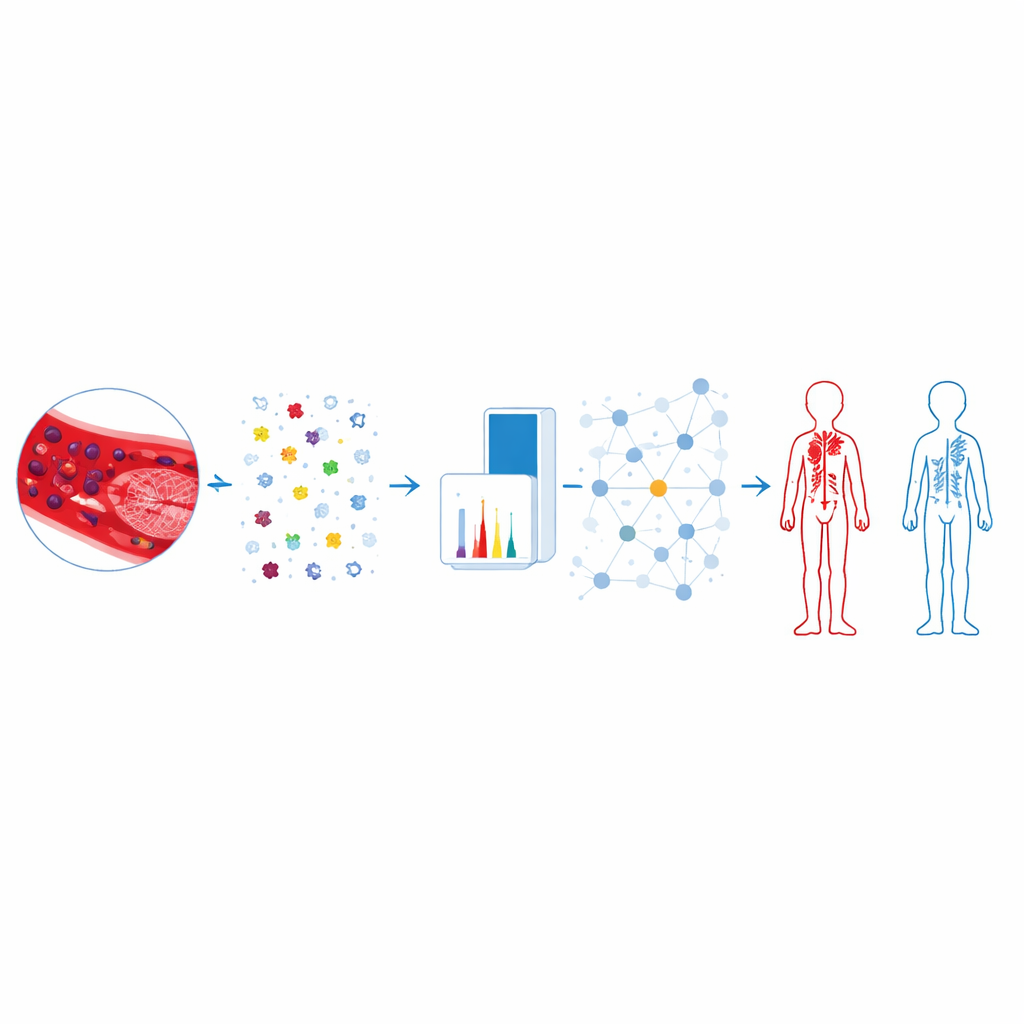
Verknüpfung von Protein-Netzwerken mit Thromboserisiko
Als die 33 Proteine in bekannte Interaktionsnetzwerke eingeordnet wurden, zeigten sich mehrere eng verbundene Cluster. Ein Cluster enthielt insbesondere Proteine, die mit dem Komplement- und dem Gerinnungssystem des Körpers verbunden sind — zwei verflochtene Kaskaden, die sowohl Immunantworten als auch Blutgerinnung steuern. Innerhalb dieser Gruppe hoben die Autorinnen und Autoren Proteine wie CFHR2, CFHR5, KNG1 und F12 hervor, die upstream in diesen Wegen liegen und in früheren Studien mit Thromboserisiko in Verbindung gebracht wurden. Wichtig ist, dass mehrere dieser Kandidaten in großen öffentlichen Krebsdatensätzen wenig mit dem Krankheitsstadium variierten, was darauf hindeutet, dass Änderungen ihrer Blutspiegel eher durch Thromboserisiko als allein durch Tumorlast getrieben sein könnten. Andere Kandidaten standen im Zusammenhang mit Thrombozytenaktivität und Stoffwechsel und deuten auf zusätzliche Mechanismen hin, durch die sich bei diesen Patienten Gerinnsel bilden könnten.
Was das für die künftige Versorgung bedeutet
Diese Arbeit liefert noch keinen sofort einsetzbaren klinischen Test, und die Autorinnen und Autoren betonen mehrere Einschränkungen, darunter die geringe Patientenzahl und das Fehlen eines direkten Vergleichs mit etablierten Werkzeugen wie D‑Dimer in größeren Kohorten. Die Studie zeigt jedoch eine sorgfältige Strategie, um aussagekräftige Signale aus wertvollen, schwer zu beschaffenden Proben zu gewinnen, und liefert eine fokussierte Liste von Proteinkandidaten, die nun in größeren, diverseren Patientengruppen geprüft werden können. Bestätigen künftige Studien, dass einige dieser Proteine verlässlich Mesotheliom-Patienten mit hohem Risiko für gefährliche Blutgerinnsel markieren, könnten Ärztinnen und Ärzte eine einfache Blutentnahme vor der Operation nutzen, um die Prävention zu personalisieren — mit intensiverer Überwachung und Schutzmaßnahmen für Hochrisikopatienten, während andere unnötige Eingriffe und Medikamente erspart blieben.
Zitation: Shami-shah, A., Roth, S., Morton, S.R. et al. Candidate biomarkers to identify mesothelioma patients at risk of developing venous thromboembolism post-surgery. Sci Rep 16, 9313 (2026). https://doi.org/10.1038/s41598-026-39805-9
Schlüsselwörter: pleurales Mesotheliom, venöse Thromboembolie, Blut-Biomarker, Proteomik, postoperative Komplikationen