Clear Sky Science · de
Auswirkungen der Oxidation von G-Quadruplex-RNA auf ihre Konformationsdynamik und Wechselwirkung mit dem ALS-assoziierten TDP-43
Warum das für die Gesundheit der Nerven wichtig ist
Die amyotrophe Lateralsklerose (ALS) ist eine tödliche Erkrankung, bei der die Nervenzellen, die die Bewegung steuern, allmählich absterben, doch die Ursachen dieser selektiven Schädigung bleiben rätselhaft. Diese Studie stellt eine einfache, aber wichtige Frage: Führt die altersbedingte, „rostähnliche“ chemische Schädigung unserer Zellen dazu, dass Abnutzung an der RNA – der Arbeitskopie unserer Gene – lebenswichtige Signale stört, die Motoneurone am Leben erhalten? Indem sie sich auf eine besondere gefaltete RNA-Struktur und ein zentrales, mit ALS verknüpftes Protein namens TDP-43 konzentriert, zeigt die Arbeit, wie winzige chemische Narben zur Krankheitsentstehung beitragen können. 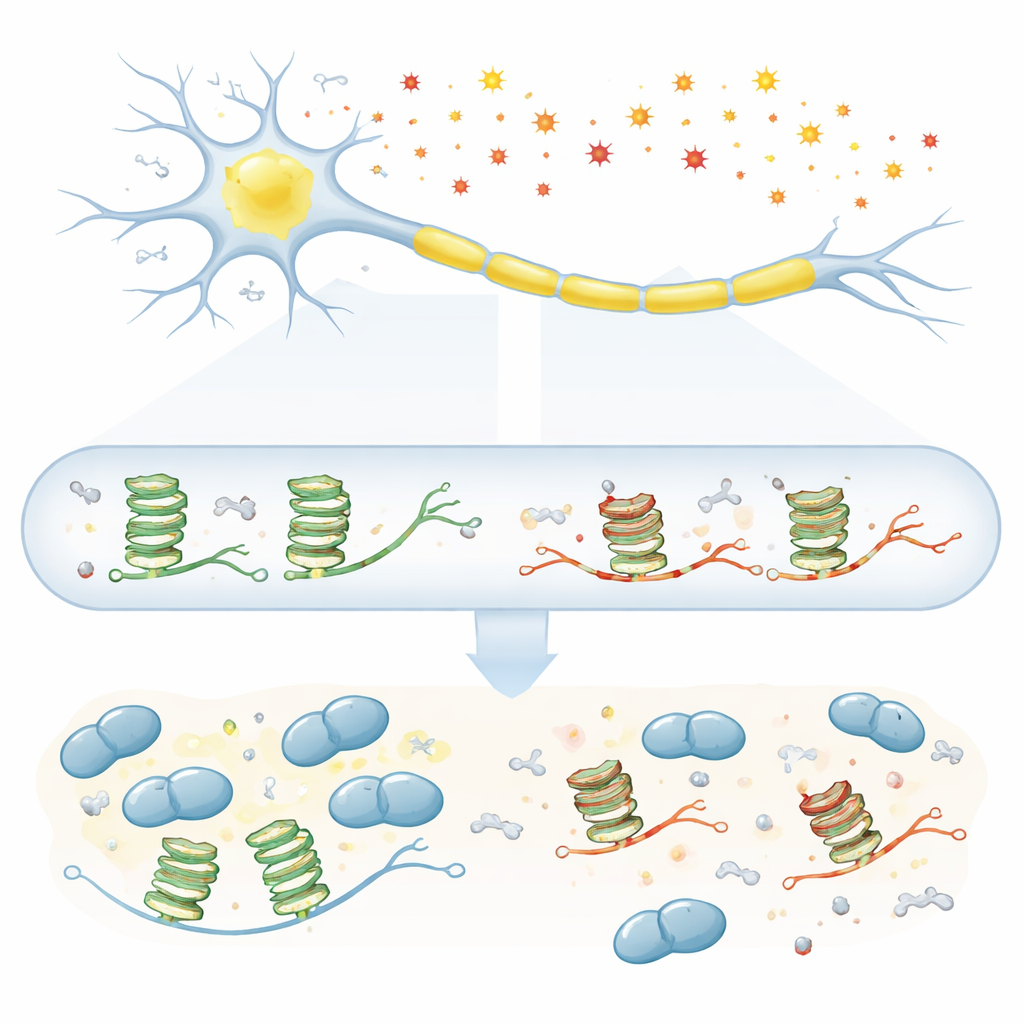
Ein zerbrechlicher RNA-Knoten im Zentrum der Motoneurone
Motoneurone sind auf den Langstreckentransport von RNA-Nachrichten entlang ihrer Axone angewiesen, damit Proteine vor Ort an den Verbindungen zum Muskel produziert werden können. Viele dieser Nachrichten tragen eine spezielle strukturelle „Schlinge“, das G-Quadruplex, aufgebaut aus Guanin-reichen Abschnitten. Proteine wie TDP-43 erkennen diesen Knoten und hängen die RNA an Transportgranula, die entlang des Axons wandern. Problematisch ist, dass Guanin die Base ist, die bei oxidativem Stress am leichtesten oxidiert wird; reaktive Sauerstoffspezies, die mit dem Alter zunehmen, fördern dies. Frühe Hinweise deuteten darauf hin, dass G-Quadruplexe und TDP-43 eine zentrale Rolle bei ALS spielen, doch es war unklar, wie genau die Oxidation dieser RNA-Knoten ihre Zusammenarbeit beeinträchtigen könnte.
Beobachtung, wie oxidativer Stress RNA-Formen verzerrt
Die Forschenden setzten zuerst humane Neuroblastomzellen Wasserstoffperoxid aus, einem häufigen Oxidationsmittel, und untersuchten dann den Zustand der G-Quadruplex-Strukturen. Die Signale einer G-Quadruplex-sensitiven Sonde fielen mit zunehmendem oxidativem Stress, was darauf hindeutet, dass diese kompakten RNA-Knoten ihre normale Form verloren. Um die zugrunde liegende Chemie zu klären, stellte das Team synthetische RNAs her, die G-Quadruplexe bilden, und mischte gezielt unterschiedliche Mengen an 8-Oxoguanin ein, einer bekannten oxidierten Form von Guanin, die in alternden Neuronen und ALS-Gewebe vorkommt. Mithilfe eines Spektrums biophysikalischer Methoden zeigten sie, dass bereits moderate Mengen dieser Modifikation die geordnete Stapelung des G-Quadruplexes lockern, wobei das genaue Ergebnis von der umliegenden RNA-Sequenz abhängt. 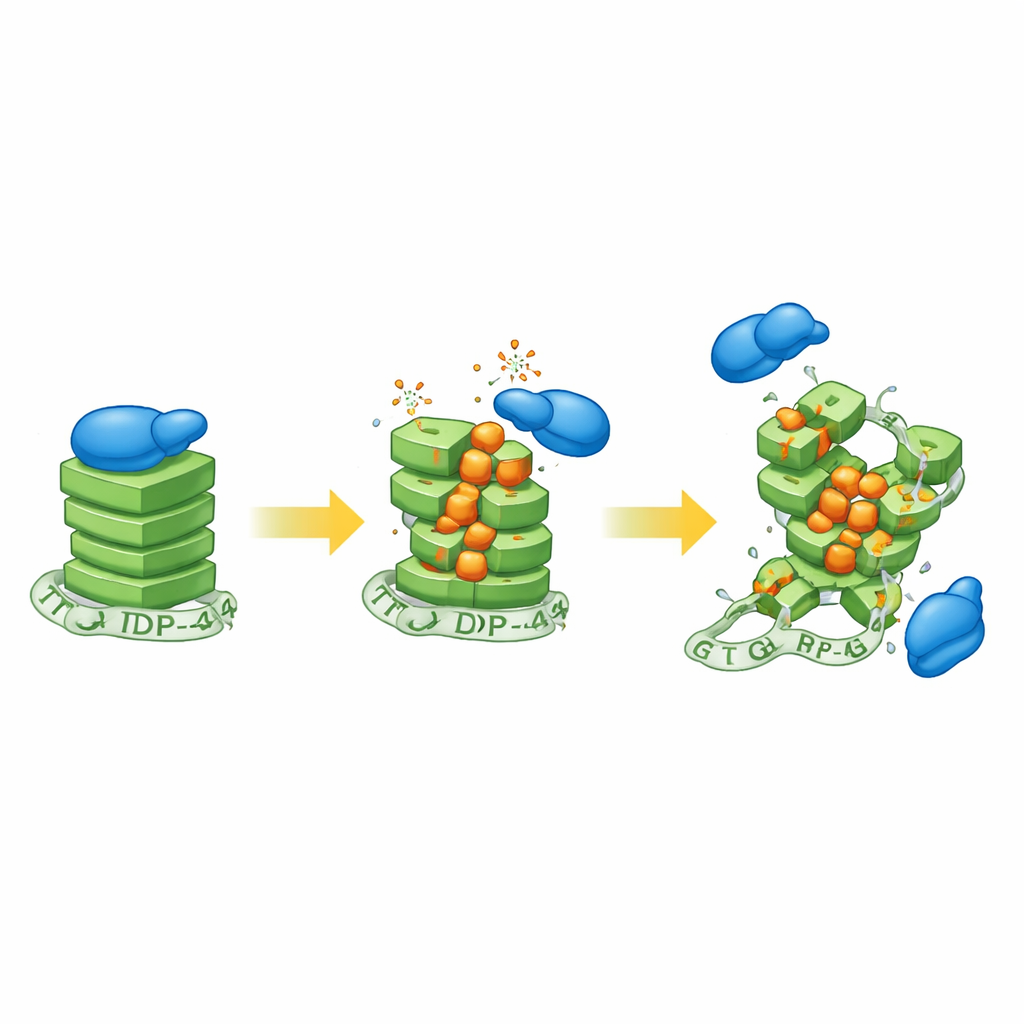
Neue Fehler: Fehlgepaarte Basen und falsch verbundene Stränge
Eine genauere Analyse offenbarte zwei unterschiedliche Arten struktureller Probleme. In einem G-Quadruplex, das aus der PSD-95-Nachricht stammt, neigten oxidierte Guanine dazu, unangemessen mit benachbarten Adeninen zu paaren und so „Mismatch“-Paare zu bilden, die die Faltung subtil verzerren. Diese Fehlpaarungen traten besonders bei mittleren Oxidationsgraden auf, wenn die RNA noch zeitweise ein G-Quadruplex bilden konnte und dadurch die falschen Partner zusammenbrachte. In einem anderen G-Quadruplex aus der CaMKIIα-Nachricht destabilisierte starke Oxidation den üblichen intramolekularen Knoten so stark, dass die verbliebenen intakten Guaninen Partner auf anderen RNA-Strängen suchten und abnormal intermolekulare G-Quadruplexe förderten. Solche falsch verdrahteten Strukturen könnten verschiedene RNAs miteinander verheddern und den normalen RNA-Verkehr innerhalb von Neuronen stören.
Wenn beschädigte RNA ihren Proteinpartner verliert
Die Studie untersuchte dann, wie diese verzerrten Knoten mit TDP-43 interagieren. Mit gelbasierten Bindungsassays zeigten die Forschenden, dass TDP-43 intakte, parallele G-Quadruplexe deutlich bevorzugt und zunehmend nicht mehr bindet, je mehr oxidierte Basen eingeführt werden. Die CaMKIIα-Struktur, die ohnehin dicht gepackt ist, erwies sich als besonders empfindlich: Schon geringe Oxidation hob die TDP-43-Bindung nahezu auf. Ein zweites Protein, FUS – ebenfalls mit ALS assoziiert – zeigte einen ähnlichen, wenn auch etwas weniger ausgeprägten Affinitätsverlust, was darauf hindeutet, dass Oxidation allgemein den Halt von G-Quadruplex-bindenden Proteinen schwächt. Interessanterweise deuteten die Ergebnisse darauf hin, dass TDP-43 bei leicht oxidierter RNA eher eine instabile Zwischenform des G-Quadruplexes bindet als einen vollständig gefalteten Knoten, was auf einen dynamischen Wettstreit zwischen Stabilisierung und Zerfall hindeutet.
Zusätzliche Verwundbarkeit bei ALS-assoziierten Mutanten
Die Arbeit untersuchte ferner zehn TDP-43-Varianten aus ALS-Patienten, die meisten mit Veränderungen in einem flexiblen, glycinreichen C-Terminus, der die RNA-Erkennung feinjustiert. All diese Mutanten banden normale G-Quadruplexe bereits schwächer als das Wildtyp-Protein. Wenn oxidierte G-Quadruplex-RNAs als Konkurrenten eingeführt wurden, waren die Mutanten noch weniger in der Lage als das normale Protein, die beschädigten Strukturen zu erkennen und zu binden. Besonders betroffen waren Varianten in stark unordnungsanfälligen Regionen. Das legt nahe, dass es bei älteren Personen mit solchen Mutationen einen doppelten Schlag gibt: Ihr TDP-43 ist nicht nur intrinsisch weniger effektiv, sondern altersbedingte RNA-Oxidation schwächt zusätzlich dessen Fähigkeit, wichtige Nachrichten entlang der Axone von Motoneuronen zu begleiten.
Was das für das Verständnis von ALS bedeutet
Kurz gesagt zeigt diese Studie, dass altersbedingte chemische Schädigung empfindliche RNA-Knoten umformt, die den Nachrichtentransport in Motoneuronen steuern, und dass diese missgestalteten Knoten nicht mehr gut mit TDP-43 oder verwandten Proteinen zusammenarbeiten. Das Ergebnis ist eine erhöhte Wahrscheinlichkeit fehlgeleiteter oder blockierter RNA-Fracht, gerade in den langen, besonders verletzlichen Axonen, die die Muskeln steuern. Bei Personen mit vererbten TDP-43-Mutationen kann diese oxidationserzeugte Schwächung der RNA–Protein-Interaktionen bereits belastete Neurone noch näher an das Versagen bringen. Indem die Studie diese subtile, aber wirkmächtige Kette von Ereignissen beleuchtet – von oxidativem Stress über veränderte RNA-Architektur bis hin zu gestörtem Transport – stellt sie die Oxidation von G-Quadruplex-RNA als vielversprechende molekulare Verbindung zwischen Altern und ALS dar und als potenzielles Ziel für zukünftige schützende Therapien.
Zitation: Ishiguro, A. Impact of G-quadruplex RNA oxidation on its conformational dynamics and interaction with ALS-associated TDP-43. Sci Rep 16, 8802 (2026). https://doi.org/10.1038/s41598-026-39767-y
Schlüsselwörter: amyotrophe Lateralsklerose, RNA-Oxidation, G-Quadruplex, TDP-43, Degeneration motorischer Neurone