Clear Sky Science · de
Identifizierung von mit Schäden der Blut-Hirn-Schranke im Zusammenhang stehender Biomarker bei zerebralen Infarkten mittels transkriptomischer Analyse
Warum das für Schlaganfall und Hirngesundheit wichtig ist
Wenn jemand einen Schlaganfall durch ein verstopftes Blutgefäß im Gehirn erleidet, können Ärztinnen und Ärzte die Schäden in Bildgebungen sehen, haben aber oft Schwierigkeiten vorherzusagen, wer eine zunehmende Schwellung, Blutungen oder bleibende Behinderungen entwickeln wird. Ein großer Teil dieses Schadens entsteht an der Schutzbarriere des Gehirns, der Blut‑Hirn‑Schranke, die normalerweise verhindert, dass schädliche Substanzen aus dem Blut in das empfindliche Nervengewebe eindringen. Diese Studie stellte eine einfache, aber wichtige Frage: Gibt es charakteristische molekulare Signale, die offenbaren, wenn diese Barriere zusammenbricht, und könnten diese Signale eines Tages bessere Diagnose- und Behandlungsentscheidungen für Schlaganfallpatienten ermöglichen?
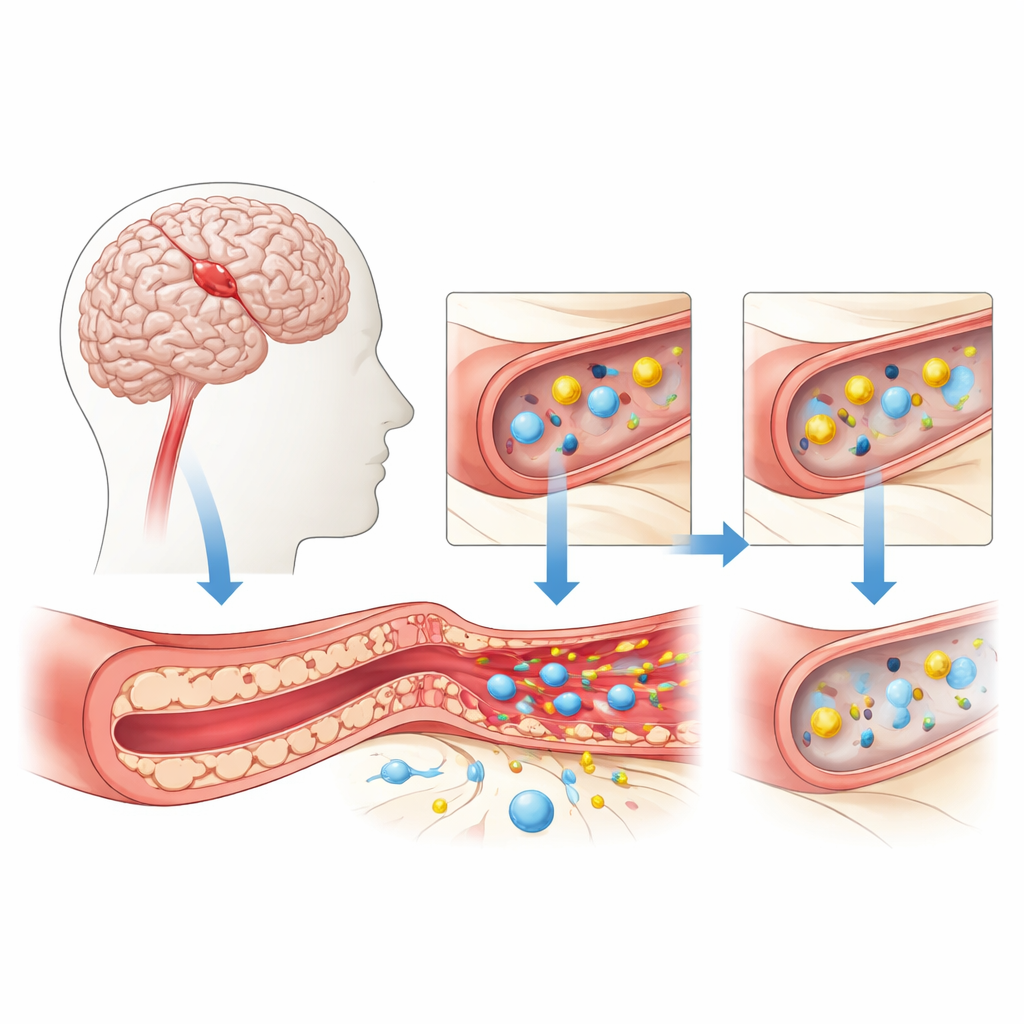
Die Schutzpforte des Gehirns unter Stress
Die Blut‑Hirn‑Schranke wird von dicht gepackten Zellen gebildet, die die kleinen Hirngefäße auskleiden. Diese Zellen kontrollieren genau, was vom Blut ins Gehirn gelangen darf: Sie lassen lebenswichtige Nährstoffe wie Sauerstoff und Glukose hinein und halten Toxine sowie Immunzellen, die Schaden anrichten könnten, fern. Bei einem zerebralen Infarkt, also einem ischämischen Schlaganfall, bricht die Blutversorgung plötzlich zusammen. Ohne ausreichend Sauerstoff und Zucker geraten diese gefäßauskleidenden Zellen unter Stress und verlieren nach und nach ihre dichten Verbindungen. Zwischen ihnen öffnen sich Lücken, Flüssigkeit tritt in das umliegende Gewebe ein, und entzündliche Botenstoffe fluten die Region — all das kann Hirnschwellung und Gewebeschaden verstärken.
Schadensmuster des Schlaganfalls im Labor nachstellen
Um zu untersuchen, was in diesen Barrierezellen vor sich geht, verwendeten die Forschenden eine etablierte menschliche Zelllinie, die die Auskleidung von Hirngefäßen nachahmt. Sie setzten diese Zellen einer sauerstoff‑ und zuckerarmen Umgebung aus — der sogenannten Sauerstoff‑Glukose‑Deprivation — um die Bedingungen eines Schlaganfalls zu simulieren, und stellten anschließend normale Bedingungen wieder her, um Behandlung und Erholung nachzubilden. Sie maßen das Überleben der Zellen, das Ausmaß einer Freisetzung eines Zellschadensenzyms und die Menge freigesetzter Entzündungsmediatoren. Wie erwartet verringerte die belastende Behandlung die Zellgesundheit, steigerte entzündliche Signale wie IL‑1β, IL‑6 und TNF‑α und erhöhte das Austreten eines Schadensmarkers namens LDH. Nach Wiederherstellung von Sauerstoff und Nährstoffen besserten sich viele dieser schädlichen Veränderungen, und die Zellen erlangten in einem Wachstumsversuch teilweise ihre Fähigkeit zur Bildung gefäßähnlicher Röhrchen zurück.
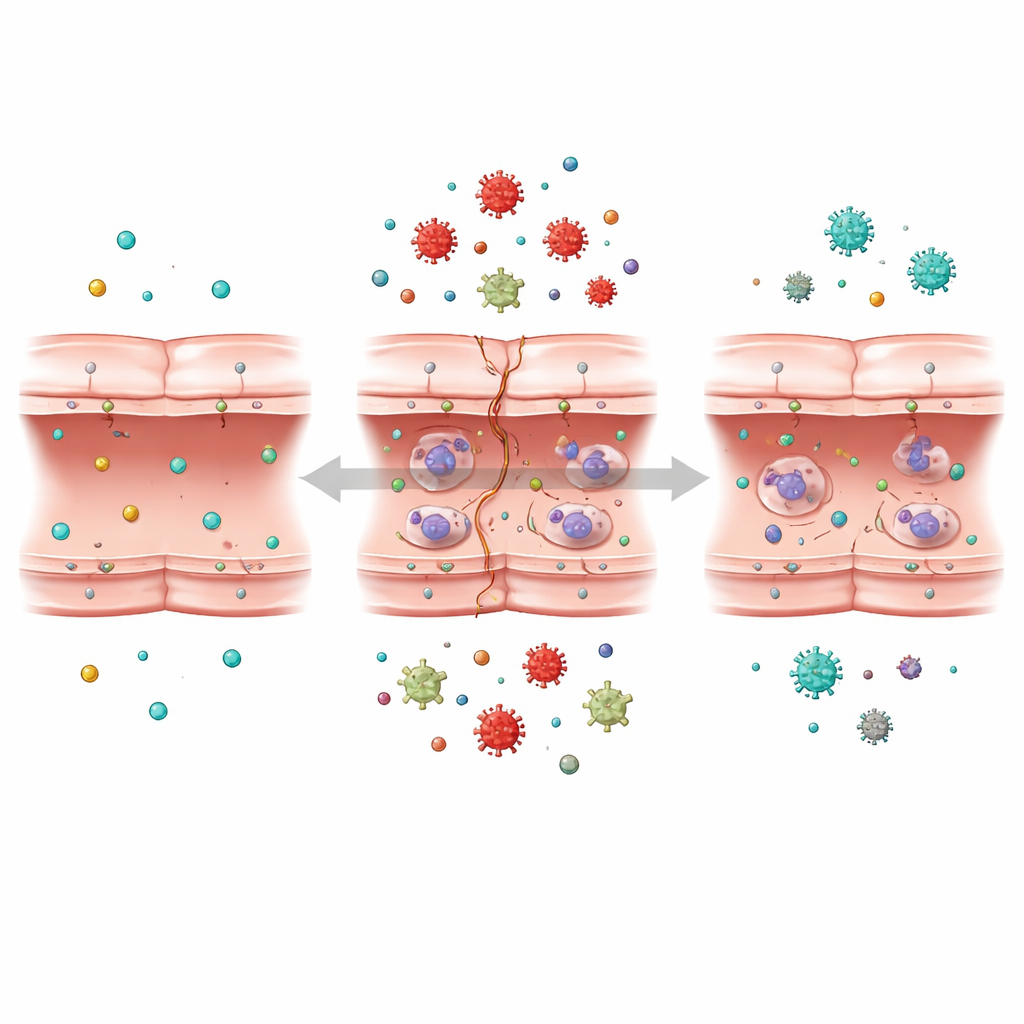
Dem molekularen Dialog der Zelle zuhören
Das Team wandte anschließend eine leistungsfähige Methode namens Transkriptomik an, die die Aktivitätsniveaus von Tausenden Genen gleichzeitig ausliest. Durch den Vergleich normaler Zellen, sauerstoff‑glukose‑deprivierter Zellen und sich erholender Zellen identifizierten sie mehr als tausend Gene, deren Aktivität als Reaktion auf den stressähnlichen Zustand verändert war. Mithilfe fortschrittlicher Datenwerkzeuge und maschinellen Lernens gruppierten sie Gene mit ähnlichem Verhalten und suchten nach denen, die am stärksten mit Barriereverletzung verknüpft sind. Sie fanden heraus, dass viele der am stärksten betroffenen Gene mit drei Schlüsselstrukturen innerhalb der Zelle zusammenhängen: dem Ribosom, das Proteine herstellt; dem endoplasmatischen Retikulum, das beim Falten und Verarbeiten der Proteine hilft; und den Mitochondrien, den kleinen Kraftwerken, die Energie bereitstellen.
Ribosomen treten als aussagekräftige Signale hervor
Aus diesem großen Gensatz verwendeten die Forschenden einen Random‑Forest‑Algorithmus — eine Form des baumbasierten maschinellen Lernens — um eine kurze Liste besonders informativer Gene einzuschränken. Sie kartierten dann, wie die entsprechenden Proteine miteinander interagieren. Diese Analyse hob sechs Kern‑Gene hervor, die größtenteils mit dem Ribosom, der Proteinfabrik der Zelle, verbunden sind. Im schlaganfallähnlichen Zustand zeigten diese ribosomalen Gene eine verstärkte Aktivierung, während ihre Aktivität bei Wiederherstellung von Sauerstoff und Glukose wieder in Richtung Normalwerte sank. Dieses Muster deutet darauf hin, dass Veränderungen in der Proteinproduktionsmaschinerie der Zelle ein empfindliches frühes Signal für Verletzung und Erholung der Blut‑Hirn‑Schranke sein könnten.
Was das für künftige Behandlungsmöglichkeiten bedeuten könnte
Für Nichtfachleute lautet die Kernaussage: Diese Studie weist auf eine neue Klasse molekularer "Warnleuchten" hin, die angehen, wenn die schützende Barriere des Gehirns während eines Schlaganfalls beschädigt wird. Anstatt sich nur auf bekannte Täter wie Enzyme zu konzentrieren, die die Gefäßwand angreifen, zeigt die Arbeit, dass die Proteinfabriken der Zelle selbst stark auf Verletzung reagieren und sich bei Besserung der Bedingungen wieder beruhigen. Wenn zukünftige Forschung bestätigt, dass diese ribosombezogenen Marker in Patientenproben wie Blut nachweisbar sind, könnten Ärztinnen und Ärzte sie eines Tages nutzen, um das Ausmaß der Barriereschädigung zu beurteilen, den Zeitpunkt entzündungs- und schwellungsreduzierender Behandlungen besser zu bestimmen und neue Medikamente zu testen, die darauf abzielen, diesen wichtigen Wächter der Hirngesundheit zu erhalten.
Zitation: Liu, X., He, Y., Zhang, N. et al. Identification of blood-brain barrier injury-related biomarkers in cerebral infarction using transcriptomic analysis. Sci Rep 16, 8119 (2026). https://doi.org/10.1038/s41598-026-39763-2
Schlüsselwörter: ischämischer Schlaganfall, Blut-Hirn-Schranke, Biomarker, ribosomale Gene, Endothelzellen