Clear Sky Science · de
Bakterielle Besiedlung von Tumoren treibt Immunaktivierung und die Wirksamkeit von Checkpoint-Blockaden
Warum winzige Bewohner in Tumoren wichtig sind
Die Krebsbehandlung wurde durch Immuntherapien revolutioniert, die die körpereigenen Immunzellen gegen Tumore entfesseln. Dennoch profitieren viele Patientinnen und Patienten kaum, und vorherzusagen, wer ansprechen wird, ist schwierig. Diese Studie untersucht einen unerwarteten Akteur, der die Waage zum Kippen bringen kann: Bakterien, die direkt in Tumoren leben. Anhand von Maus-Krebsmodellen zeigen die Forschenden, dass diese mikroskopischen Bewohner das Verhalten des Immunsystems in und um einen Tumor verändern können und so mitbestimmen, ob eine häufig eingesetzte Immuntherapie namens Anti–PD-1 gut wirkt oder versagt.
Verborgene Bakterien innerhalb von Tumoren
Jahrelang richtete sich die Aufmerksamkeit vor allem auf die Billionen von Mikroben im Darm und deren Einfluss auf die allgemeine Immunität. Kürzlich entdeckten Wissenschaftler jedoch, dass auch viele menschliche Tumore kleine, aber aktive bakterielle Gemeinschaften beherbergen. Das Team hinter dieser Studie stellte zwei grundlegende Fragen: Enthalten gebräuchliche Maus-Tumormodelle ebenfalls Bakterien, und wenn ja, beeinflussen diese Bakterien tatsächlich, wie Tumore wachsen und auf Therapien reagieren? Sie verglichen zwei Modelle: MCA-205, eine Form von Sarkom, und MOC1, ein Modell für Kopf‑ und Halskrebs. Mit DNA-basierten Tests, Sequenzierung und Kulturmethoden fanden sie, dass MCA-205-Tumore durchgehend lebensfähige Bakterien trugen, während MOC1-Tumore dies nicht taten — selbst wenn sie in die bakterienreiche Mundhöhle verpflanzt wurden. Bei MCA-205 stiegen die Bakterienzahlen tendenziell mit wachsender Tumorgröße, was darauf hindeutet, dass der wachsende Tumor einen günstigen Lebensraum für Mikroben bietet.
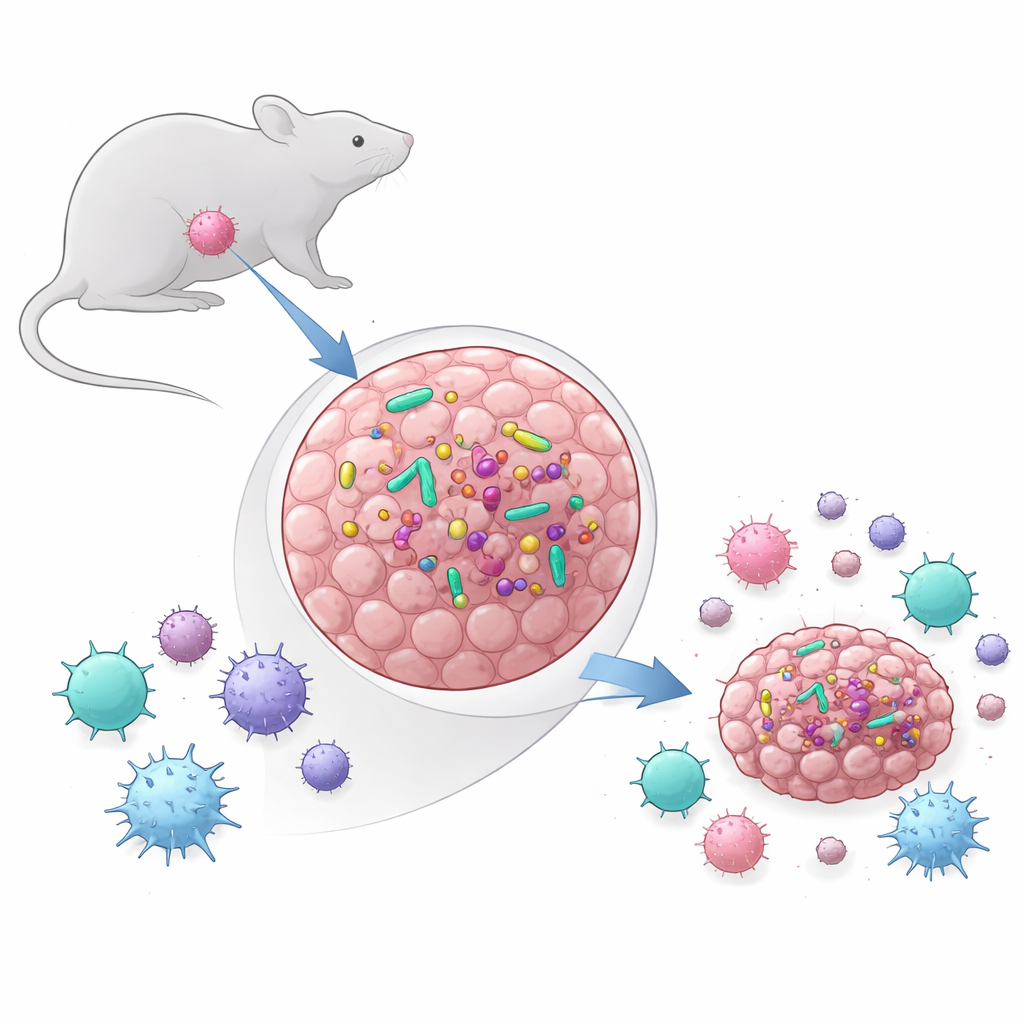
Nachverfolgen, woher die Keime stammen
Die Entdeckung von Bakterien in Tumoren warf eine weitere Frage auf: Stammen diese Eindringlinge von der Haut, dem Mund oder dem Darm? Durch den Vergleich der bakteriellen DNA in Tumoren mit Proben aus Stuhl, Hautabstrichen und Mundabstrichen fanden die Forschenden heraus, dass die intratumorale Gemeinschaft einfacher und weniger divers war als die reichen Ökosysteme im Darm und Mund. Die meisten bakteriellen Typen in den Tumoren überschneiden sich mit denen des Magen‑Darm‑Trakts, während vergleichsweise wenige mit der Haut übereinstimmen. Das spricht dafür, dass Bakterien aus Darm oder Mund in den Blutkreislauf gelangen und dann den Tumor besiedeln, wobei nur bestimmte Arten dauerhaft bestehen. Die Zusammensetzung der bakteriellen Gruppen entsprach der, die in mehreren menschlichen Krebsarten berichtet wurde, und stärkt die Idee, dass diese Maus-Tumore reale Tumor‑Mikroben‑Interaktionen abbilden können.
Wie Tumorbakterien den Erfolg der Immuntherapie formen
Die zentrale Erkenntnis der Studie ist, dass in Tumoren lebende Bakterien den Erfolg der Anti–PD-1-Therapie — eines Checkpoint‑Blockers zur Wiederbelebung erschöpfter Killer‑T‑Zellen — entscheidend beeinflussen können. Als das Team Antibiotika einsetzte, die in den Tumor eindringen und lokale Bakterien auslöschen, während die Darmbesiedlung weitgehend erhalten blieb, reagierten MCA-205-Tumore deutlich schlechter auf Anti–PD-1. Die Ansprechraten sanken noch weiter, wenn die Darmmikrobiota breit gestört wurde. Im Gegensatz dazu hatten Antibiotika in den von Anfang an bakterienfreien MOC1-Tumoren kaum Einfluss auf die bakterielle Belastung oder den Therapieerfolg. Bei MCA-205 zeigten die Tumore, die auf Anti–PD-1 schrumpften, tendenziell eine höhere bakterielle Belastung als therapieresistente Tumore, was eine höhere intratumorale Bakterienlast mit besserer Wachstums‑kontrolle verknüpft.
Im Inneren der immunologischen Frontlinie
Um zu verstehen, wie Bakterien das immunologische Gleichgewicht verschieben, untersuchten die Forschenden Immunzellen innerhalb und um die Tumore. Nach Entfernung intratumoraler Bakterien mit tumordurchdringenden Antibiotika infiltrierten weniger CD8‑Killerzellen den Tumor, und das Verhältnis dieser Zellen zu regulatorischen T‑Zellen verschob sich zugunsten der Unterdrückung. Dendritische Zellen, die Späher, die Tumormaterial aufnehmen und T‑Zellen aktivieren, waren ebenfalls seltener und zeigten geringere Aktivierungszeichen bei Abwesenheit der Bakterien. Interessanterweise führte allein das Hinzufügen eines harmlosen E. coli‑Stamms in den Tumor oder das Ausschalten eines wichtigen Mikroben‑Erkennungswegs (MyD88) in Schlüssel‑Immunzellen nicht zu einer verbesserten Therapie. Das legt nahe, dass nicht jede bakterielle Präsenz oder einfache Alarmierung ausreicht; spezifische Gemeinschaften und nuanciertere Kommunikation mit dem Immunsystem sind vermutlich erforderlich.
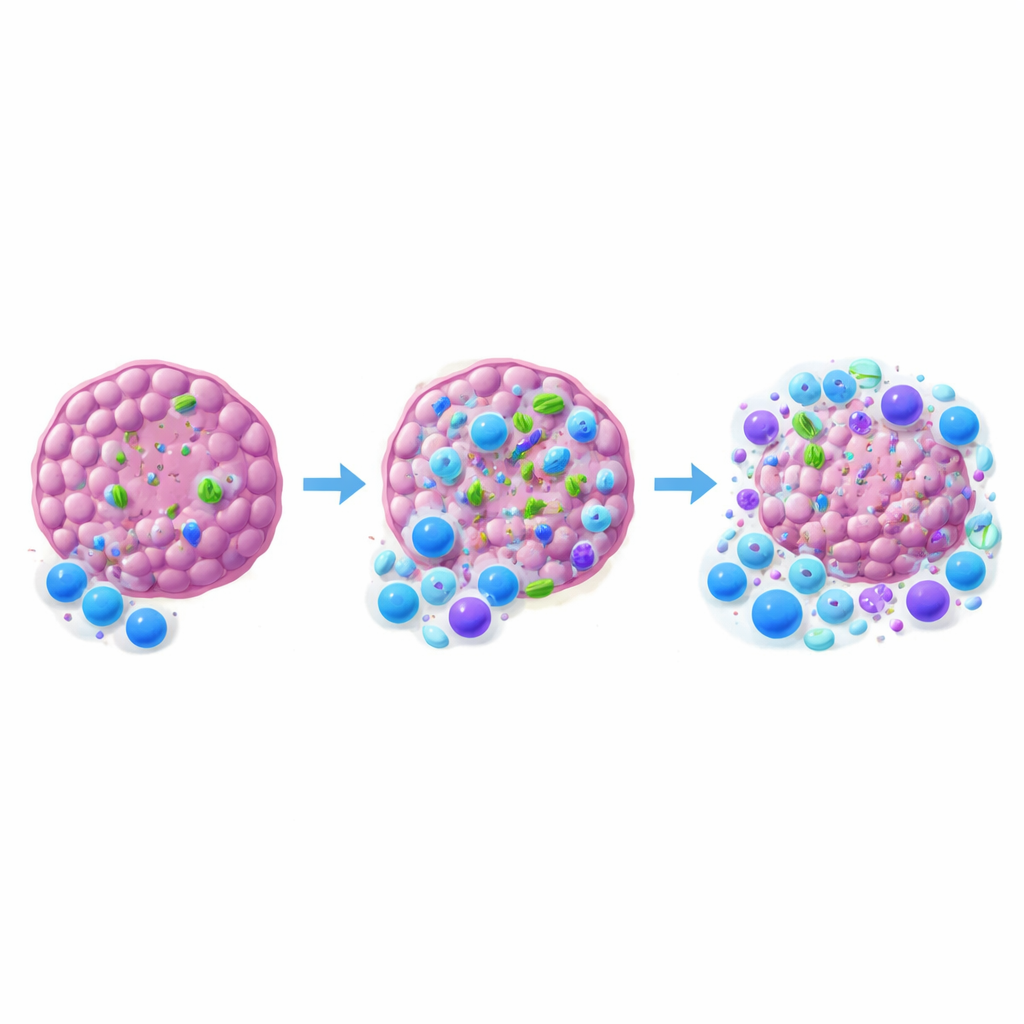
Was das für die künftige Krebsversorgung bedeutet
Für Nicht‑Spezialisten ist die Schlussfolgerung, dass Bakterien in Tumoren keine bloßen Zuschauer sind. In zumindest einigen Krebsarten tragen sie dazu bei, die richtigen Immunzellen in den Tumor zu rekrutieren und die Wirkung von Anti–PD-1‑Medikamenten zu unterstützen. Andere Tumore können nahezu bakterienfrei bleiben und ganz anders reagieren. Wenn Wissenschaftler neue Behandlungen an Mäusen entwerfen und testen, kann die Kenntnis, ob ein bestimmtes Tumormodell Bakterien trägt — und wenn ja, welche — entscheidend dafür sein, Ergebnisse zu interpretieren und Strategien auszuwählen, die sich auf Patientinnen und Patienten übertragen lassen. Langfristig könnte das gezielte Abstimmen der winzigen Gemeinschaften innerhalb von Tumoren neben Medikamenten und Immunzellen als neues Werkzeug zur Verbesserung der Krebsimmuntherapie hinzukommen.
Zitation: Rolig, A.S., Ziglari, T., McGee, G.H. et al. Bacterial colonization of tumors drives immune activation and checkpoint blockade efficacy. Sci Rep 16, 8464 (2026). https://doi.org/10.1038/s41598-026-39758-z
Schlüsselwörter: intratumorale Mikrobiota, Krebsimmuntherapie, Anti-PD-1, Tumormikroumgebung, Bakterien und Tumoren