Clear Sky Science · de
Mit Autismus assoziierte Sema5A p.Arg676Cys aktiviert Arf6/FE65-Signalgebung und führt zu abnormer Zellmorphogenese
Wie eine winzige Änderung die Verschaltung des Gehirns stören kann
Autismus-Spektrum-Störungen beeinflussen, wie Menschen kommunizieren, interagieren und auf ihre Umwelt reagieren. Die biologischen Schritte, die von einer DNA-Veränderung zu veränderter Gehirnfunktion führen, bleiben jedoch oft rätselhaft. Diese Studie untersucht eine solche genetische Veränderung in einem neuronalen "Leitungs"-Protein namens Sema5A und zeigt ungewöhnlich detailliert, wie ein einziger ausgetauschter Baustein in diesem Protein junge Nervenzellen dazu bringen kann, übermäßig lange, verknotete Verzweigungen auszubilden. Das Verständnis dieses mikroskopischen Verdrahtungsfehlers könnte langfristig helfen, Behandlungen zu entwerfen, die die Form von Gehirnzellen wieder in Richtung eines gesünderen Zustands lenken.
Nervenzellen, die zu weit wachsen
Während der Gehirnentwicklung senden junge Nervenzellen lange, dünne Fortsätze aus, die nach den richtigen Partnern suchen und die Schaltkreise bilden, die Denken und Verhalten zugrunde liegen. Dieses Wachstum muss streng kontrolliert werden: Zu wenig Verzweigung führt zu fehlenden Verbindungen; zu viel kann Schaltkreise laut oder fehlverdrahten. Frühere Arbeiten zeigten, dass eine mit Autismus verknüpfte Variante von Sema5A, bei der an Position 676 eine Arginin- gegen eine Cystein-Rest ausgetauscht ist, Nervenzellen im Kulturversuch ungewöhnlich lange Fortsätze wachsen lässt. Die neue Studie wollte herausfinden, welche internen Schalter und Hilfsproteine diese mutierte Sema5A verwendet, um dieses ungebremste Wachstum anzutreiben.
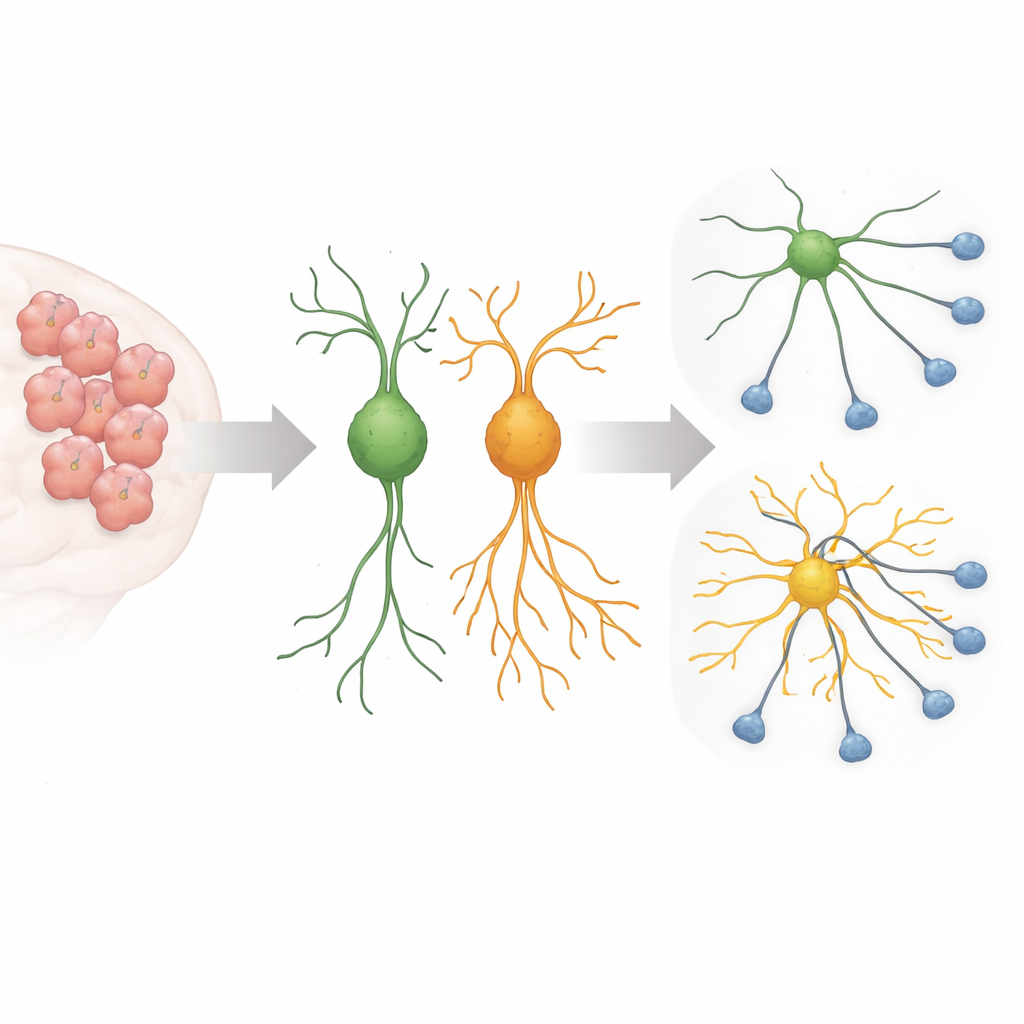
Ein irreführendes Signal im Inneren der Zelle
Die Forschenden konzentrierten sich auf einen kleinen molekularen Schalter namens Arf6 und ein Gerüstprotein namens FE65, die beide dafür bekannt sind, Zellmembranen und das innere Gerüst, das Zellfortsätze stützt, zu formen. Mithilfe eines CRISPR–Cas13-Systems, um diese Proteine selektiv in mausähnlichen Nervenzellen und in primären Maus-Hirnzellen zu reduzieren, fanden sie heraus, dass das Herunterregeln von Arf6 oder FE65 das übermäßige Auswachsen, das durch die mutierte Sema5A verursacht wurde, stark verringerte. Die langen, spinnennetzartigen Fortsätze schrumpften auf eher typische Längen, und Marker neuronaler Reifung nahmen ab, was nahelegt, dass die Wirkung der Mutation stark von diesem speziellen Signalweg abhängt.
Anschluss an die Form‑Maschine der Zelle
Im Inneren von Nervenzellen steuert eine Molekülfamilie als Form-"Maschine" das Aktin, das wichtigste Strukturfilament in Zellfortsätzen. Ein zentrales Mitglied dieser Familie, Rac1, wird normalerweise aktiviert, um beim Auswachsen von Neuriten zu helfen; zu viel Aktivität kann jedoch unkontrolliertes Wachstum antreiben. Das Team zeigte, dass in Zellen mit normaler Sema5A Arf6 für die übliche Rac1-Aktivierung während gesunden Auswachsens nötig ist, während FE65 nicht essenziell ist. Mit der mutierten Sema5A jedoch wurden sowohl Arf6 als auch FE65 kritisch: Die Verringerung eines von beiden, oder das Überfluten der Zelle nur mit dem FE65-Bereich, der an seinen Partner ELMO2 bindet, senkte die ungewöhnlich hohe Rac1-Aktivität wieder in Richtung Normalwert. Dies deutet darauf hin, dass die schädliche Sema5A-Version gezielt ein Arf6–FE65–ELMO2–DOCK5-Komplex nutzt, um Rac1 überzubelasten und Neuriten zu überstrecken.
Ein dichtes Zentrum von Signalpartnern
Um zu sehen, wie diese Teile zusammenwirken, betrachteten die Wissenschaftlerinnen und Wissenschaftler auch ELMO2-basierte "Signalosome" – Proteinkluster, die sich zur Weiterleitung von Wachstumssignalen zusammenlagern. Wenn Arf6 oder FE65 reduziert wurden, bildeten Zellen mit mutierter Sema5A weniger dieser ELMO2-Komplexe in ihren Zellkörpern und Wachstumsenden, was mit der Idee übereinstimmt, dass Arf6 und FE65 beim Aufbau der Maschinerie helfen, die die Sema5A-Mutation in eine physische Formveränderung der Zelle übersetzt. Die Arbeit fügt sich in ein größeres Bild ein, in dem kleine molekulare Schalter wie Arf6 und Rac1, unterstützt von Gerüsten wie FE65, als zentrale Knoten fungieren, die viele mit Autismus assoziierte Gene mit der endgültigen Architektur neuronaler Schaltkreise verbinden.
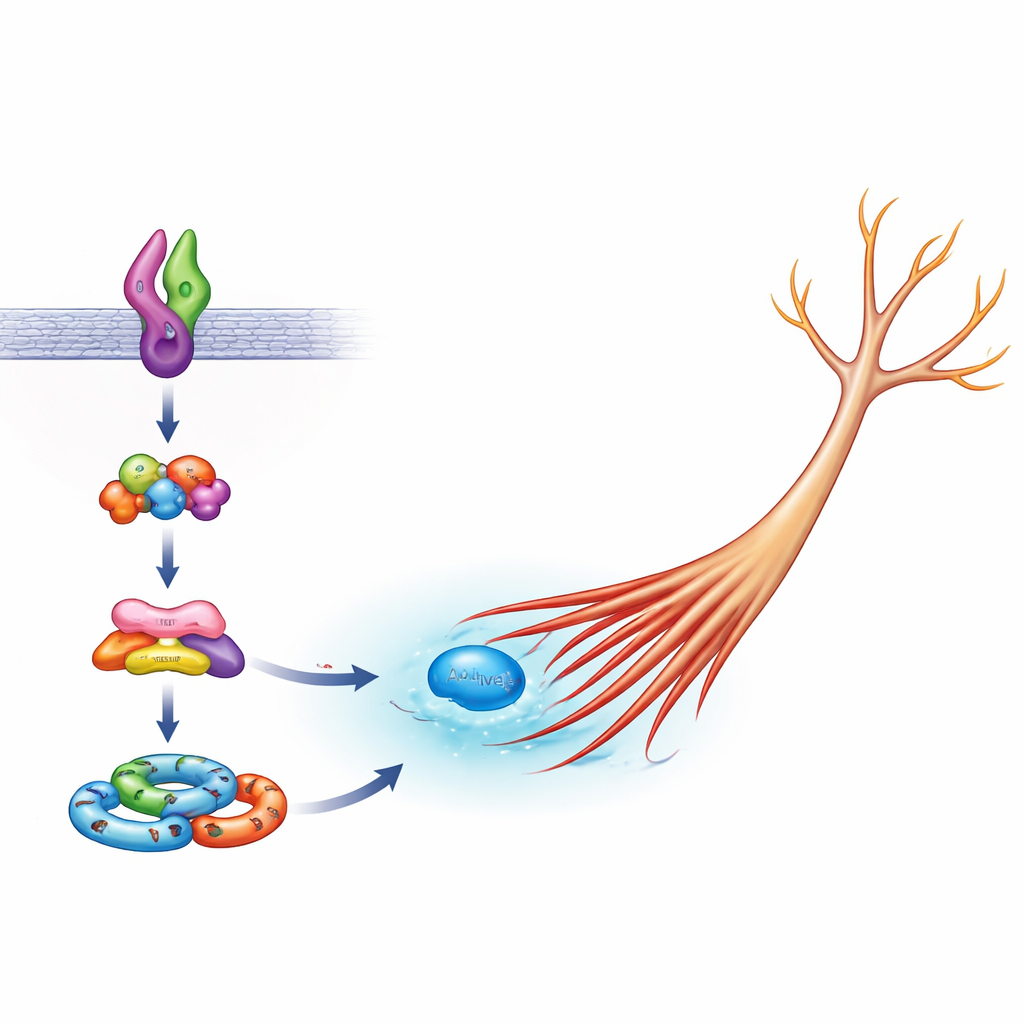
Warum diese mikroskopische Kette wichtig ist
Für Nicht‑Spezialisten kann die Buchstabensuppe der Proteinbezeichnungen weit entfernt vom gelebten Autismus‑Erleben erscheinen. Dennoch bietet diese Studie eine konkrete Brücke: Sie verfolgt nach, wie eine präzise genetische Veränderung in Sema5A eine bestimmte Kette von Helfermolekülen überaktivieren kann, wodurch Nervenzellen ihre Verzweigungen zu weit ausdehnen und das Gehirn möglicherweise auf atypische Weise verdrahten. Indem Arf6, FE65 und der ELMO2-Signalcomplex als entscheidende Glieder dieser Kette identifiziert werden, hebt die Arbeit potenzielle Ziele für zukünftige Medikamente hervor. Grundsätzlich könnten Wirkstoffe, die diesen überaktiven Weg behutsam dämpfen, eines Tages helfen, die zugrundeliegenden Formveränderungen der Zellen bei Sema5A‑assoziierten Formen von Autismus zu korrigieren und damit ein wichtiges Puzzlestück im Verständnis von neuroentwicklungsbedingten Störungen beizutragen.
Zitation: Takahashi, M., Yako, H., Miyamoto, Y. et al. Autism spectrum disorder-associated Sema5A p.Arg676Cys drives Arf6/FE65 signaling and aberrant cell morphogenesis. Sci Rep 16, 9423 (2026). https://doi.org/10.1038/s41598-026-39722-x
Schlüsselwörter: Autismus-Spektrum-Störung, Sema5A-Mutation, neurale Morphogenese, Rac1-Signalgebung, Arf6-FE65-Weg