Clear Sky Science · de
Tödliche Wirkungen von Ivermectin-Strukturen auf Malaria-Vektoren und in-silico-Analyse der Wechselwirkungen mit deren glutamatgesteuerten Chloridionenkanälen
Ein Entwurmungsmittel in einen Mückenkiller verwandeln
Ivermectin ist vor allem als Medikament gegen parasitäre Würmer beim Menschen und bei Nutztieren bekannt, hat aber eine überraschende Nebenwirkung: Mücken, die behandeltes Blut saugen, sterben häufig. Das weckt eine interessante Idee für die Malariabekämpfung — könnte die Gabe von Ivermectin an Menschen oder Tiere lokale Mückenpopulationen so schwächen, dass die Übertragung sinkt? Diese Studie untersucht eingehend, wie Ivermectin und verwandte Moleküle Anopheles-Mücken, die Malaria übertragen, töten und welche Veränderungen es eines Tages erlauben könnten, dass Mücken seinen Effekten entkommen.
Warum das Töten über Blut wichtig ist
Die traditionelle Malariakontrolle beruht auf Moskitonetzen und Insektizidsprays, die Mücken von außen angreifen. Ivermectin bietet eine andere Strategie: Wenn Menschen oder Tiere das Medikament einnehmen, wird ihr Blut für blutsaugende Mücken tödlich. Die Forschenden konzentrierten sich auf zwei wichtige südostasiatische Malariavektoren, Anopheles dirus und Anopheles minimus, die sich stark darin unterscheiden, wie leicht Ivermectin sie tötet. Durch den Vergleich dieser Arten hoffte das Team zu verstehen, warum das Medikament bei manchen Mücken wirksamer ist als bei anderen und wie die chemische Struktur diesen tödlichen Effekt beeinflusst.
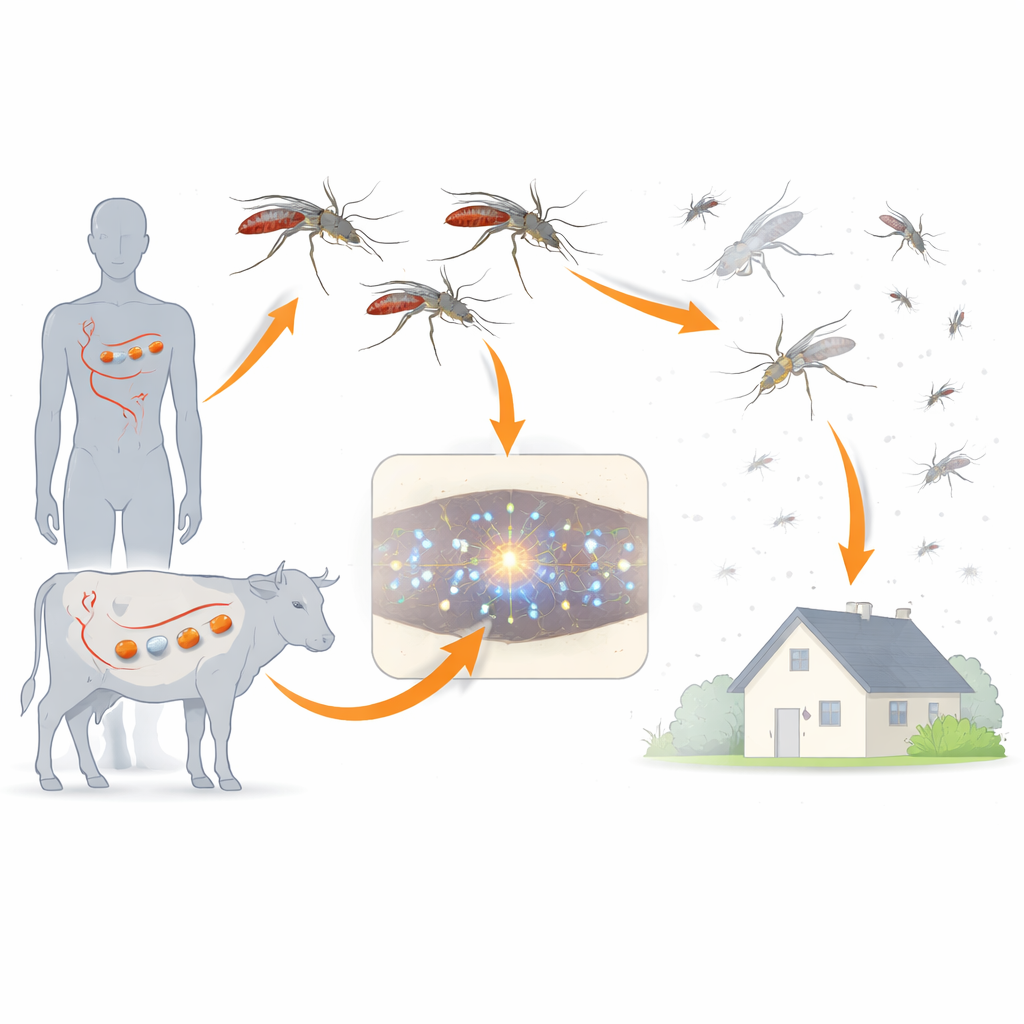
Welche Teile des Wirkstoffs eine Rolle spielen
Ivermectin ist ein voluminöses Molekül, das um einen großen Ring herum aufgebaut ist und zwei angehängte Zuckerringe trägt. Das Team verglich das vollständige Ivermectin (mit beiden Zuckern) mit einer Version mit nur einem Zuckerring (Monosaccharid genannt) und mit einem reduzierten Kern ohne Zucker (Aglykon). Diese Verbindungen wurden in unterschiedlichen Konzentrationen Tausenden von Mücken in Blutmahlzeiten gefüttert und die Überlebensraten über zehn Tage verfolgt. Das vollständige Ivermectin war hochgradig tödlich, insbesondere für An. minimus, während das Monosaccharid deutlich schwächer und das Aglykon bei realistischen Dosen fast wirkungslos war. Mit anderen Worten: Das Entfernen eines Zuckerrings verwandelte einen starken Mückenkiller in ein deutlich schwächeres Mittel, das Entfernen beider Ringe löschte die Wirkung nahezu aus.
Blick ins Nerventor der Mücke
Ivermectin wirkt an einem winzigen Tor in Nerven- und Muskelzellen, dem glutamatgesteuerten Chlorid-(GluCl-)Kanal. Wenn dieses Tor erzwungen geöffnet wird, strömen Chloridionen ein, die elektrische Aktivität bricht zusammen und die Mücke wird gelähmt und stirbt. Mithilfe fortschrittlicher Proteinstrukturvorhersage und Computer-Docking bauten die Forschenden dreidimensionale Modelle des Anopheles-GluCl-Kanals und simulierten, wie sich Ivermectin und seine Varianten in den Kanal einlagern. Sie fanden heraus, dass in Mücken ein spezifischer Abschnitt der Proteinschleife nahe der Pore — mit einer Aminosäure namens Threonin an Position 304 — eine Wasserstoffbrücke mit dem zweiten Zuckerring von Ivermectin bilden kann. Diese Bindung, zusammen mit schwächeren Anziehungen in der Umgebung, scheint eine durch das Medikament stabilisierte Konformation zu schaffen, die den Kanal offenhält.
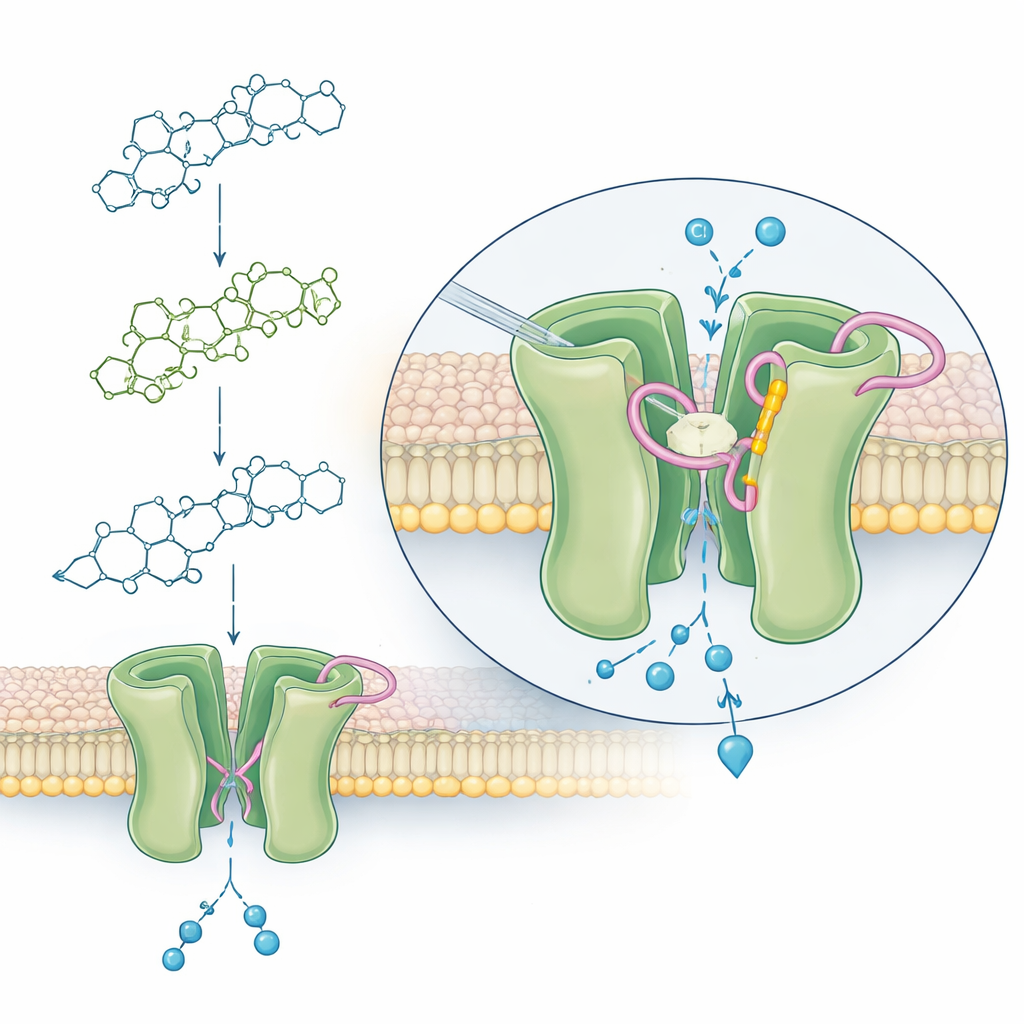
Warum manche Varianten töten und andere nicht
Die Simulationen zeigten ein konsistentes Muster: Vollständiges Ivermectin und drei wichtige Ivermectin-Abbauprodukte, die beim Menschen vorkommen, reichen tief in den Kanal hinein, sodass ihr zweiter Zuckerring eng mit der Schlüssel-Schleife interagieren kann. Diese Formen erzeugten alle starke prognostizierte Bindungen und erwiesen sich in früheren Arbeiten als ebenso tödlich für Mücken wie das Ausgangsmedikament. Das Monosaccharid, dem dieser zweite Zuckerring fehlt, konnte die Schleife nur schwach berühren, aber nicht dieselbe stabilisierende Bindung eingehen, was mit seiner deutlich geringeren Tödlichkeit übereinstimmt. Das Aglykon kam überhaupt nicht mit der Schleife in Kontakt, was mit seinem Versagen, Mücken in Fütterungstests zu töten, übereinstimmt. Über alle Strukturen hinweg trat zudem eine gemeinsame Wechselwirkung mit einem anderen Teil des Kanals (in der gegenüberliegenden Untereinheit) als wichtig hervor, was darauf hindeutet, dass mehrere Kontaktpunkte zusammenwirken, um das Tor offen zu halten.
Blick voraus: Resistenz und bessere Werkzeuge
Die Ergebnisse deuten darauf hin, dass der zweite Zuckerring von Ivermectin — und seine Fähigkeit, mit einer spezifischen Schleife des Mücken-GluCl-Kanals zu binden — zentral für seine mückenabtötende Wirkung ist. Dieses klarere Bild davon, wie das Medikament in den Kanal passt, hebt potenzielle Schwachstellen hervor, an denen zukünftige Mutationen die Bindung reduzieren und zu Resistenz führen könnten. Es liefert auch Hinweise, wie Chemiker Ivermectin-ähnliche Moleküle so verändern könnten, dass ihre Wirkung gegen Mücken erhalten bleibt oder verstärkt wird. Zwar stützt sich die Studie auf Computermodelle, die noch experimentell bestätigt werden müssen, doch sie untermauert die Argumentation für ivermectinbasierte Strategien als Teil des Malariabekämpfungs-Instrumentariums und zeigt molekulare Merkmale auf, die bei der Einführung solcher Strategien besonders beobachtet werden sollten.
Zitation: Nguyen, M.N., Jones, A.K., Hotwagner, D. et al. Lethal effects of ivermectin structures on malaria vectors and in silico analysis of interactions with their glutamate-gated chloride ion channels. Sci Rep 16, 8141 (2026). https://doi.org/10.1038/s41598-026-39698-8
Schlüsselwörter: ivermectin, Malaria-Vektoren, Anopheles-Mücken, Ionenkanäle, Insektenresistenz