Clear Sky Science · de
Frühe motorische Defizite, Schlafstörungen und Reduktion dopaminerger Neuronen in einem PARK7-/- Zebrafisch-Larvenmodell der Parkinson-Krankheit
Warum winzige Fische für eine große Hirnkrankheit wichtig sind
Die Parkinson-Krankheit wird meist erst diagnostiziert, wenn Menschen Zittern und Steifheit entwickeln, doch lange vorher laufen bereits subtile Veränderungen in Bewegung, Tastsinn und Schlaf ab. Diese Studie nutzt transparente Zebrafisch-Larven, nur wenige Tage alt, um frühe Merkmale der Parkinson-Krankheit in einem einfachen Tier nachzubilden. Indem die Forschenden beobachten, wie diese winzigen Fische schwimmen, schlafen und Berührung wahrnehmen, und ihre Gehirnzellen genau betrachten, entsteht ein leistungsfähiges neues Modell, das die Suche nach Behandlungen beschleunigen kann, die darauf abzielen, die Krankheit zu verlangsamen oder zu stoppen, nicht nur Symptome zu lindern. 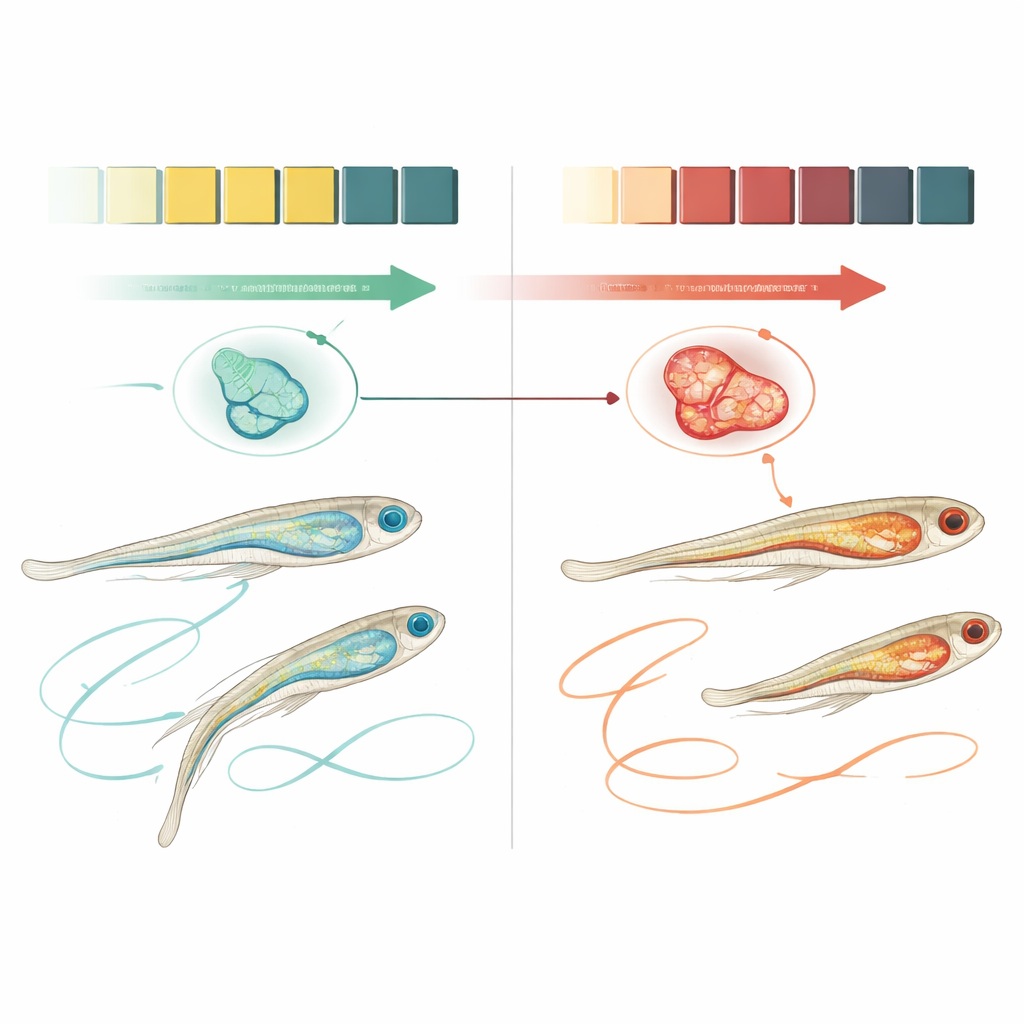
Ein Fischmodell der frühen Parkinson-Phase aufbauen
Das Team konzentrierte sich auf ein Gen namens PARK7, das ein Protein produziert, das Nervenzellen vor Stress schützt. In einigen Familien führen schädliche Veränderungen in diesem Gen zu einer frühen Form der Parkinson-Krankheit, und selbst bei typischen Fällen der Erkrankung erscheint dasselbe Protein im Hirngewebe oft beschädigt oder fehlgelagert. Mit Geneditierungstools erzeugten die Forschenden Zebrafische, denen PARK7 vollständig fehlt. Frühere Arbeiten zeigten, dass adulte Fische ohne dieses Gen Bewegungs- und andere hirnbezogene Probleme entwickeln. Hier stellten die Wissenschaftler eine grundlegendere Frage: Treten Probleme schon im Larvenstadium auf, wenn sich das Nervensystem noch entwickelt und die Tiere erst wenige Tage alt sind?
Bewegungs- und Tastsinnstörungen bei jungen Larven
Auf den ersten Blick wirkten die PARK7-losen Larven normal. Körperform, Augengröße und die frühesten Schwanzbewegungen direkt nach der Bildung ähnelten denen gewöhnlicher Fische. Doch fünf Tage nach der Befruchtung traten Unterschiede zutage. In einem Überwachungssystem, das das Schwimmverhalten über mehrere Tage erfasst, bewegten sich die mutanten Larven während ihrer üblichen tagsüber aktiven Phase weniger als ihre gesunden Geschwister. Das Team testete außerdem einen einfachen Reflex: ein sanfter Reiz am Kopf oder Schwanz mit einer Pipettenspitze. Gesunde Larven schossen fast immer weg, wohingegen PARK7-defiziente Larven deutlich weniger reaktionsfreudig waren, was der verminderten Berührungsempfindung ähnelt, die bei Menschen mit Parkinson häufig berichtet wird. Ein chemisches Toxin namens MPP+, das selektiv dieselbe Art von Gehirnzellen schädigt, die bei Parkinson betroffen sind, schwächte diese Berührungsantwort bei normalen und mutanten Fischen weiter und zeigte, dass diese Schaltkreise besonders verletzlich sind. 
Schlafveränderungen spiegeln frühe Warnzeichen wider
Schlafprobleme treten meist Jahre vor den klassischen Bewegungsstörungen der Parkinson-Krankheit auf. Die Zebrafisch-Larven boten eine Möglichkeit, Schlaf und Aktivität rund um die Uhr unter kontrollierten Hell–Dunkel-Zyklen zu verfolgen. Alle Fische zeigten einen Tagesrhythmus, waren im Licht aktiver und in der Dunkelheit ruhiger. PARK7-losen Larven jedoch fiel das Einschlafen nach Lichtausfall schwerer, und sie verbrachten während der Lichtphase mehr Zeit schlafend als üblich — ein Muster, das einer erhöhten Tagesmüdigkeit ähnelt. Interessanterweise blieben diese Schlafveränderungen über mehrere Tage bestehen, selbst als die Gesamtbewegung schwankte. Die toxinbehandelten normalen Fische entwickelten nicht dasselbe Schlafmuster, was unterstreicht, dass der genetische Verlust von PARK7 nichtmotorische Merkmale erfasst, die im gängigen Toxinmodell fehlen.
Verlust von Gehirnzellen im „Bewegungszentrum“ der Fische
Um Verhalten mit Veränderungen im Gehirn zu verknüpfen, untersuchten die Forschenden einen spezifischen Zellcluster dopaminproduzierender Nervenzellen im Diencephalon der Zebrafische. Diese Gruppe entspricht eng der menschlichen Substantia nigra, der Region, die bei der Parkinson-Krankheit degeneriert. Mithilfe fluoreszenter Markierung und Konfokalmikroskopie zählten sie diese Zellen zu mehreren frühen Zeitpunkten. Bereits nach fünf Tagen hatten Larven ohne PARK7 deutlich weniger dieser Dopaminneurone als normale Fische, und das Defizit vergrößerte sich, als die Larven von drei auf fünf Tage heranwuchsen. Andere nahegelegene Dopaminzellgruppen blieben unverändert, was darauf hinweist, dass der Verlust auf dieselbe besonders verwundbare Population fokussiert ist, wie sie auch beim Menschen beobachtet wird. Die Zugabe von MPP+ verringerte die Zellzahlen sowohl bei normalen als auch bei mutanten Fischen weiter, doch die Mutanten zeigten in diesem frühen Stadium keine dramatisch erhöhte Empfindlichkeit gegenüber ihren Wildtyp-Geschwistern.
Wie dieses winzige Modell den Menschen helfen kann
Insgesamt zeigt die Arbeit, dass Zebrafisch-Larven ohne PARK7 bereits eine Kombination aus reduzierter Bewegung, abgeschwächten Berührungsreaktionen, gestörtem Schlaf und einem selektiven Rückgang zentraler dopaminerger Neuronen aufweisen. Das sind Kennzeichen der Parkinson-Krankheit, komprimiert in ein schnelles, transparentes und genetisch definiertes System. Für Nicht-Spezialisten lautet die Kernbotschaft: Winzige, durchsichtige Fische können nun nicht nur die offensichtlichen motorischen Zeichen der Parkinson-Krankheit nachahmen, sondern auch die früheren, leiseren Symptome, die häufig unbemerkt bleiben. Da Wirkstoffe direkt ins Wasser gegeben werden können und viele Larven gleichzeitig getestet werden können, eignet sich dieses Modell gut, um Verbindungen zu finden, die verletzliche Gehirnzellen schützen oder frühe Schlaf- und Sensorikprobleme korrigieren — ein vielversprechender Weg zu Therapien, die die Wurzeln der Parkinson-Krankheit angehen statt nur ihre sichtbaren Folgen.
Zitation: Solheim, N., Pinho, B.R., Oliveira, N.A.S. et al. Early motor deficits, sleep dysfunction and reduction in dopaminergic neurons in a PARK7-/- zebrafish larval model of Parkinson’s disease. Sci Rep 16, 9525 (2026). https://doi.org/10.1038/s41598-026-39692-0
Schlüsselwörter: Parkinson-Krankheit, Zebrafisch-Modell, Dopamin-Neuronen, Schlafstörungen, DJ-1 PARK7