Clear Sky Science · de
Gezielte Ansprache spezifischer Neuronentypen im Gehirn nicht-menschlicher Primaten mittels eines rekombinanten Immunotoxins, das an murines CD25 bindet
Warum diese Hirnstudie wichtig ist
Zu verstehen, wie bestimmte Gruppen von Gehirnzellen Bewegung, Emotionen und Verhalten steuern, ist entscheidend für die Behandlung von Erkrankungen wie Parkinson und Autismus. Das Gehirn ist jedoch ein dichtes Geflecht miteinander verflochtener Zellen, und die meisten Werkzeuge treffen viele Zelltypen gleichzeitig. Diese Studie stellt eine Methode vor, nur einen ausgewählten Neuronentyp im Affengehirn zu entfernen, bei minimalem Kollateralschaden, und ermöglicht damit deutlich präzisere Experimente dazu, wie bestimmte Schaltkreise Verhalten und Krankheit formen.
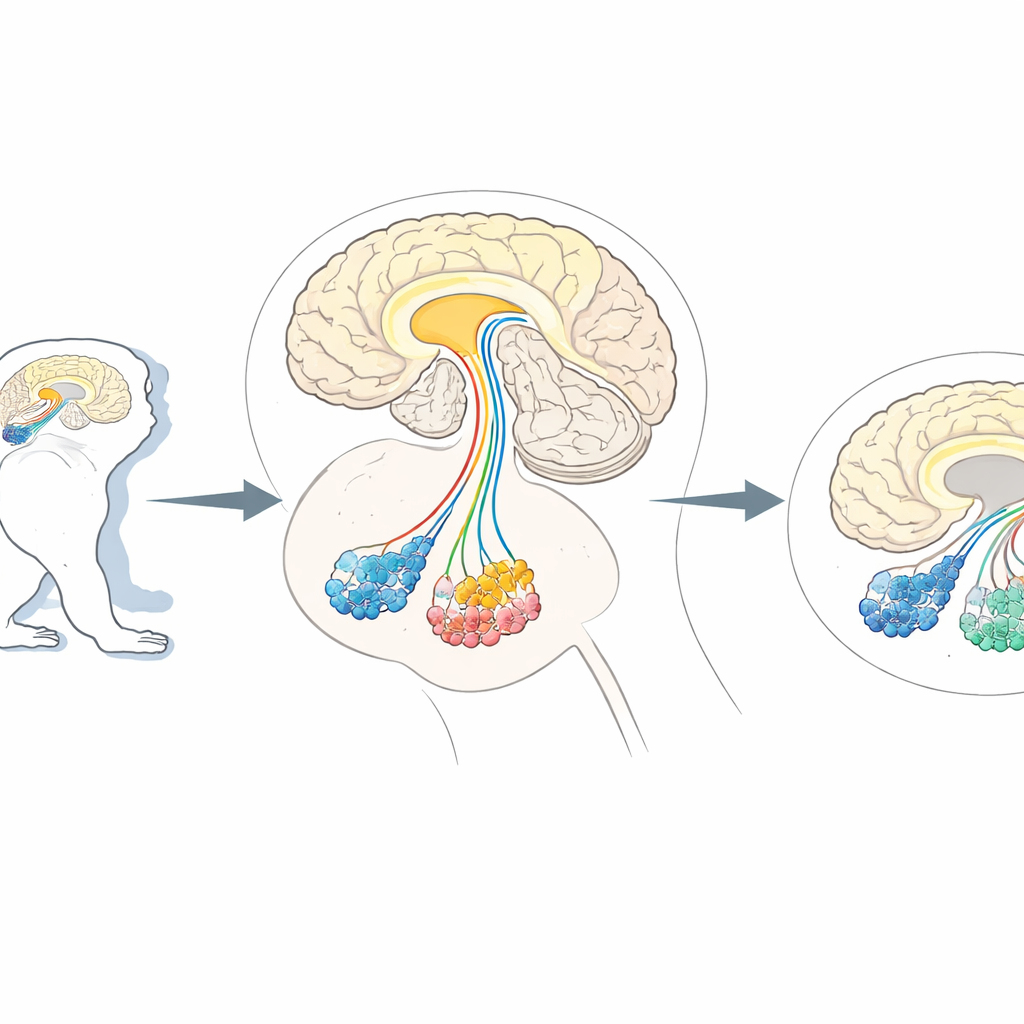
Der Bedarf an präzisem „Zellbeschnitt“ im Gehirn
Forscher greifen häufig auf nicht-menschliche Primaten wie Marmosetten und Makaken zurück, weil ihre Gehirne unserer Organisation sehr ähneln. Diese Tiere sind wertvolle Modelle für Störungen, die höhere Gehirnfunktionen betreffen – von Parkinson-ähnlichen Bewegungsproblemen bis hin zu autismusähnlichen Veränderungen im Sozialverhalten. Bestehende Methoden können bestimmte Bahnen stummschalten oder aktivieren, aber in diesen komplexen Gehirnen wirklich nur einen Neuronentyp zu entfernen, ohne andere zu schädigen, blieb schwierig. Frühere Arbeiten in Mäusen nutzten einen Trick: ausgewählte Neurone wurden so verändert, dass sie einen zellulären Oberflächenmarker namens CD25 zeigten, der von einem konstruierten Toxin erkannt wird und nur die markierten Zellen tötet. Dieser Marker kommt jedoch natürlicherweise in primaten Immunzellen und möglicherweise auch im Gehirn vor, was das Risiko birgt, dass das Toxin in Affen falsche Zielzellen angreift.
Entwicklung eines sichereren molekularen Skalpells
Die Autoren machten sich daran, ein neues molekulares Skalpell für den Einsatz in Primaten zu entwickeln. Anstatt die menschliche Form von CD25 anzusprechen, konzentrierten sie sich auf die murine Variante, die deutlich weniger Ähnlichkeit mit dem natürlichen CD25 der Primaten aufweist. Zunächst immunisierten sie ein Kaninchen mit dem murinen CD25-Protein und nutzten eine chipbasierte Methode, um einzelne Kaninchenzellen zu isolieren, die Antikörper produzierten, die stark an murines CD25, aber nicht an die humane Form binden. Daraus identifizierten sie einen herausragenden Antikörper, genannt RMAb-52, mit sehr hoher Bindungsstärke. Die Schlüsselteile dieses Antikörpers kombinierten sie anschließend mit einem toxischen Fragment des Bakteriums Pseudomonas, um ein einzelnes konstruiertes „Immunotoxin“-Protein zu erzeugen, das anti-mCD25-PE38 genannt wurde.
Das Werkzeug auf die Probe gestellt
In Reagenzglas-Experimenten heftete sich das neue Immunotoxin deutlich fester an murines CD25 als an humanes CD25, was seine Selektivität bestätigte. Auf kultivierten Zellen, die murines CD25 tragen, reduzierte das Toxin das Überleben bereits bei sehr niedrigen Dosen stark, während Zellen mit humanem CD25 unversehrt blieben. Anschließend ging das Team zu lebenden Marmosetten über. Mit einem speziellen viralen Vektor, der retrograd entlang von Nervenfasern transportiert wird, brachten sie das Gen für murines CD25 in dopaminproduzierende Neurone ein, die Signale von einer tiefen Hirnregion, der Substantia nigra, zum Striatum senden – einer Bahn, die für die Bewegungssteuerung entscheidend ist. Nachdem dem Virus Zeit gegeben worden war, den Marker in diesen Neuronen zu aktivieren, injizierten sie das anti-mCD25-PE38-Protein direkt in das Zielgebiet im Mittelhirn.
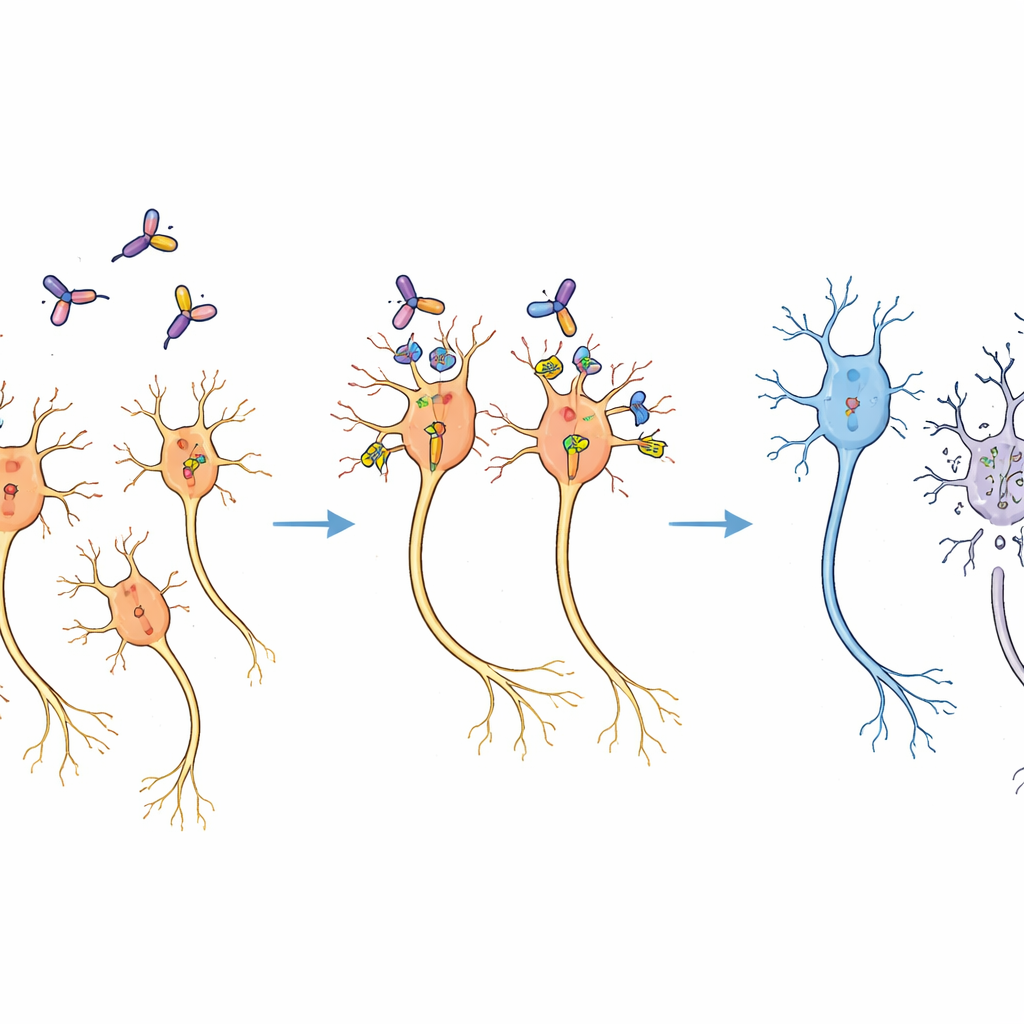
Selektiver Verlust ohne großflächige Schäden
Zwei Wochen nach der Behandlung ergaben Gehirnschnitte der Marmosetten ein klares Bild. Auf der Seite, die das Immunotoxin erhalten hatte, war die Zahl der Dopaminneurone auf etwa zwei Drittel derjenigen der unbehandelten Seite reduziert, wie eine Färbung für ein dopaminbildendes Enzym zeigte. Das umliegende Gewebe wirkte im Mikroskop normal, und andere Hirnregionen, die ebenfalls den viralen Vektor erhielten, zeigten keinen offensichtlichen Zellverlust. Pilotversuche hatten bereits einen Dosisbereich etabliert, der unspezifische Gewebeschäden vermeidet, und die gewählte Dosis lag gut innerhalb dieses sicheren Bereichs. Das Muster des Verlusts entsprach der erwarteten Ausbreitung von Virus und Toxin, was darauf hindeutet, dass Neurone gezielt eliminiert wurden, weil sie so verändert wurden, dass sie murines CD25 zeigten – und nicht, weil das Toxin Zellen unselektiv beschädigte.
Was das für die zukünftige Hirnforschung bedeutet
Für eine nicht-fachkundige Leserschaft ist die Kernbotschaft, dass die Forscher einen hochselektiven „Löschknopf“ für ausgewählte Neuronenpopulationen in Primatenhirnen entwickelt haben. Durch die Kombination eines retrograden viralen Liefersystems mit einem maus-spezifischen Immunotoxin können definierte Bahnen – etwa dopaminerge Schaltkreise, die bei der Parkinson-Krankheit eine Rolle spielen – entfernt werden, während benachbarte Zellen verschont bleiben. Diese Strategie vermeidet gefährliche Kreuzreaktionen mit dem körpereigenen CD25 der Tiere und ist besonders nützlich, wenn dieser natürliche Rezeptor in der Krankheit vorhanden oder erhöht ist. Langfristig wird dieser Ansatz Wissenschaftlern helfen, nachzuzeichnen, wie einzelne Leitungsbahnen im Gehirn zu Bewegung, Entscheidungsfindung und psychiatrischen Symptomen beitragen, und uns näher an gezielte Therapien bringen, die fehlerhafte Schaltkreise korrigieren, statt das gesamte Gehirn breit zu beeinflussen.
Zitation: Kobayashi, T., Kato, S., Kimura, S. et al. Targeting of specific neuronal types in the non-human primate brain by using a murine CD25-specific recombinant immunotoxin. Sci Rep 16, 8247 (2026). https://doi.org/10.1038/s41598-026-39662-6
Schlüsselwörter: Neuroscience nicht-menschlicher Primaten, Immunotoxin-Targeting, Dopaminerge Neurone, Schaltkreise im Marmosetengehirn, Modelle der Parkinson-Krankheit