Clear Sky Science · de
Kälteinduzierbares RNA‑bindendes Protein fördert die Aktivierung von Fibroblasten und seine Hemmung stellt ein potenzielles therapeutisches Ziel bei pulmonaler Fibrose dar
Warum Lungenvernarbung wichtig ist
Pulmonale Fibrose ist ein Zustand, bei dem sich die Lungen allmählich von weichem, dehnbarem Gewebe in steifes, narbenartiges Material verwandeln. Wenn sich die Vernarbung ausbreitet, wird das Atmen schwerer und die Sauerstoffwerte sinken; viele Patientinnen und Patienten sterben innerhalb weniger Jahre nach der Diagnose. Aktuelle Medikamente können das Fortschreiten verlangsamen, verändern aber selten die langfristige Prognose. Diese Studie untersucht ein stressreaktives Protein namens CIRBP und stellt eine einfache Frage mit großen Folgen: Treibt dieses Protein die Lungenvernarbung voran, und wenn ja, kann seine Blockade die Lunge schützen?
Ein Stresssignal, das offen zutage liegt
CIRBP wird normalerweise in vielen Zelltypen gebildet, wenn sie Stress ausgesetzt sind, etwa Kälte, Sauerstoffmangel oder toxische Schäden. Innerhalb der Zelle stabilisiert es RNA, die Botschaften, die den Zellen sagen, welche Proteine sie herstellen sollen. CIRBP kann jedoch auch aus den Zellen entweichen oder sezerniert werden und verhält sich außerhalb der Zelle eher wie ein Alarmsignal, das Entzündungen anheizt. Frühere klinische Arbeiten zeigten, dass Menschen mit idiopathischer pulmonaler Fibrose mehr CIRBP in ihrem vernarbten Lungengewebe und im Blut haben und dass höhere Werte mit schlechteren Verläufen korrelieren. Die neue Studie wollte prüfen, ob CIRBP lediglich ein Stillstehender ist, der Gewebsstress widerspiegelt, oder ein aktiver Akteur, der die Erkrankung vorantreibt.
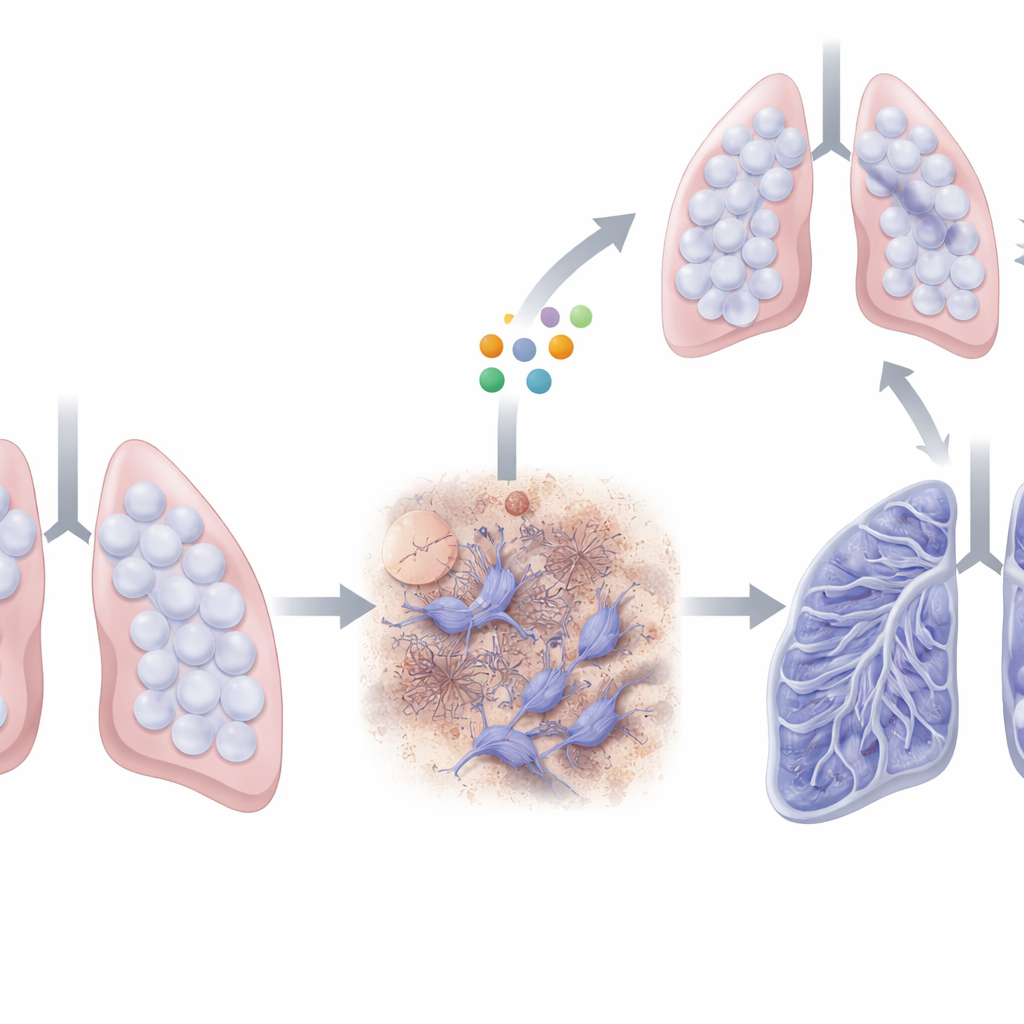
CIRBP im Test in erkrankten Lungen
Die Forscher verwendeten ein übliches Mausmodell der Lungenfibrose, bei dem das Chemotherapeutikum Bleomycin direkt in die Atemwege eingebracht wird und über mehrere Wochen Verletzung und Vernarbung auslöst. Sie verglichen normale Mäuse mit genetisch veränderten Tieren, denen CIRBP fehlt. Nach Bleomycin‑Einwirkung zeigten normale Mäuse einen starken Anstieg von CIRBP, besonders in den am stärksten fibrotischen Bereichen der Lunge. Im Gegensatz dazu überlebten Mäuse ohne CIRBP länger, wiesen weniger sichtbare Vernarbungen in Gewebeschnitten auf und hatten niedrigere Werte an Kollagen und anderen fibrotischen Markern. Diese Befunde deuten darauf hin, dass CIRBP nicht nur vorhanden ist, sondern aktiv zum Aufbau von Narbengewebe beiträgt.
Wie CIRBP Fibroblasten in Überdrive versetzt
Um den Mechanismus näher zu untersuchen, isolierte das Team primäre Fibroblasten, die Bindegewebszellen, die Kollagen ablagern und zentral für die Fibrose sind. Wenn sie gereinigtes CIRBP zu diesen Zellen in Kultur hinzufügten, sezernierten die Fibroblasten mehr Kollagen, teilten sich schneller und bewegten sich leichter – Verhaltensweisen, die zusammen die Ausbreitung von Narbengewebe begünstigen. Interessanterweise erhöhte CIRBP nicht eindeutig die klassischen Marker vollständig umgewandelter „Myofibroblasten“ innerhalb der Zellen, was darauf hindeutet, dass es hauptsächlich deren Aktivität moduliert, statt ihre Identität grundlegend zu verändern. Genexpressionsanalysen zeigten, dass CIRBP‑behandelte Fibroblasten viele Immun‑ und Entzündungsgene hochfuhren, und Proteinanalyse hob ein Molekül besonders hervor: das Zytokin IL‑6, das als Reaktion auf CIRBP stark anstieg.
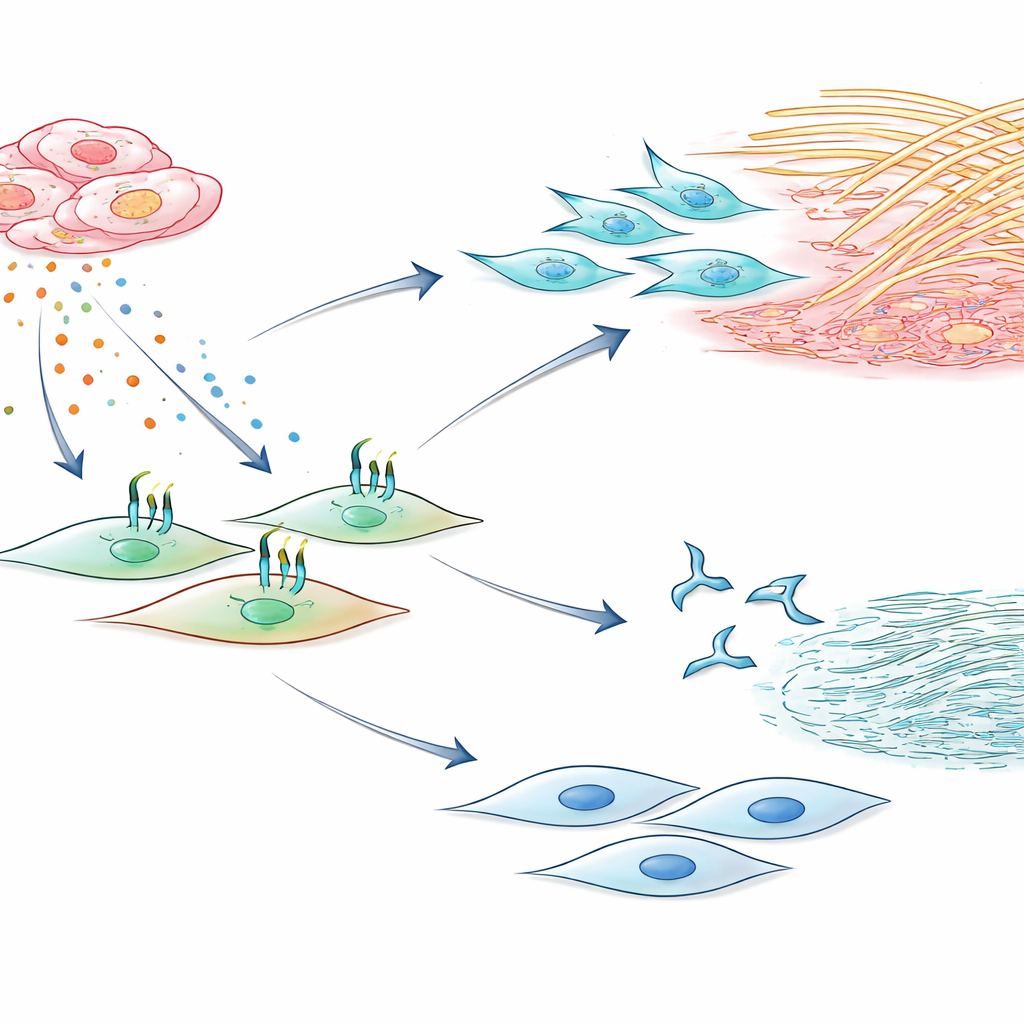
Eine Signalkette, die unterbrochen werden kann
Die Studie kartierte anschließend die Signalkette, die CIRBP mit der Aktivierung von Fibroblasten verbindet. CIRBP außerhalb der Zelle scheint zwei angeboren‑immunologische Rezeptoren auf Fibroblasten zu binden, bekannt als TLR2 und TLR4. Wenn diese Rezeptoren CIRBP wahrnahmen, sezernierten die Zellen mehr IL‑6, das wiederum in einem autokrinen Kreis auf dieselben Fibroblasten zurückwirkte und die Kollagenausschüttung sowie das Zellwachstum weiter verstärkte. Das Blockieren von IL‑6 mit neutralisierenden Antikörpern reduzierte die Kollagensekretion und Proliferation und bestätigte damit seine zentrale Rolle in dieser Schleife. Ebenso schwächten Wirkstoffe, die TLR2 oder TLR4 hemmen, CIRBP‑vermittelte Effekte auf IL‑6, Kollagen und Zellteilung ab. Am auffälligsten reduzierte ein kurzes Peptid namens C23, das aus CIRBP selbst abgeleitet wurde und dafür entworfen ist, mit diesen Rezeptoren um Bindung zu konkurrieren, stark die IL‑6‑Produktion und die nachgelagerten fibrotischen Verhaltensweisen in kultivierten Fibroblasten.
Peptidbehandlung, die den Schlag abschwächt
Abschließend prüften die Wissenschaftler, ob die gezielte Hemmung von CIRBP Tieren mit bereits bestehender Lungenverletzung nützt. Im Bleomycin‑Modell begannen sie eine Woche nach der initialen Schädigung mit C23‑Injektionen, also zu einem Zeitpunkt, an dem die Schäden bereits im Gange sind. Im Vergleich zu Placebo überlebten C23‑behandelte Mäuse besser, zeigten auf Histologie mildere Vernarbungen und hatten einen geringeren Lungenkollagengehalt sowie reduzierte Spiegel von fibrose‑assoziierten Proteinen. Diese Ergebnisse deuten darauf hin, dass die Blockade der CIRBP‑Signalgebung den Verlauf der Lungenfibrose spürbar abschwächen kann, selbst wenn die Behandlung erst nach Auftreten der Verletzung beginnt.
Was das für künftige Lungenbehandlungen bedeutet
Für Nichtfachleute ist die Kernbotschaft, dass die Studie CIRBP als stressinduziertes Alarmprotein identifiziert, das die Lungenvernarbung fördert, indem es Fibroblasten über eine TLR2/TLR4–IL‑6‑Signalkette in einen aggressiveren, kollagen‑sezernierenden Zustand versetzt. Das Unterbrechen dieser Kette, insbesondere mit dem C23‑Peptid, milderte die Fibrose und verbesserte das Überleben bei Mäusen. Obwohl noch viel Arbeit nötig ist, bevor ein solcher Ansatz Patienten erreichen kann, rückt CIRBP nun als vielversprechendes, upstream‑gerichtetes Ziel in den Fokus: Die Abschwächung seines Signals könnte tödliche Lungenvernarbung verlangsamen oder verhindern und dabei große Teile der normalen Immunabwehr intakt lassen.
Zitation: Mochizuka, Y., Hozumi, H., Watanabe, H. et al. Cold inducible RNA binding protein promotes fibroblast activation and its inhibition represents a potential therapeutic target in pulmonary fibrosis. Sci Rep 16, 8324 (2026). https://doi.org/10.1038/s41598-026-39649-3
Schlüsselwörter: pulmonale Fibrose, Fibroblasten, CIRBP, IL‑6‑Signalgebung, Lungenvernarbung