Clear Sky Science · de
Der hypoxieinduzierbare Faktor 1α übt duale Rollen beim Fortschreiten von Blasenkrebs über die TIMP3-vermittelte Regulation von Angiogenese und Invasion aus
Warum sauerstoffarme Tumoren wichtig sind
Krebszellen wachsen oft so schnell, dass sie ihre Blutversorgung überholen und Teile eines Tumors unter Sauerstoffmangel geraten. Diese sauerstoffarme, also hypoxische, Umgebung zwingt Zellen dazu, Überlebensprogramme zu aktivieren, die Krebserkrankungen schwerer behandelbar machen können. Beim Blasenkrebs — einem häufigen Tumor des Harntrakts — vermuteten Wissenschaftler lange, dass ein solches oxygensensitives Programm, gesteuert von einem Protein namens HIF-1α, vor allem das Tumorwachstum und die Ausbreitung fördert. Diese Studie geht dem genauer nach und zeigt eine überraschende Wendung: Unter bestimmten Bedingungen kann eine Reduktion von HIF-1α Blasenkrebszellen tatsächlich aggressiver machen, und ein zweites Protein, TIMP3, steht im Zentrum dieses Paradoxons.
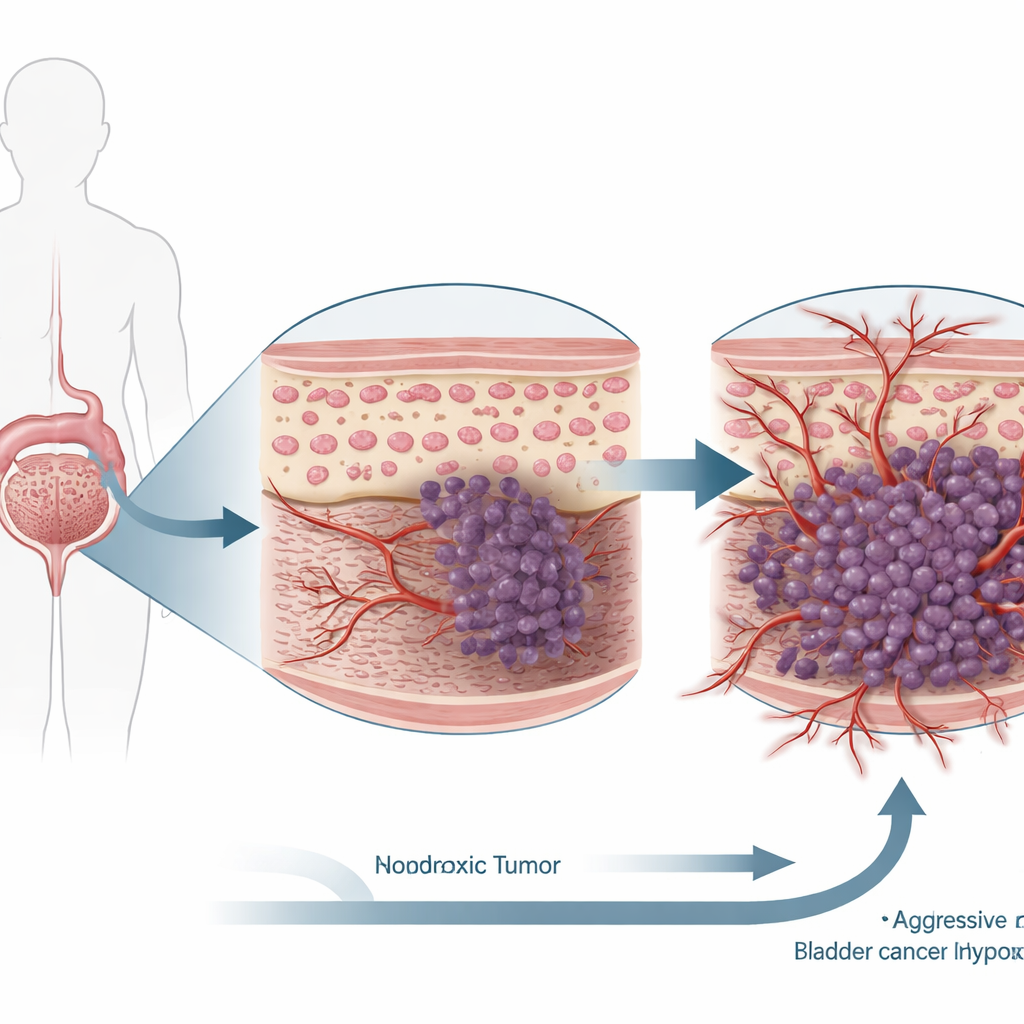
Ein genauerer Blick auf Blasenkrebszellen
Die Forschenden arbeiteten mit zwei etablierten menschlichen Blasenkrebszelllinien und setzten sie entweder normalen Sauerstoffbedingungen oder Hypoxie aus, um die sauerstoffarmen Nischen in echten Tumoren nachzuahmen. Anschließend nutzten sie genetische Werkzeuge, um HIF-1α in diesen Zellen herunterzuregulieren, und maßen, wie sich diese Veränderung auf grundlegende Krebsmerkmale auswirkte: wie schnell sich die Zellen vermehrten, wie anfällig sie für Zelltod waren und wie gut sie sich bewegen, in Barrieren eindringen und neues Blutgefäßwachstum fördern konnten. Parallel untersuchten sie Blasentumorproben von Patientinnen und Patienten, um die Spiegel von HIF-1α und TIMP3 im Tumorgewebe mit dem benachbarten normalen Blasenepithel zu vergleichen.
Eine überraschende Rollenkehrung unter Sauerstoffmangel
Die Patientenproben bestätigten, dass HIF-1α in Blasentumoren tatsächlich höher ist als im Normalgewebe, was seiner Reputation als tumorfördernder Faktor entspricht. Doch in den Zellexperimenten unter Hypoxie hatte die Reduktion von HIF-1α das Gegenteil dessen zur Folge, was viele erwartet hätten. Wurde HIF-1α herabreguliert und war wenig Sauerstoff vorhanden, wuchsen die Krebszellen über die Zeit schneller, gingen seltener in den programmierten Zelltod und waren besser in Migration und Invasion durch Modellbarrieren. Sie setzten außerdem Signale frei, die Endothelzellen dazu anregten, dichtere und ausgedehntere röhrenförmige Netzwerke zu bilden — ein Kennzeichen erhöhter Tumorversorgung durch Blutgefäße. Kurz gesagt: Mit weniger HIF-1α in einer sauerstoffarmen Umgebung verhielten sich Blasenkrebszellen maligner.
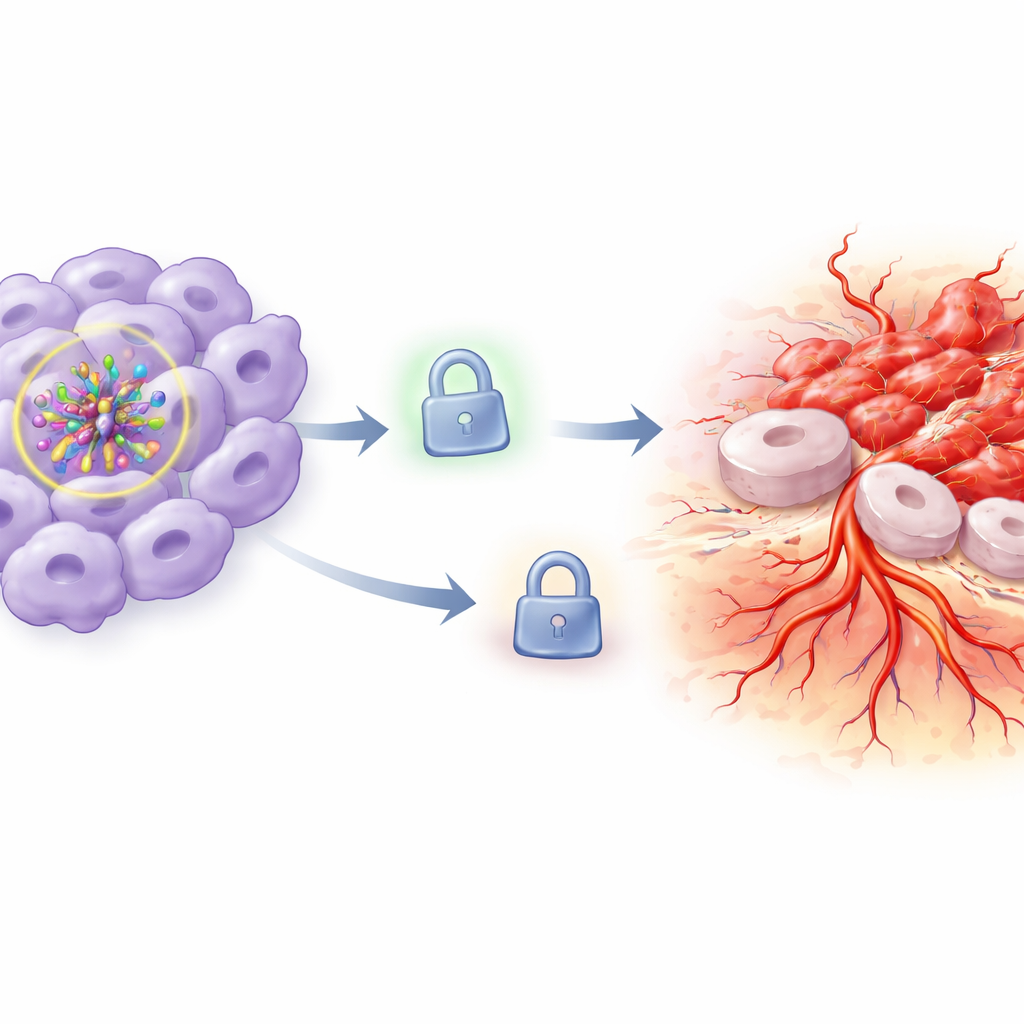
Die fehlende Bremse der Tumorausbreitung
Um zu verstehen, warum das geschah, konzentrierte sich das Team auf TIMP3, ein Protein, das normalerweise als Bremse des Gewebeabbaus und des Gefäßneubaus wirkt, indem es Enzyme blockiert, die die umgebende Matrix zersetzen. In HIF-1α-verminderten Zellen unter normalen Sauerstoffbedingungen blieben die TIMP3-Spiegel relativ hoch. Fielen die Sauerstoffwerte jedoch, sank das TIMP3-Protein stark. Dieser Verlust an TIMP3 passte gut zu dem beobachteten Anstieg von Invasion und Gefäßbildung: Mit abgeschwächter Bremse konnten Krebszellen ihre Umgebung leichter umgestalten und expandieren. Die Forschenden schalteten dann um, indem sie die Zellen zwangen, zusätzliches TIMP3 zu produzieren, während HIF-1α weiterhin herunterreguliert war und Hypoxie herrschte. Die Wiederherstellung von TIMP3 kehrte das aggressive Verhalten teilweise oder nahezu vollständig um: Die Zellen wuchsen weniger, starben leichter, bewegten sich und drangen weniger ein und lösten weniger sowie kürzere gefäßähnliche Strukturen aus.
Was das für künftige Behandlungen bedeutet
Diese Ergebnisse deuten darauf hin, dass HIF-1α beim Blasenkrebs eine doppelte Persönlichkeit besitzt. Einerseits sind seine Gesamtspiegel in Tumoren erhöht und es treibt bekannte tumorfördernde Programme voran. Andererseits scheint es unter starkem Sauerstoffmangel dazu beizutragen, das schützende Vorhandensein von TIMP3 aufrechtzuerhalten. Das Entfernen von HIF-1α in diesem Kontext kann unbeabsichtigt TIMP3 senken und invasivere, gefäßfördernde Eigenschaften freisetzen. Für die Therapie bedeutet dies, dass eine einfache Blockade von HIF-1α nach hinten losgehen kann, sofern nicht gleichzeitig Wege gefunden werden, TIMP3 oder ähnliche Bremsen zu erhalten. Die Arbeit unterstreicht die Bedeutung, nicht nur einzelne Ziele, sondern das breitere Netzwerk von Kontrollen und Gleichgewichten zu verstehen, die bestimmen, wie ein Tumor auf seine raue, sauerstoffarme Umgebung reagiert.
Zitation: Wang, X., Guo, J., Zhang, R. et al. Hypoxia-inducible factor 1α exerts dual roles in bladder cancer progression through TIMP3-mediated regulation of angiogenesis and invasion. Sci Rep 16, 8425 (2026). https://doi.org/10.1038/s41598-026-39635-9
Schlüsselwörter: Blasenkrebs, Tumorhypoxie, HIF-1α, TIMP3, Angiogenese