Clear Sky Science · de
Molekulares Docking und Dynamik zeigen neuartige CDK6‑Inhibitoren für eine zielgerichtete Glioblastom‑Therapie
Warum diese Gehirntumor‑Studie wichtig ist
Das Glioblastom ist eine der aggressivsten Formen von Hirntumoren, und für viele Patientinnen und Patienten reichen die heutigen Therapien noch nicht aus oder wirken nicht lang genug. Diese Studie untersucht einen neuen Ansatz, um das Glioblastom anzugreifen, indem sie eine einzelne überaktivierte Schaltstelle in Tumorzellen ins Visier nimmt — ein Protein namens CDK6. Statt mit Tieren oder Reagenzgläsern arbeiteten die Forschenden mit fortgeschrittenen Computersimulationen, durchsuchten Hunderte von wirkstoffähnlichen Molekülen und identifizierten einen besonders vielversprechenden Kandidaten, bezeichnet als Verbindung 21, die eines Tages helfen könnte, diese tödliche Erkrankung zu verlangsamen oder zu stoppen.
Ein tödlicher Tumor, der aktuellen Behandlungen ausweicht
Glioblastome wachsen schnell, dringen in benachbartes Hirngewebe ein und treten nach Operation, Strahlentherapie und Chemotherapie fast immer wieder auf. Standardmedikamente wie Temozolomid können die Tumoren zunächst verkleinern, doch viele Krebszellen passen sich an und werden resistent, was zu Rückfällen führt. Ein Grund ist, dass ihre interne Teilungsmaschinerie dauerhaft auf "Start" steht. Proteine namens CDKs fungieren als Zeitgeber, die der Zelle sagen, wann sie ihre DNA kopieren und sich teilen soll. Beim Glioblastom ist der CDK4/6‑Signalweg häufig überaktiv und treibt die Zellteilung weiter voran, selbst unter Strahlen‑ und medikamentöser Behandlung. Das macht CDK6 zu einem attraktiven Ziel: Wenn Forschende es gezielt in Tumorzellen ausschalten könnten, ließe sich das Wachstum bremsen und die Wirksamkeit bestehender Therapien verbessern.
Auf der Suche nach einem besseren CDK6‑Blocker am Computer
Statt im Labor zu beginnen, führte das Team eine großangelegte virtuelle Suche durch. Ausgehend von einem bereits bekannten CDK6‑bindenden Molekül ließ ein Screening‑Programm Hunderte ähnlicher Strukturen aus einer Wirkstoffdatenbank finden. Von den anfänglich 400 Kandidaten wurden 109 für ein detailliertes Computerdocking gegen die 3‑D‑Struktur des menschlichen CDK6 ausgewählt. Docking ist wie das Ausprobieren vieler Schlüssel in einem Schloss: die Software sagt voraus, welche Moleküle am besten in die aktive Tasche des Proteins passen und wie stark sie binden könnten. Achtundvierzig Kandidaten sahen sogar besser aus als das ursprüngliche Referenzmolekül, doch einer, Verbindung 21, stach hervor mit der stärksten vorhergesagten Bindung und besonders günstigen Kontakten an spezifischen Stellen von CDK6, die für Selektivität bekannt sind.
Prüfen, ob das „virtuelle Medikament“ sich wie ein echtes Arzneimittel verhält
Starke Bindung ist nur ein Teil der Geschichte; ein brauchbares Medikament muss zudem das Gehirn erreichen, sich gut lösen und gesunde Gewebe schonen. Die Forschenden nutzten weitere Programme, um vorherzusagen, wie jedes Top‑Kandidat aufgenommen, im Körper verteilt und ausgeschieden würde. Verbindung 21 bestand die üblichen Regeln zur "Drug‑Likeness", zeigte gute vorhergesagte Löslichkeit und wurde, wichtig für Hirntumoren, als fähig eingestuft, die Blut‑Hirn‑Schranke zu überwinden, während es zugleich als verhältnismäßig sicher galt. Ein separates Toxizitäts‑Tool deutete an, dass Verbindung 21 abgesehen von möglichen Problemen bei sehr hohen oralen Dosen weniger wahrscheinlich Haut‑ oder Augenreizungen verursacht oder schwere akute Schäden auslöst als viele andere Kandidaten. Eine weitere Rechenreihe untersuchte die Elektronenverteilung im Molekül, was Hinweise auf seine chemische Stabilität und die Neigung zu unerwünschten Nebenreaktionen gibt; auch hier schnitt Verbindung 21 besser ab als das ursprüngliche Referenzmedikament.
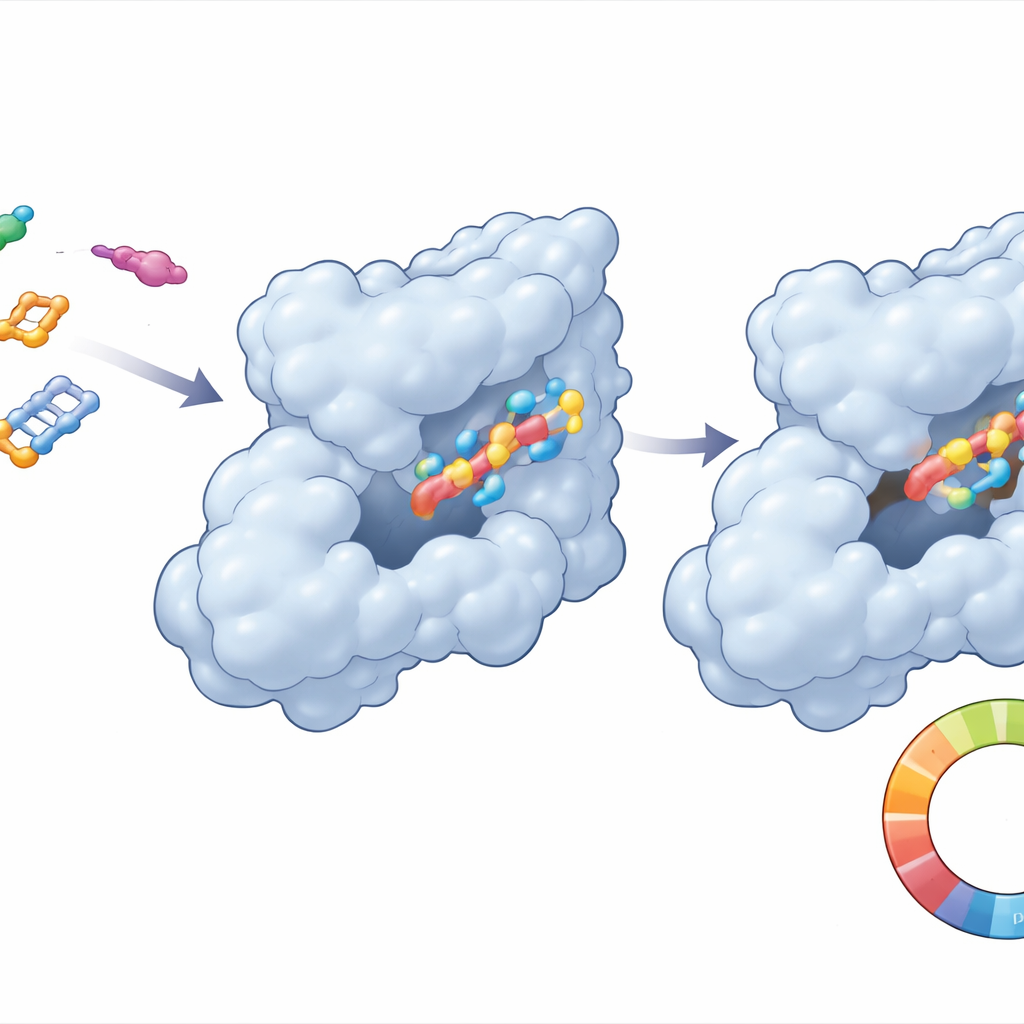
Beobachten, wie Wirkstoff und Ziel zusammen bewegen
Da Proteine und Wirkstoffmoleküle nicht starr sind, führten die Forschenden lange Computer‑"Filme" über 250 Milliardstel Sekunden durch, um zu sehen, wie CDK6 und jedes Molekül in einer wässrigen, körpereigenen Umgebung tatsächlich reagieren. Für Verbindung 21 stellte sich das Komplex schnell in eine stabile Anordnung und schwankte nur mäßig — ein gutes Zeichen dafür, dass das Molekül in der CDK6‑Tasche verankert bleibt. Wichtige Kontaktstellen zwischen Wirkstoff und Protein blieben erhalten, während die Gesamtform von CDK6 kompakt blieb. Im Gegensatz dazu zeigte das Referenzmolekül größere Fluktuationen und schwächere, weniger konstante Kontakte. Zusätzliche Energieberechnungen stützten die Auffassung, dass CDK6 bevorzugt Verbindung 21 stärker bindet, hauptsächlich durch enge hydrophobe (ölähnliche) Wechselwirkungen und gut positionierte Wasserstoffbrücken.
Was das für die künftige Behandlung von Hirntumoren bedeuten könnte
Zusammen ergeben diese computerbasierten Tests eine starke Argumentation, dass Verbindung 21 ein hochwertiger Ausgangspunkt für ein neues Glioblastom‑Medikament mit Ziel CDK6 ist. Sie wirkt selektiver, stabiler und besser geeignet, das Gehirn zu erreichen, als das Referenzmolekül, und umgeht viele gängige Toxizitätsfallen. Die Arbeit befindet sich jedoch noch auf einer Vorhersagestufe: In dieser Studie wurden keine Zellen oder Tiere behandelt. Die nächsten Schritte sind die Synthese von Verbindung 21, die Überprüfung, ob sie im Labor tatsächlich das Wachstum von Glioblastomzellen verlangsamt, und Tests in Tiermodellen. Bestätigen diese Studien die Simulationen, könnte dieses Molekül — oder verbesserte Versionen davon — letztlich zu präziseren, zielgerichteten Therapien beitragen, die Glioblastom‑Patientinnen und ‑Patienten bessere Aussichten und länger anhaltende Krankheitskontrolle bieten.
Zitation: Khan, M.U., Munir, M., Manzoor, H. et al. Molecular docking and dynamics reveal novel CDK6 inhibitors for targeted glioblastoma therapy. Sci Rep 16, 9000 (2026). https://doi.org/10.1038/s41598-026-39629-7
Schlüsselwörter: Glioblastom, CDK6‑Inhibitoren, zielgerichtete Therapie, virtuelles Wirkstoff‑Screening, Gehirntumor