Clear Sky Science · de
Ein multimodales Zebrafisch-Werkzeugkasten zur Untersuchung der Blut-Hirn-Schranke in Gesundheit und Krankheit
Warum undichte Hirngefäße wichtig sind
Wenn Blutgefäße im Gehirn oder Auge zu lecken beginnen, sickern Flüssigkeit und Proteine in das umliegende Nervengewebe und verursachen Schwellungen, die das Sehen trüben oder das Denken beeinträchtigen können. Diese Art der "Wasseransammlung" – als vasogenes Ödem bezeichnet – spielt eine Rolle bei diabetischer Sehverschlechterung, Schlaganfall, Hirnverletzungen und bestimmten Formen von Demenz. Dennoch fehlen Wissenschaftlern einfache, kostengünstige Methoden, um diesen Schutzwall in Echtzeit beim Versagen zu beobachten. Diese Studie stellt ein vielseitiges Zebrafisch-Modell vor, mit dem Forscher sehen, messen und untersuchen können, wie hoher Blutzucker die Gefäßbarriere des Gehirns schwächt und damit die Suche nach neuen Behandlungen beschleunigen könnte.
Ein winziger Fisch mit klarem Vorteil
Zebrafisch-Larven bieten ein einzigartiges Fenster in das lebende Gehirn. Im Gegensatz zu Säugetieren sind ihre Körper in frühen Lebensstadien transparent, und ihre Hirngefäße können unter dem Mikroskop zum Leuchten gebracht werden. Die Autorinnen und Autoren nutzten dies, indem sie sich auf die Blut–Hirn-Schranke konzentrierten, die enge Abdichtung zwischen Blut und Gehirngewebe, die der inneren Blut-Retina-Schranke ähnelt, die unsere Augen schützt. Da dieselben Zelltypen und viele der gleichen Schutzproteine zwischen Gehirn und Netzhaut geteilt werden, nutzte das Team die Hirnbarriere der Zebrafische als Stellvertreter, um Erkrankungen wie diabetisches Makulaödem und andere neurovaskuläre Störungen zu untersuchen — schneller, ethischer und kostengünstiger als traditionelle Nagetiermodelle.
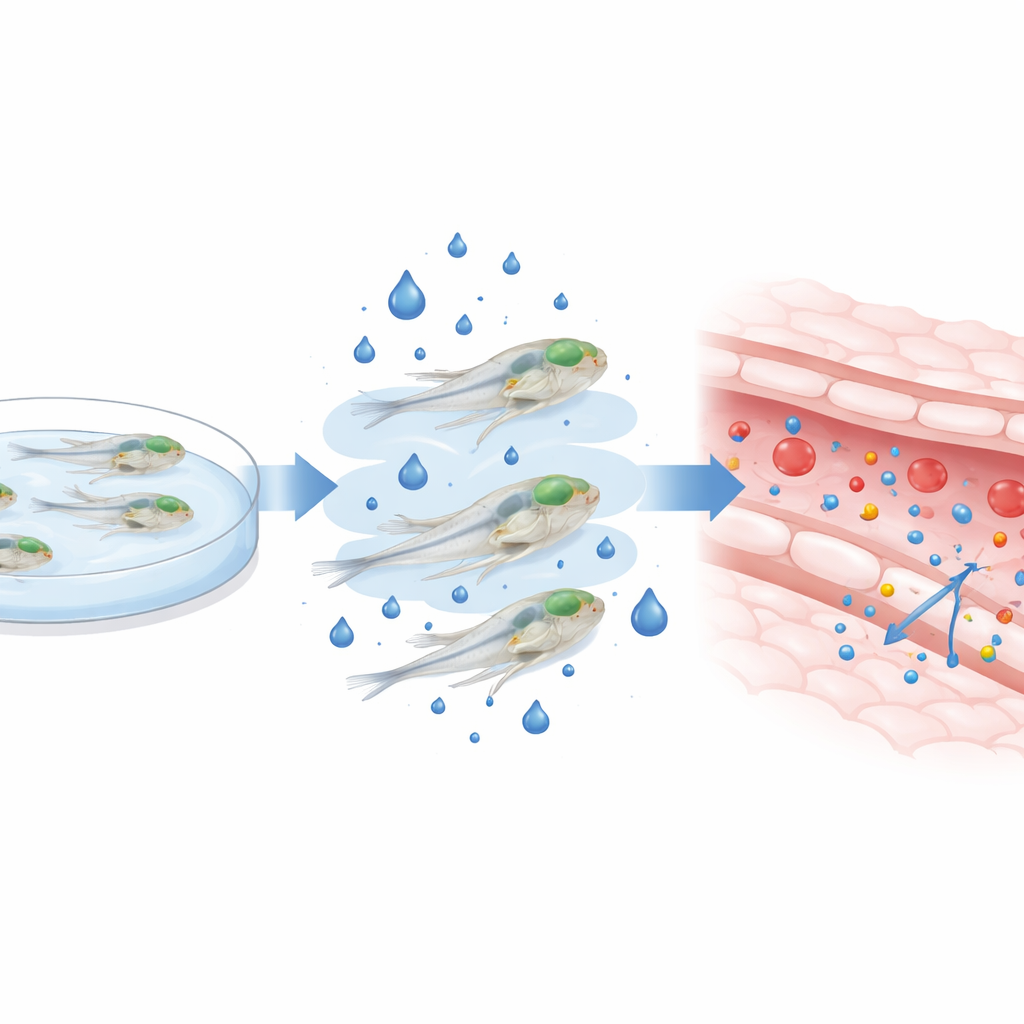
Erhöhung des Blutzuckers bei jungen Zebrafischen
Um den bei Diabetes beobachteten hohen Blutzucker nachzuahmen, hielten die Forschenden Zebrafisch-Larven zwischen dem dritten und fünften Tag nach der Befruchtung in Wasser mit zusätzlichem Glukosegehalt — einem kritischen Zeitfenster, in dem die Hirnbarriere noch reift. Sie bestätigten, dass dieses äußere Zuckergemisch die inneren Glukosespiegel mehrmals erhöhte, ohne die Larven zu töten oder ihre Gesamtgestalt zu verändern. Solange die Fische noch lebten und schwammen, injizierten sie fluoreszierende Farbstoffe unterschiedlicher Größe in den Kreislauf und verfolgten mit hochauflösenden Konfokalmikroskopen, wie viel Farbstoff aus den Hirngefäßen in das umliegende Gewebe sickerte. Nach zwei Tagen hoher Glukoseexposition traten sowohl bei kleinen als auch bei großen Farbstoffmolekülen verstärkte Austritte in das Gehirn auf, insbesondere bei der höheren Zuckerdosis, was darauf hindeutet, dass die Barriere durchlässiger geworden war.
Was mit der Gefäßwand passiert
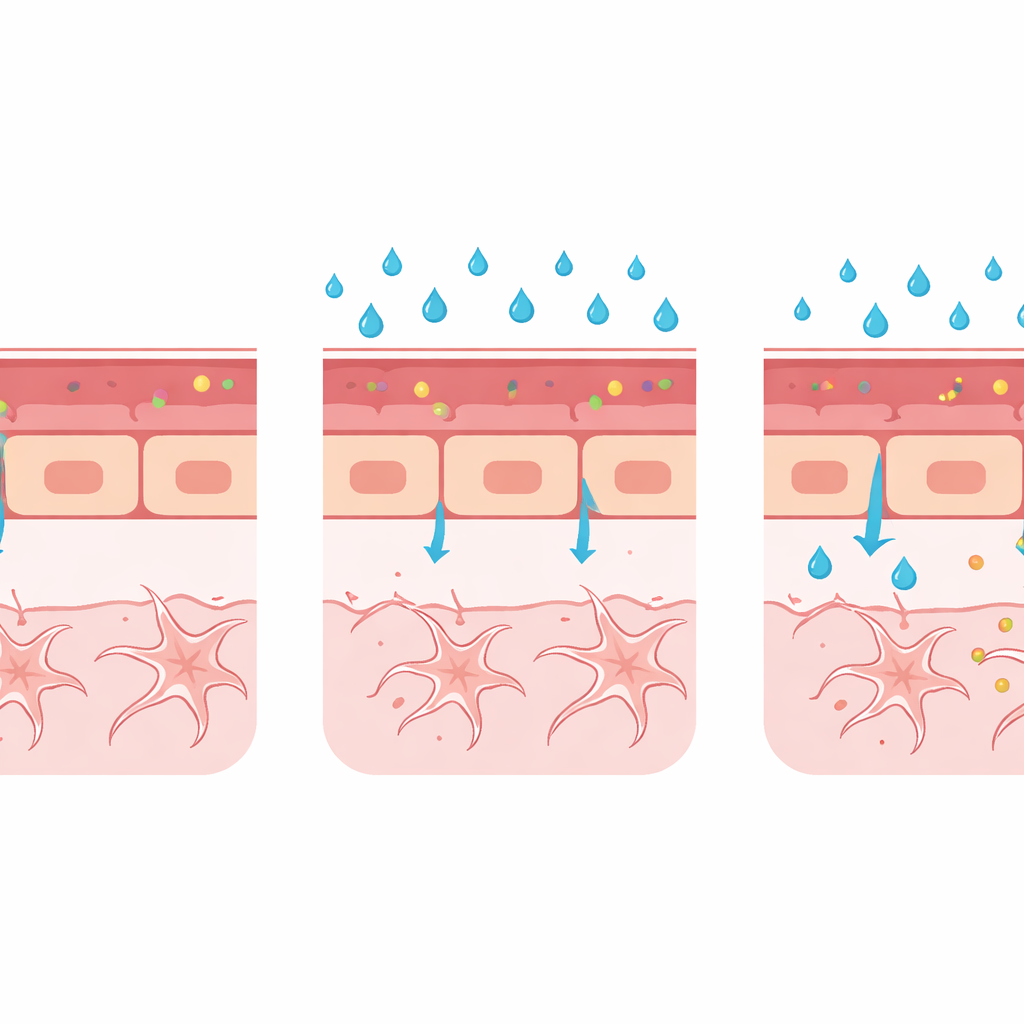
Über die reine Messung von Leckagen hinaus entwickelte das Team einen multimodalen "Werkzeugkasten", um zu untersuchen, was in der Gefäßwand selbst schieflief. Sie maßen den Durchmesser einer wichtigen Hirnarterie und stellten fest, dass hoher Glukosespiegel das Gefäß erweiterte — eine frühe Veränderung, die auch bei Menschen mit diabetischen Augenerkrankungen beobachtet wird. Mit Zebrafischen, die so gezüchtet wurden, dass bestimmte Proteine aufleuchten, zeigten sie, dass hoher Glukosespiegel die Menge von Claudin-5 verringerte, einem Hauptbestandteil der engen Verbindungen zwischen benachbarten Gefäßzellen, und die Level von PLVAP erhöhte, einem Protein, das mit unreifen, ausbruchsfähigen Gefäßen assoziiert ist und Material über die Zellschicht transportiert. Die Elektronenmikroskopie, die Strukturen im Nanometerbereich sichtbar macht, bestätigte subtile Erweiterungen an den Zellverbindungen, obwohl die winzigen Transporttaschen, sogenannte Caveolae, in diesem ersten Durchgang zu selten waren, um sie zuverlässig zu quantifizieren.
Eine flexible Plattform für künftige Krankheitsforschung
Zusammengefasst zeichnen diese Veränderungen — mehr Farbstoffleckage, erweiterte Gefäße, schwächere Zellverbindungen und erhöhtes PLVAP — ein konsistentes Bild: Hoher Blutzucker kann die richtige Ausbildung der Barriere im sich entwickelnden Gehirn verzögern oder stören. Das Modell bildet noch nicht den Zusammenbruch einer voll ausgereiften Barriere ab, wie er bei chronischen menschlichen Erkrankungen auftritt, eignet sich jedoch hervorragend, um zu zeigen, wie schädliche Bedingungen während der Entwicklung verhindern können, dass die Barriere jemals richtig abdichtet. Da die Techniken mit einer Reihe fluoreszenter Reporter-Linien und fortgeschrittener Bildgebung kompatibel sind, kann dieselbe Plattform erweitert werden, um andere Auslöser für Barriereschäden zu untersuchen, wie entzündliche Moleküle, veränderte Stützzellen wie Perizyten und Gliazellen oder Störungen in wichtigen Signalwegen.
Was das für Patienten bedeutet
Für Nichtfachleute ist die Kernbotschaft, dass diese Arbeit ein praktisches, lebendes Testfeld liefert, um zu beobachten, wie die Schutzwand des Gehirns unter Stress versagt — und das mit winzigen transparenten Fischen statt größeren Säugetieren. Indem Forscher in Echtzeit verfolgen, wie hoher Blutzucker Gefäßstruktur und -funktion verändert, können sie schneller herausfinden, welche Moleküle und Zelltypen es zu adressieren gilt, um die Barriere intakt zu halten. Letztlich könnten solche Erkenntnisse die Entwicklung neuer Medikamente oder Behandlungsstrategien leiten, um Flüssigkeitsaustritte in Auge und Gehirn zu verhindern oder zu verringern — was dazu beitragen würde, das Sehvermögen zu bewahren und die kognitive Funktion bei Menschen mit Diabetes und anderen neurovaskulären Erkrankungen zu schützen.
Zitation: Bakker-van Bugnum, N., Snijders, E.E., Hogendorp, E.F. et al. A zebrafish multimodal toolbox to study the blood-brain barrier in health and disease. Sci Rep 16, 9422 (2026). https://doi.org/10.1038/s41598-026-39616-y
Schlüsselwörter: Blut-Hirn-Schranke, Zebrafisch-Modell, diabetische Komplikationen, gefäßbedingte Leckage, neurovaskuläre Erkrankung