Clear Sky Science · de
Integratives Profiling von Transkriptom und H3K27ac-Modifikation zeigt Veränderungen im Zusammenhang mit BCG‑induziertem trainierten Immunsystem in bovinen Immunzellen
Warum das Training des Immunsystems wichtig ist
Impfstoffe werden normalerweise entwickelt, um den Körper auf einen bestimmten Erreger vorzubereiten. In den letzten zehn Jahren haben Forschende jedoch entdeckt, dass einige Impfstoffe dem Immunsystem auch eine allgemeinere Leistungssteigerung verleihen können, sodass es schneller und stärker auf verschiedene Bedrohungen reagiert. Diese Studie untersucht, wie der seit Langem verwendete Tuberkuloseimpfstoff BCG die vordersten Abwehrzellen junger Rinder umgestaltet und liefert Hinweise, die die Tiergesundheit verbessern, die Entwicklung von Humanimpfstoffen informieren und unser Verständnis der „angeborenen Immunerinnerung“ vertiefen könnten.
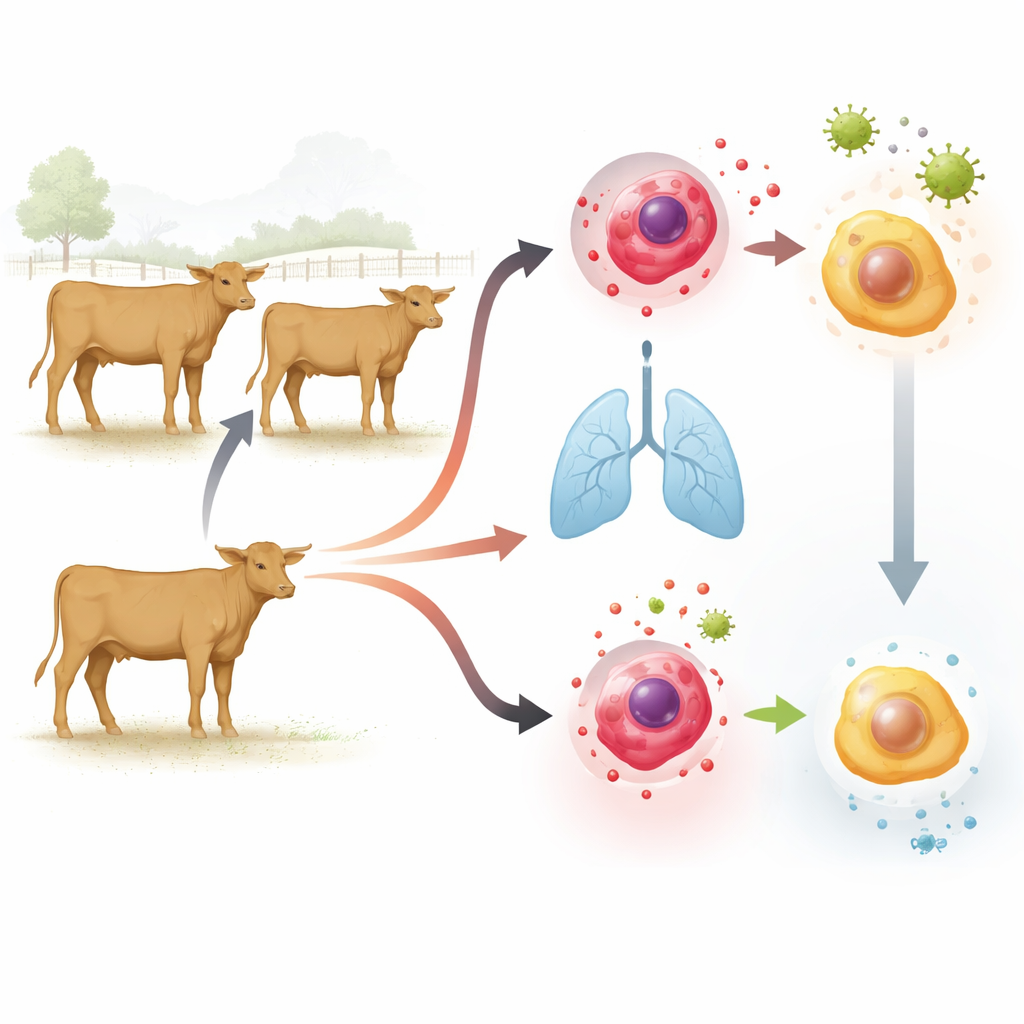
Ein klassischer Impfstoff mit breiterer Wirkung
BCG wird seit einem Jahrhundert zur Vorbeugung von Tuberkulose beim Menschen eingesetzt und auch Rindern zur Verhinderung der bovinen TB verabreicht. Überraschenderweise zeigen geimpfte Kinder häufig geringere Sterblichkeitsraten durch Infektionen, die nichts mit Tuberkulose zu tun haben. Das weckte die Idee, dass BCG angeborene Immunzellen „trainieren“ könnte — jene schnell reagierenden Zellen, die innerhalb von Stunden statt Tagen aktiv werden. In früheren Arbeiten zeigten die Autorinnen und Autoren, dass Kälber, die BCG erhielten, nachfolgenden Herausforderungen mehr entzündliche Botenstoffe, sogenannte Zytokine, produzierten. In der vorliegenden Studie stellten sie eine tiefergehende Frage: Was ändert sich innerhalb dieser Zellen, sodass sie Wochen nach der Impfung anders reagieren?
Wie das Team Immunerinnerung bei Kälbern testete
Die Forschenden arbeiteten mit zwanzig jungen Holstein–Angus‑Färsen. Die Hälfte erhielt zwei subkutane BCG‑Gaben im Abstand von zwei Wochen; die andere Hälfte erhielt als Kontrolle Kochsalzlösung. Einige Wochen später sammelte das Team zwei Zelltypen: im Blut zirkulierende Monozyten und in den Lungenbläschen lebende Makrophagen. Im Labor setzten sie diese Zellen verschiedenen Alarmreizen aus, die virale und bakterielle Eindringlinge nachahmen, und maßen, wie viel IL‑1β und IL‑6 — zwei zentrale entzündliche Zytokine — die Zellen produzierten. Zusätzlich nutzten sie Next‑Generation‑Sequencing, um zu protokollieren, welche Gene an- oder abgeschaltet wurden, und kartierten chemische Markierungen auf DNA‑verpackenden Proteinen (Histonen), die die Genaktivität steuern.
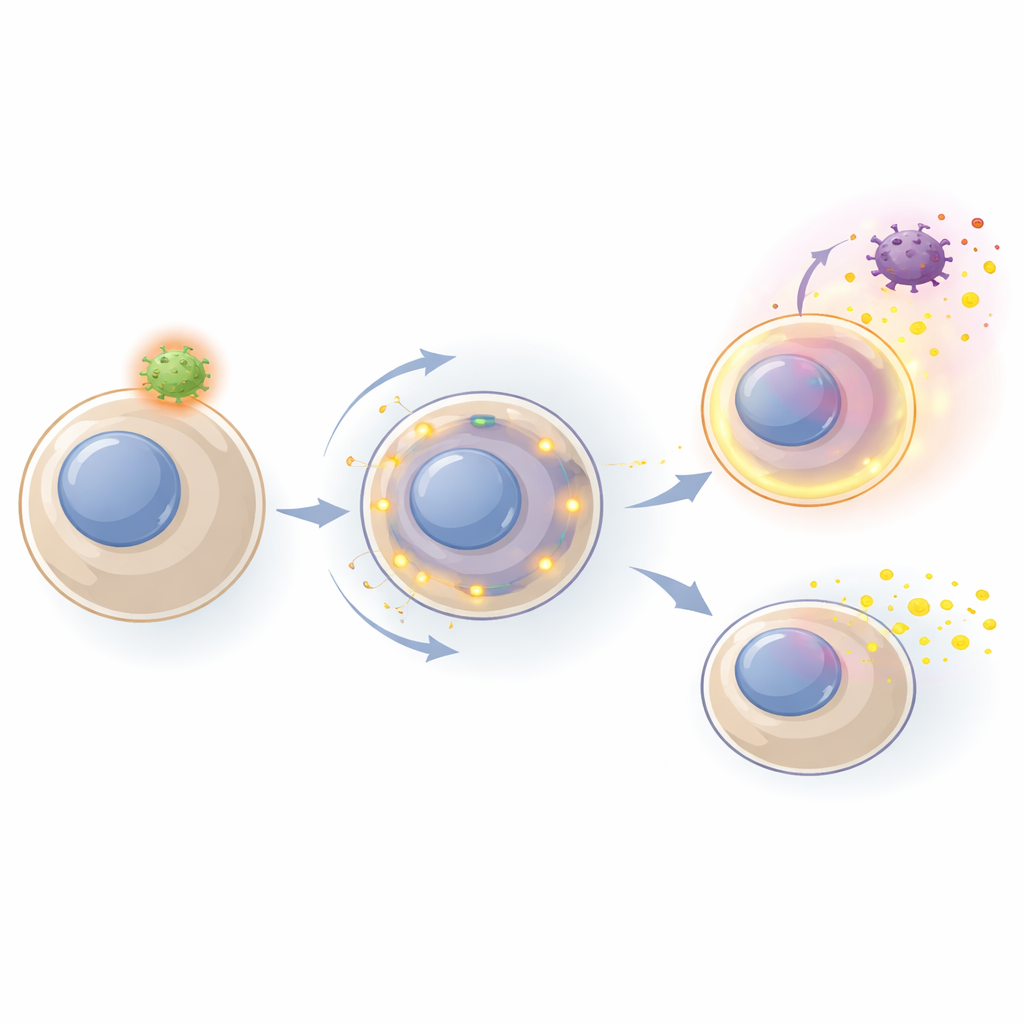
Stärkere Signale aus trainierten Frontzellen
Monozyten von BCG‑geimpften Kälbern verhielten sich deutlich anders. Bei Stimulation sezernierten sie mehr IL‑1β und IL‑6 als Monozyten aus ungeimpften Tieren, besonders als Reaktion auf ein synthetisches, viral ähnliches Signal. Auf Genebene schalteten diese Monozyten nach einer erneuten Stimulation eine breitere Reihe von Genen ein und zeigten eine stärkere Aktivierung von Signalwegen, die mit angeborener Immunität und antimikrobieller Abwehr verknüpft sind. Die gesteigerte Reaktion bedeutete nicht, dass Gene völlig neu von „aus“ zu „an“ wechselten; vielmehr verstärkte sie vorhandene Muster, wobei viele der gleichen Gene reagierten, aber in stärkerem Ausmaß. In der Lunge zeigten die residenten Makrophagen einen moderateren Trainingseffekt — insbesondere eine erhöhte IL‑1β‑Produktion als Antwort auf ein bakterielles Signal — was deutlich macht, dass verschiedene Gewebe unterschiedlich stark trainiert werden können.
Verborgene Markierungen, die Erfahrungen bewahren
Um aufzudecken, wie Zellen die frühere BCG‑Exposition „erinnerten“, untersuchten die Wissenschaftlerinnen und Wissenschaftler eine spezifische Histonmarkierung namens H3K27ac, die mit aktiven Schaltern im Genom assoziiert ist. Wochen nach der Impfung fanden sie Hunderte von Regionen in der DNA von Monozyten und Lungenmakrophagen, in denen diese Markierung bei BCG‑behandelten Tieren im Vergleich zu Kontrollen verändert war. In Monozyten lagen viele dieser Veränderungen in der Nähe von Genen, die an Immunregulation und Zytokinsteuerung beteiligt sind, was darauf hindeutet, dass BCG dauerhafte chemische Spuren hinterlässt, die bestimmte Gene später leichter aktivierbar machen. Einige der veränderten Regionen überschneiden sich mit Stellen, die in Studien am Menschen identifiziert wurden, was darauf hindeutet, dass Teile dieses Trainingsprogramms zwischen Arten geteilt werden, während viele andere Regionen rindspezifisch erscheinen.
Was das für Tier- und Humanmedizin bedeutet
Insgesamt zeigen die Ergebnisse, dass eine Standard‑BCG‑Impfung die frühzeitigen Immunabwehrkräfte von Rindern umgestalten kann: Ihre Monozyten und Lungenmakrophagen werden fähiger, bei Begegnung mit neuen Bedrohungen starke Entzündungsreaktionen auszulösen. Diese Verschiebung hängt nicht nur mit dem zusammen, was die Zellen tun — mehr Zytokine freisetzen und mehr Gene aktivieren — sondern auch mit der Art, wie ihr genetisches Material verpackt und markiert ist. Für eine nichtfachliche Leserschaft ist die Kernidee, dass angeborene Immunzellen nicht so „vergesslich“ sind, wie man einst annahm. Stattdessen können sie eine biochemische Erinnerung an frühere Herausforderungen tragen, die ihnen hilft, beim nächsten Mal stärker zu reagieren. Das Verständnis und die Nutzbarmachung dieser Form des trainierten Immunsystems könnten zu intelligenteren Impfstrategien und robusteren Nutztieren führen und sogar neue Ansätze zur Stärkung der menschlichen Resilienz gegenüber einer breiten Palette von Infektionen inspirieren.
Zitation: Samuel, B.E.R., Yang, P., Tuggle, C.K. et al. Integrative profiling of transcriptome and H3K27ac modification reveals changes associated with BCG-induced trained immunity in bovine immune cells. Sci Rep 16, 8216 (2026). https://doi.org/10.1038/s41598-026-39580-7
Schlüsselwörter: trainiertes Immunsystem, BCG‑Impfstoff, Rindergesundheit, angeborene Immunzellen, epigenetische Veränderungen