Clear Sky Science · de
Validierter umfassender RP-HPLC-Ansatz zur Trennung und Quantifizierung von Solifenacin und Mirabegron in Anwesenheit ihrer Abbauprodukte
Warum sorgfältige Prüfung von Blasenmedikamenten wichtig ist
Millionen von Menschen mit überaktiver Blase sind auf zwei moderne Arzneimittel angewiesen, Solifenacin und Mirabegron, um plötzliche Harndranggefühle und häufige Toilettengänge zu reduzieren. Aber wie alle Medikamente können diese Tabletten winzige Mengen unerwünschter Nebenprodukte enthalten, die während der Herstellung, bei der Lagerung oder sogar im Körper entstehen. Die Studie hinter diesem Artikel konzentriert sich auf die Entwicklung eines schnellen, zuverlässigen Labortests, um diese Spuren von Verunreinigungen und Abbauprodukten zu erkennen und zu quantifizieren, und so die Wirksamkeit und Sicherheit der Medikamente zu unterstützen.
Zwei Arzneimittel, die eine überaktive Blase beruhigen
Solifenacin und Mirabegron lindern Blasensymptome auf unterschiedliche, sich aber ergänzende Weise. Solifenacin wirkt, indem es Signale blockiert, die den Blasenmuskel zur Kontraktion veranlassen, wodurch Krämpfe nachlassen und das Fassungsvermögen der Blase steigt. Mirabegron greift an einem anderen Rezeptor an und entspannt die Blasenwand sanft, was ebenfalls die Speicherung erhöht, jedoch ohne einige der typischen Nebenwirkungen wie Mundtrockenheit und Verstopfung. Da diese Wirkstoffe weit verbreitet verschrieben und oft gemeinsam in einer Tablette verwendet werden, sind Aufsichtsbehörden und Hersteller besonders wachsam gegenüber zusätzlichen Substanzen, die zusammen mit den Wirkstoffen eingeschleppt werden könnten.
Verborgene Mitreisende in einer Tablette
Unerwünschte Moleküle können entstehen, wenn ein Wirkstoff erstmals synthetisiert wird, wenn er gelagert wird oder wenn er Hitze, Licht oder reaktiven Chemikalien ausgesetzt ist. Bei Solifenacin können mehrere bekannte „offizielle" Verunreinigungen gebildet werden, von denen einige in frühen Studien mit erhöhter Toxizität oder abgeschwächter Wirksamkeit in Verbindung gebracht wurden. Mirabegron kann ebenfalls in verwandte Moleküle zerfallen, einschließlich eines Metaboliten, der nach Einnahme im menschlichen Körper auftritt. Obwohl diese Substanzen in sehr geringen Mengen vorkommen, können sie dennoch das Verhalten des Arzneimittels verändern oder neue Risiken einführen. Internationale Richtlinien verlangen daher empfindliche Methoden, die sowohl die Hauptwirkstoffe als auch ihre Nebenprodukte in einem einzigen Lauf trennen und quantifizieren können.
Ein anspruchsvoller Filter für komplexe Gemische
Die Forschenden bauten ihren Ansatz um die Hochleistungsflüssigkeitschromatographie auf, eine bewährte Technik, bei der eine flüssige Probe durch eine spezielle Säule gepresst wird, die mit feinen Partikeln gefüllt ist. Unterschiedliche Moleküle passieren dieses Packbett mit unterschiedlicher Geschwindigkeit, sodass sie zu verschiedenen Zeiten austreten und einzeln gemessen werden können. In dieser Studie optimierte das Team jeden Teil der Ausstattung: Sie wählten eine kompakte Säule, passten das Mischungsverhältnis aus Wasser, organischem Lösungsmittel und einer kleinen Menge Säure an, setzten die Fließgeschwindigkeit fest und wählten eine Lichtwellenlänge, bei der sowohl die Wirkstoffe als auch die meisten Verunreinigungen stark absorbieren. Das Ergebnis war ein kompakter Test, der Solifenacin, Mirabegron, zwei der wichtigsten Verunreinigungen von Solifenacin und einen bedeutenden Mirabegron-Metaboliten in knapp zehneinhalb Minuten sauber trennen konnte.
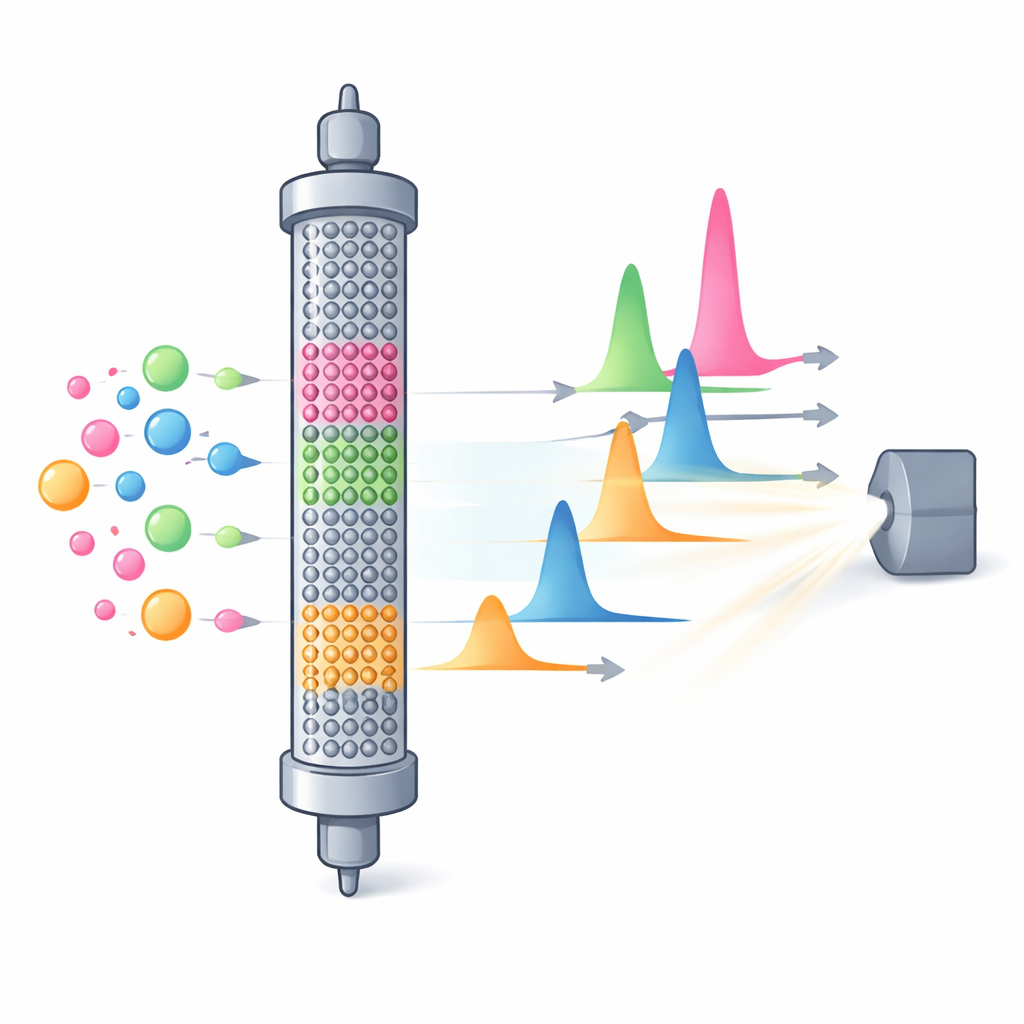
Den Test einem Härtetest unterziehen
Um sicherzustellen, dass ihr Test unter realen Bedingungen funktioniert, setzten die Wissenschaftler die reinen Wirkstoffe gezielt sauren, basischen, oxidierenden, heißen und lichtexponierten Bedingungen aus, um wahrscheinliche Abbauprodukte zu erzeugen. Anschließend nutzten sie ihr chromatographisches System zusammen mit Infrarot- und massenbasierten Messungen, um nachzuvollziehen, welche neuen Moleküle auftraten und deren Identitäten zu bestätigen. Danach prüften sie, dass die Methode über einen weiten Konzentrationsbereich genau ist, bei wiederholten Messungen an verschiedenen Tagen nahezu identische Ergebnisse liefert und selbst Spurenmengen von Verunreinigungen deutlich unterhalb regulatorischer Grenzwerte nachweisen kann. Schließlich wandten sie die Technik auf eine tatsächliche Kombinations-tablette mit beiden Wirkstoffen an und zeigten, dass übliche Tablettenhilfsstoffe die Messungen nicht beeinträchtigen.
Was das für Patienten und Hersteller bedeutet
Kurz gesagt liefert die Studie ein sensibles, zeitsparendes Labortool, das Solifenacin–Mirabegron-Produkte sowohl auf die beabsichtigten Wirkstoffe als auch auf eine Reihe wichtiger Abbauprodukte in einem Durchgang untersuchen kann. Durch die klare Trennung und Quantifizierung dieser Komponenten hilft die Methode Herstellern zu überprüfen, dass jede Chargen von Tabletten die Qualitätsstandards erfüllt und über die Zeit stabil bleibt. Für Patientinnen und Patienten stärkt diese Art von Test im Hintergrund das Vertrauen, dass die eingenommenen Pillen gegen überaktive Blase das enthalten, was sie sollen — und nur winzige, kontrollierte Mengen von dem, was sie nicht sollen.
Zitation: Kamel, E.B., Badrawy, M. & Nour, I.M. Validated comprehensive RP HPLC approach for separation and quantification of solifenacin and mirabegron in the presence of their degradation products. Sci Rep 16, 9341 (2026). https://doi.org/10.1038/s41598-026-39569-2
Schlüsselwörter: überaktive Blase, Arzneimittelverunreinigungen, Hochleistungsflüssigkeitschromatographie, Solifenacin, Mirabegron