Clear Sky Science · de
Genomische und in vitro-Charakterisierung von zwei lytischen Bakteriophagen, die die multiresistente Erwinia-Sp. Stamm AnSW2-5 infizieren
Warum bakterienbedingte Pflanzenkrankheiten uns alle angehen
Weltweit kämpfen Landwirte gegen bakterielle Krankheiten, die Früchte verfaulen, Blätter einstutzen und Ernten vernichten. Viele dieser Ausbrüche werden inzwischen durch Stämme verursacht, die auf gängige Antibiotika nicht mehr ansprechen, wodurch sowohl die Nahrungsmittelversorgung als auch Existenzen bedroht sind. Diese Studie untersucht eine aufkommende Alternative: Viren, die Bakterien angreifen — sogenannte Bakteriophagen — um einen besonders hartnäckigen Pflanzenpathogen aus dem Boden zu beseitigen, das mit hoher Antibiotikaanwendung in Verbindung steht.
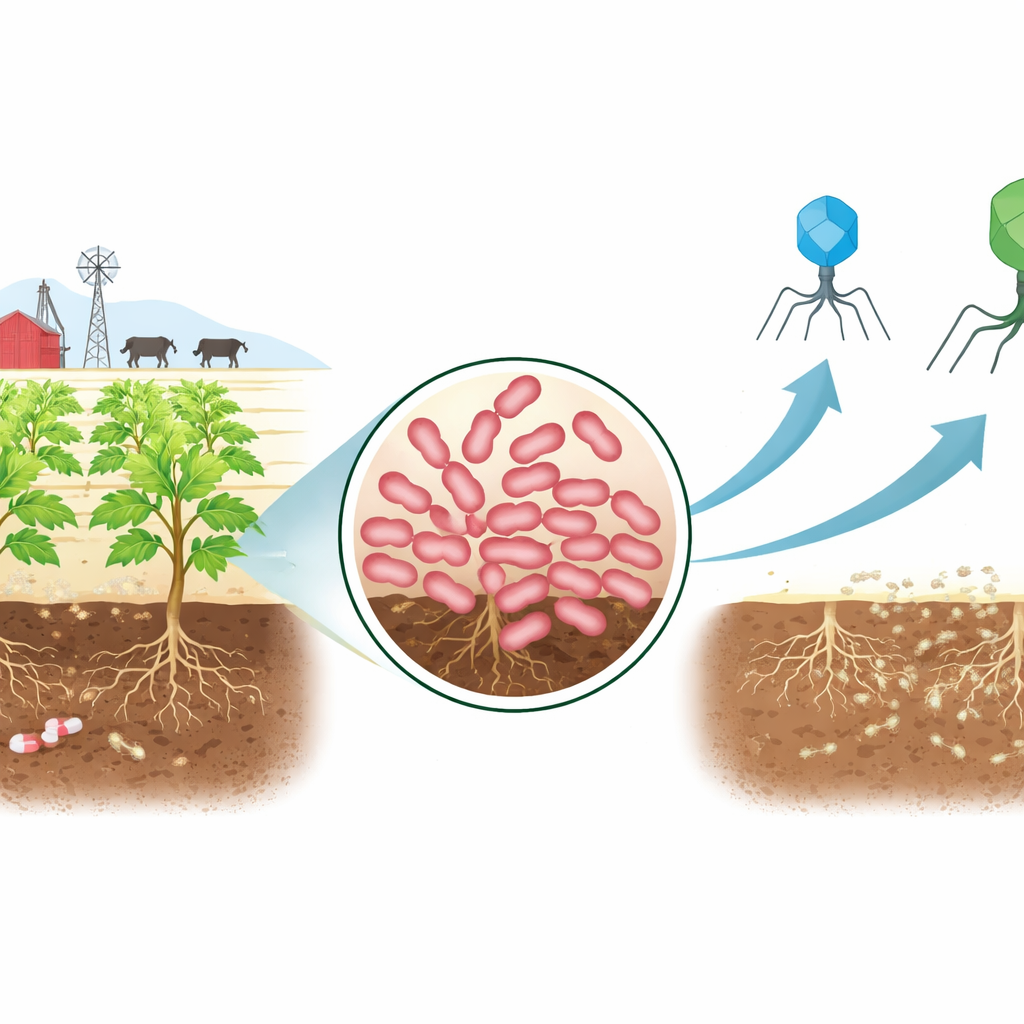
Ein neuer hartnäckiger Eindringling auf dem Hof
Die Forschenden begannen mit Bodenproben aus einem Viehstall, der bekannt dafür ist, Viehdung und Antibiotika zu erhalten. Aus dieser belasteten Umgebung isolierten sie einen Erwinia-Stamm, eine Bakteriengruppe, die berüchtigte Erreger wie den Feuerbrand bei Apfelbäumen und Weichfäule an Kartoffeln einschließt. Tests zeigten, dass dieser Stamm, AnSW2-5 genannt, gegenüber mehreren wichtigen Antibiotikaklassen resistent ist, darunter Wirkstoffe, die gegen ein breites Spektrum von Infektionen eingesetzt werden. Die genetische Analyse bestätigte die Ursache: Seine DNA trägt mehrere bekannte Resistenzgene und leistungsfähige molekulare Pumpen, die Antibiotika aus der Zelle entfernen. Gleichzeitig zeigten Genomvergleiche, dass sich dieser Stamm von zuvor beschriebenen Erwinia-Arten unterscheidet, was ihn zu einem nützlichen Modell macht, um zu untersuchen, wie neue, schwer behandelbare Pflanzenpathogene kontrolliert werden können.
Zwei winzige Räuber mit unterschiedlichen Stärken
Um natürliche Feinde dieses multiresistenten Bakteriums zu finden, nutzte das Team Süßwasser von derselben Stelle und reicherte es gezielt auf Bakteriophagen an, die AnSW2-5 infizieren konnten. Sie isolierten zwei vielversprechende Kandidaten, bezeichnet als P-A und P-K. Elektronenmikroskopisch erschien P-A kompakt mit kurzem Schwanz, ein Bau, der mit schneller, direkter Infektion verbunden ist. P-K hingegen hatte einen längeren, kontraktilen Schwanz mit komplexer Basenstruktur, was auf eine kraftvollere Eindringmethode in seinen Wirt hindeutet. Die Sequenzierung ihrer Genome zeigte, dass beide Phagen strikt lytisch sind: sie dringen ein, replizieren sich und sprengen die Zelle auf, anstatt sich leise im bakteriellen Genom zu integrieren. Doch sie tun dies mit sehr unterschiedlichen genetischen Werkzeugkästen — P-A’s schlankes Genom unterstützt einen schnellen Angriff, während P-K’s größeres Genom aufwändigere Struktur- und Replikationsmechanismen kodiert.
Wie das virale Tag-Team angreift
Als die Wissenschaftler den Lebenszyklus jedes Phagen im Labor verfolgten, stellten sie fest, dass P-A schnell zuschlägt: Es braucht nur etwa 20 Minuten, bis neue Viruspartikel erscheinen, und jede infizierte Bakterienzelle setzt rund 70 Nachkommen frei. P-K benötigt länger — etwa 35 Minuten, bevor es neue Phagen produziert — liefert dafür aber pro infizierter Zelle ungefähr 110 neue Partikel. In Ko-Kultur-Tests, bei denen Bakterien und Phagen über drei Tage zusammenwuchsen, verlangsamten beide Phagen allein das bakterielle Wachstum, verhinderten es jedoch nicht vollständig. Die Bakterien erholten sich schließlich, was dem Auftreten resistenter Überlebender entspricht. Wurden P-A und P-K jedoch in einem Cocktail kombiniert, reduzierten sie die Bakterienpopulation um mehr als 80 % und hielten sie während des gesamten 72-stündigen Experiments unterdrückt.
Resistenzbildung den Boden entziehen
Eines der auffälligsten Ergebnisse war, wie das Phagenpaar das Entstehen resistenter Mutanten beeinflusste. Bei Exposition gegenüber entweder P-A oder P-K allein schaffte es ein kleiner Bruchteil der Bakterien — ungefähr eins zu einer Million bis eins zu zehn Millionen —, der Phagenattacke zu entkommen und weiter zu wachsen. Wenn jedoch beide Phagen zusammen eingesetzt wurden, wurden resistente Kolonien so selten, dass sie unter die Nachweisgrenze des Experiments fielen. Das deutet darauf hin, dass die beiden Viren wahrscheinlich an unterschiedliche Ziele auf der bakteriellen Oberfläche binden oder die Zelle auf komplementäre Weise schädigen. Damit ein einzelnes Bakterium überlebt, müsste es beide Mechanismen gleichzeitig überwinden — ein verschwindend unwahrscheinliches Ereignis. Praktisch gesehen macht dies den Cocktail deutlich robuster gegen die evolutionären Tricks, die Antibiotika oft wirkungslos werden lassen.
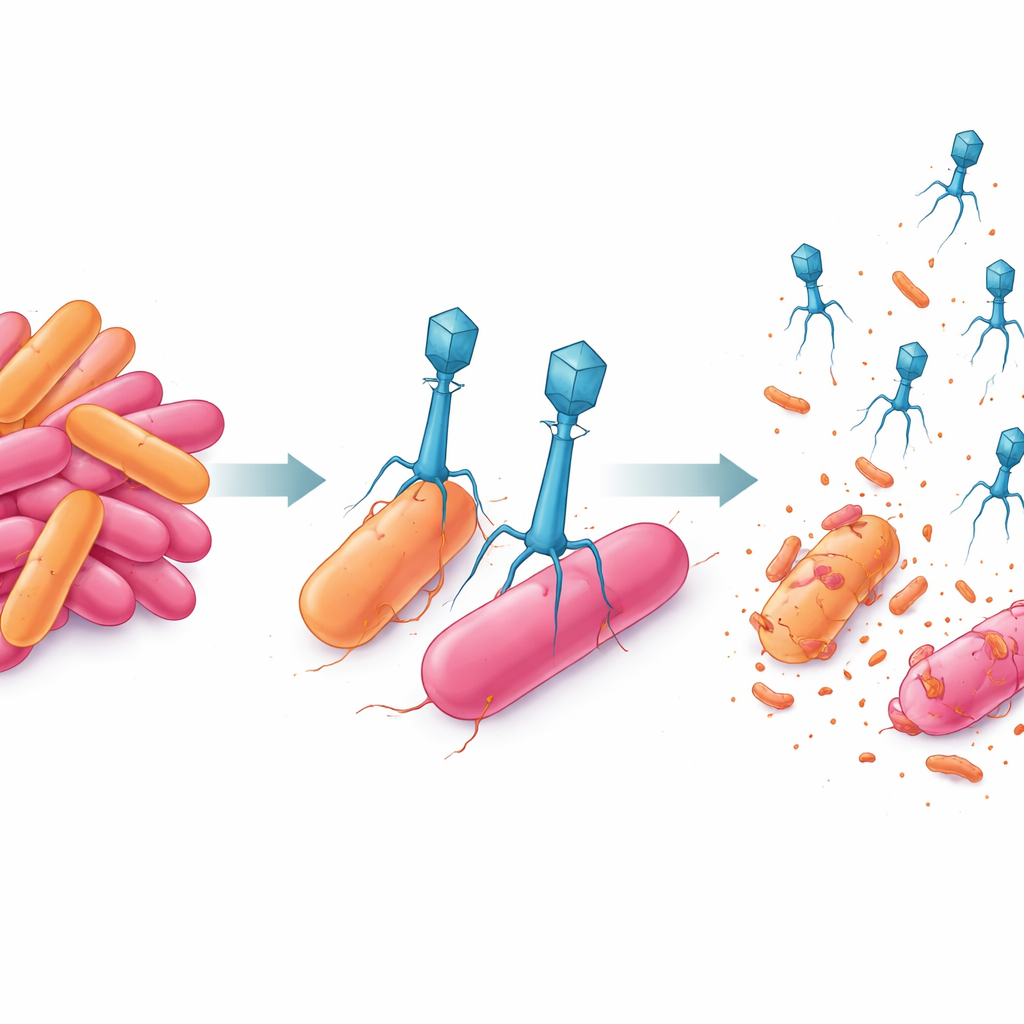
Welche Bedeutung das für künftige Ernten haben könnte
Insgesamt zeigt die Arbeit, dass sorgfältig ausgewählte Phagenpaare mehr leisten können als gefährliche Pflanzenbakterien zu reduzieren — sie können auch die Fähigkeit der Bakterien, Resistenzen zu entwickeln, stark einschränken. Durch die Kombination eines schnell wirkenden Phagen mit einem, der größere Nachkommenschaften produziert, schufen die Forschenden ein virales Tag-Team, das einen multiresistenten Erwinia-Stamm über Tage unter Kontrolle hielt und nachweisbare Fluchtvarianten verhinderte. Obwohl diese Versuche im Labor und nicht in Obstgärten oder auf Feldern durchgeführt wurden, weisen sie auf eine Zukunft hin, in der gezielte Phagenmischungen Teil des integrierten Schädlingsmanagements werden und Landwirten helfen, Pflanzen mit deutlich geringerem Einsatz traditioneller Antibiotika zu schützen.
Zitation: Baek, K., Goh, J. & Choi, A. Genomic and in vitro characterization of two lytic bacteriophages infecting multidrug-resistant Erwinia sp. strain AnSW2-5. Sci Rep 16, 8172 (2026). https://doi.org/10.1038/s41598-026-39563-8
Schlüsselwörter: Bakteriophagen-Biocontrol, Pflanzenbakterielle Krankheiten, Antibiotikaresistenz in der Landwirtschaft, Erwinia-Phagentherapie, Phagen-Kombinationen