Clear Sky Science · de
Neue Benzimidazol‑Alkanesulfonat‑Konjugate als Cholinesterase‑Hemmer mit in vitro‑ und in silico‑Validierung
Warum diese Forschung für Gedächtnis und Alterung wichtig ist
Die Alzheimer‑Krankheit zermürbt langsam das Gedächtnis, die Selbstständigkeit und die Lebensqualität von Millionen Menschen weltweit. Die heute verfügbaren Medikamente lindern meist nur die Symptome, ohne den zugrundeliegenden Schaden deutlich zu verlangsamen. Diese Studie untersucht eine neue Familie von synthetisch hergestellten Molekülen, die darauf ausgelegt sind, einen wichtigen Botenstoff im Gehirn, der für Lernen und Gedächtnis bedeutsam ist, besser zu schützen und gleichzeitig schädlichen oxidativen Stress zu bekämpfen. Indem Merkmale verschiedener erfolgreicher Wirkstofftypen in einer einzigen Struktur kombiniert werden, wollen die Forschenden einen Schritt näher zu wirksameren Behandlungen der Alzheimer‑Krankheit gelangen.
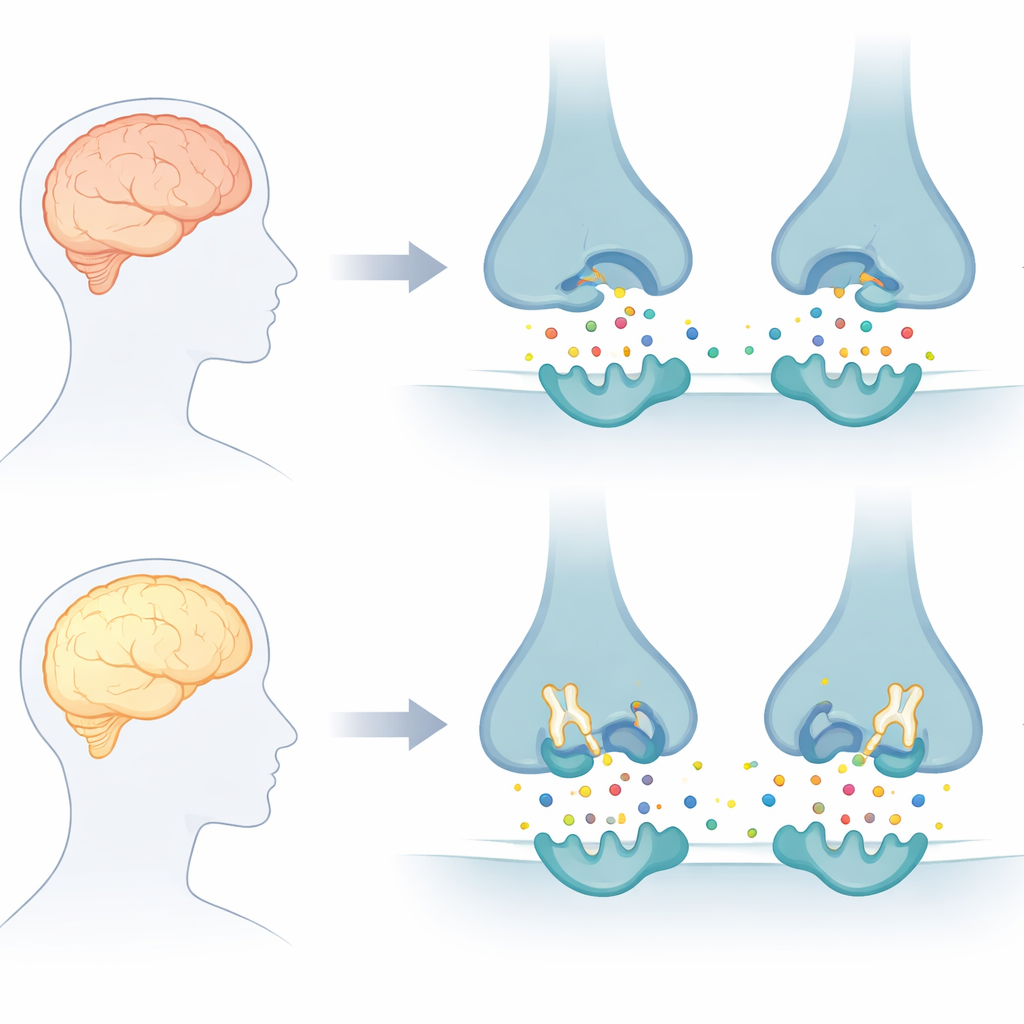
Das Hirnsignal, das zu schnell verblasst
Gesunde Nervenzellen kommunizieren über chemische Botenstoffe, von denen Acetylcholin zu den wichtigsten zählt. Bei Alzheimer wird Acetylcholin zu schnell durch zwei Enzyme abgebaut, die Acetylcholinesterase und die Butyrylcholinesterase, was zu Gedächtnisverlust und Verwirrung beiträgt. Aktuelle Medikamente blockieren meist nur eines dieser Enzyme und das nur zeitlich begrenzt, weshalb sie kurzzeitige Symptombesserung, aber keinen langfristigen Schutz bieten. Die Autorinnen und Autoren dieser Arbeit konzentrierten sich auf das Design sogenannter „Dual‑Inhibitoren“, die beide Enzyme gleichzeitig angreifen und Acetylcholin so bessere Chancen geben könnten, seine Funktion zu erfüllen.
Entwicklung eines intelligenteren molekularen Schlüssels
Um diese Dual‑Inhibitoren zu entwickeln, verwendete das Team eine Strategie namens molekulare Hybridisierung: Sie setzten Stücke aus drei Typen chemischer Bausteine zusammen, die bereits dafür bekannt sind, gut mit Cholinesterase‑Enzymen zu interagieren. Dazu gehören ein Benzimidazol‑Ring, wie er häufig in Arzneistoffen vorkommt, eine Sulfonatgruppe, die stark an Enzymtaschen binden kann, und ein Hydrazon‑Linker, der die Teile flexibel verbindet. Das Ergebnis war eine Serie verwandter Verbindungen, bezeichnet als 4a bis 4r, deren Strukturen mit standardmäßigen chemischen Methoden wie Infrarot‑ und Kernspinresonanzspektroskopie sorgfältig bestätigt wurden.
Testen der Enzymhemmung und der antioxidativen Wirkung
Die neuen Verbindungen wurden zunächst in Reagenzglasexperimenten auf ihre Fähigkeit geprüft, die beiden Cholinesterase‑Enzyme zu verlangsamen. Die meisten Mitglieder der Serie zeigten mäßige bis starke Hemmeffekte, wobei fünf Verbindungen – namentlich 4b, 4h, 4i, 4q und 4r – besonders durch ihre Hemmung der Acetylcholinesterase hervortraten. Bei der Bestimmung präziserer Wirksamkeitswerte erreichten mehrere dieser Moleküle die Leistung von Donepezil, einem der gegenwärtig eingesetzten Alzheimer‑Medikamente, oder übertrafen sie sogar. Das Team untersuchte zudem, ob die besten Enzymhemmer freie Radikale neutralisieren können, also instabile Moleküle, die Nervenzellen schädigen. Die Verbindungen 4q und 4r zeigten in mehreren Tests besonders starke antioxidative Aktivität und kamen der beziehungsweise übertrafen die Leistung des Referenzantioxidans Vitamin C.
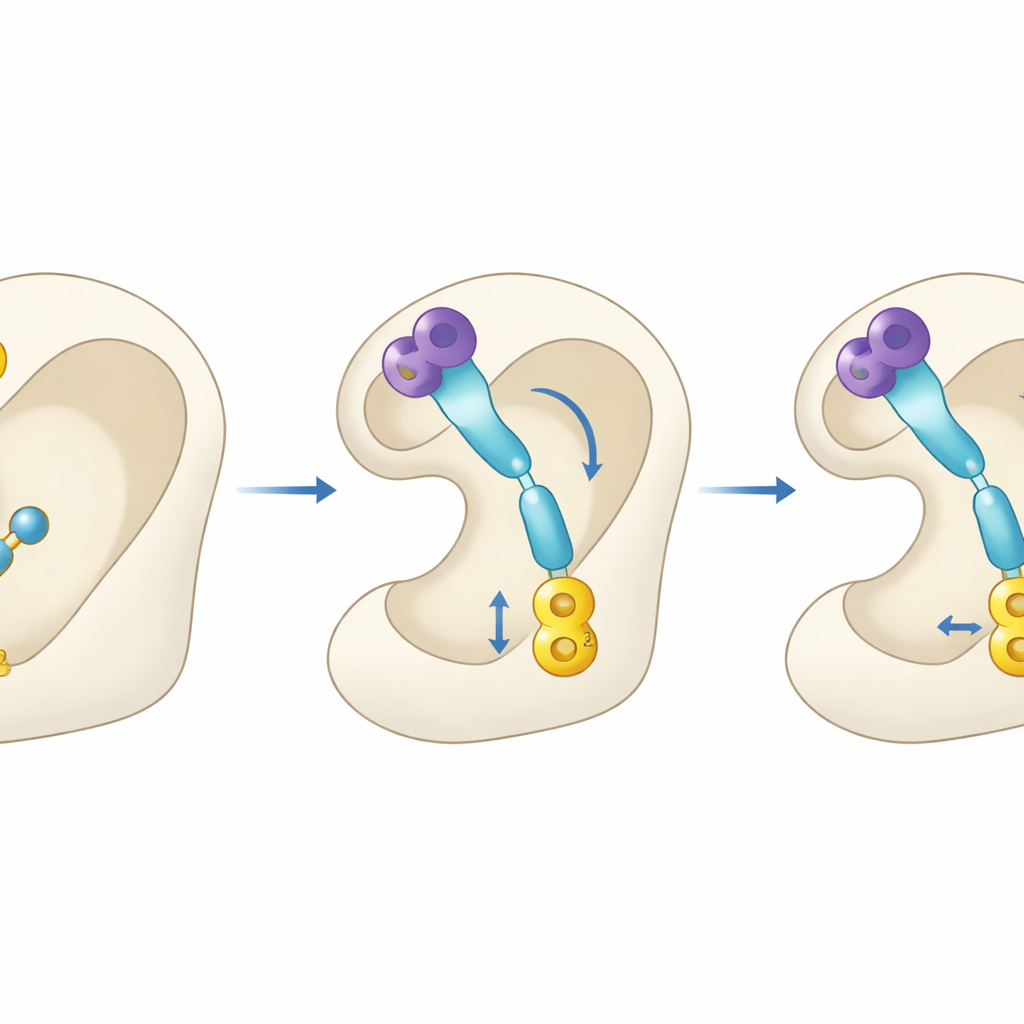
Ein Blick in das Enzym‑Schloss
Da diese Experimente außerhalb des Körpers durchgeführt wurden, griffen die Wissenschaftlerinnen und Wissenschaftler zu Computer‑Modellierungen, um vorherzusagen, wie sich die Moleküle als potenzielle Wirkstoffe verhalten könnten. Mit etablierten in silico‑Werkzeugen schätzten sie Absorptions‑, Verteilungs‑ und Stoffwechseleigenschaften und simulierten dann, wie die Verbindungen in die dreidimensionale Struktur der Acetylcholinesterase passen. Die Docking‑Studien legten nahe, dass sich der Benzimidazol‑Teil jedes Moleküls in der Nähe der äußeren Öffnung des Enzyms einlagert, während das sulfonattragende Ende tief ins katalytische Zentrum reicht, wo normalerweise Acetylcholin abgebaut wird. Bemerkenswert bildeten 4q und 4r mehrere stabilisierende Wechselwirkungen in der Enzymtasche und zeigten eine höhere berechnete Bindungsstärke als Donepezil selbst, was ihre starken Ergebnisse aus den Reagenzglassystemen widerspiegelt.
Was das für zukünftige Alzheimer‑Behandlungen bedeutet
In der Summe zeigen die Ergebnisse, dass diese neue Klasse von Benzimidazol‑Alkanesulfonat‑Konjugaten die Acetylcholinesterase stark hemmen, nützliche antioxidative Eigenschaften aufweisen und an ihr Enzymziel in einer Weise binden, die mit etablierten Prinzipien des Wirkstoffdesigns übereinstimmt. Zwar sind diese Moleküle noch weit davon entfernt, als Arzneimittel eingesetzt zu werden – sie wurden noch nicht in Tier‑ oder Humanstudien geprüft – doch liefern sie eine vielversprechende Blaupause für nächste Generationen von Alzheimer‑Therapeutika, die Enzymhemmung mit Schutz gegen oxidativen Stress kombinieren. Mit weiterer Optimierung und biologischer Prüfung könnten einige Vertreter dieser Familie eines Tages dazu beitragen, Gedächtnis und Denkvermögen im alternden Gehirn besser zu erhalten.
Zitation: Omar, M.A., Al-Ashmawy, A.A.K., Abd El Salam, H.A. et al. New benzimidazole-alkanesulfonate conjugates as cholinesterase inhibitors with in vitro and in silico validation. Sci Rep 16, 8946 (2026). https://doi.org/10.1038/s41598-026-39534-z
Schlüsselwörter: Alzheimer‑Krankheit, Acetylcholinesterase‑Hemmer, Benzimidazol‑Derivate, antioxidative Verbindungen, Wirkstoffdesign