Clear Sky Science · de
Proteomische Profilierung der bronchoalveolären Lavage nach segmentaler Endotoxin‑Provokation beim Menschen – ein mögliches Exazerbationsmodell
Warum eine kurze Phase der Lungenentzündung wichtig ist
Chronische Lungenerkrankungen wie die chronisch obstruktive Lungenerkrankung (COPD) verschlechtern sich häufig plötzlich, wenn die Atemwege akut entzündet sind, meist infolge von Infektionen. Diese Episoden, Exazerbationen genannt, führen viele Menschen ins Krankenhaus und können die Atmung dauerhaft verschlechtern. Sie direkt bei Patienten zu untersuchen ist schwierig und riskant. In dieser Studie wird eine kontrollierte, kurzzeitige Reizung der Lunge bei gesunden Freiwilligen eingesetzt, um einige Merkmale dieser Schübe nachzuahmen. Anschließend messen die Forschenden Hunderte von Proteinen in der Lungenflüssigkeit, um zu sehen, welche Signale aktiviert werden. Die Ergebnisse helfen, die Chemie der Lungenentzündung besser zu verstehen, und können die Suche nach neuen Therapien beschleunigen.
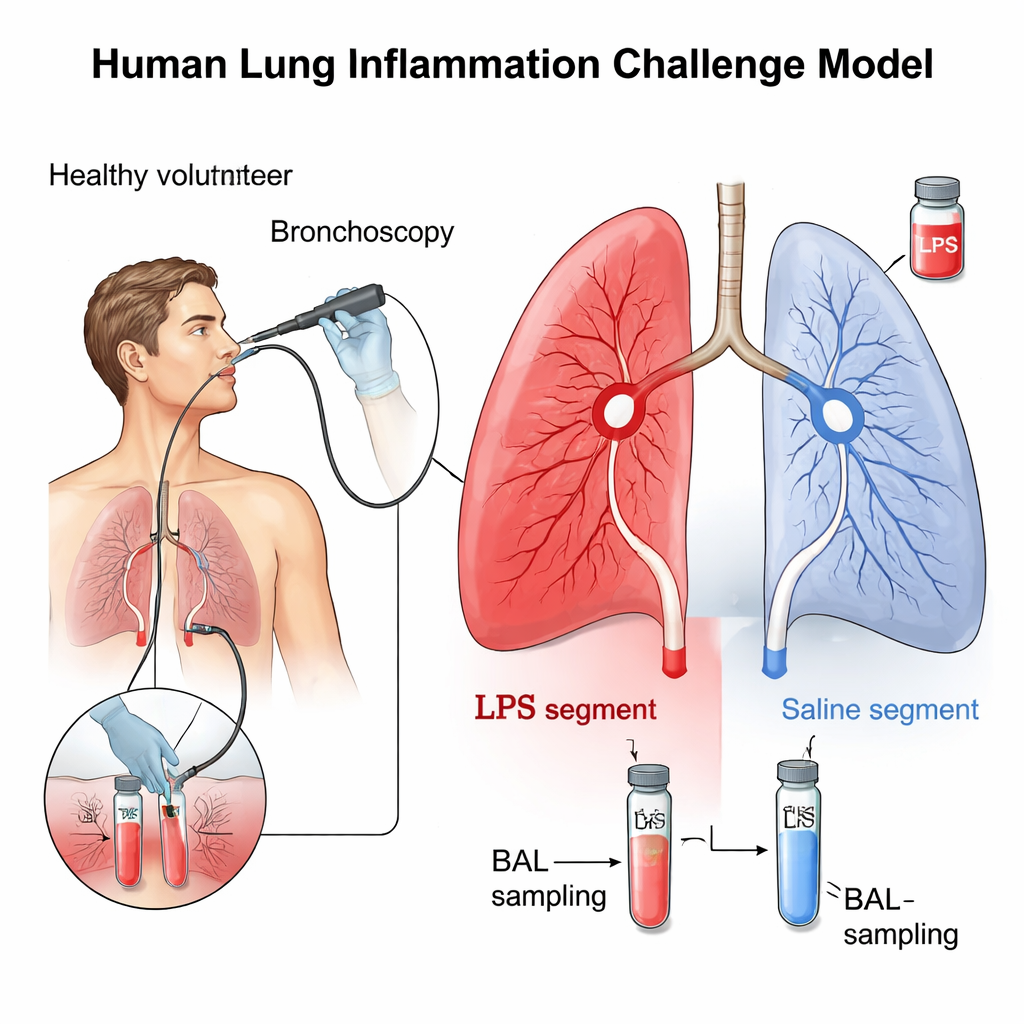
Erzeugung eines sicheren Mini‑„Lungenflairs“
Die Forschenden verwendeten eine gut etablierte Technik, die kurzzeitig und lokal eine kleine Region der Lunge reizt. Zehn gesunde, nichtrauchende Erwachsene unterzogen sich einer Bronchoskopie, bei der ein dünner flexibler Schlauch in die Atemwege geführt wird. Durch diesen Schlauch gab das Team in ein Lungenlappenstück eine winzige Dosis bakteriellen Endotoxins, bekannt als Lipopolysaccharid (LPS), und in ein entsprechendes Segment auf der anderen Seite Kochsalzlösung als Kontrolle. LPS ist ein natürlicher Bestandteil bestimmter Bakterien und aktiviert die Körperabwehr stark. Nach 24 Stunden wurden dieselben Bereiche mit Kochsalzlösung gespült – eine Prozedur, die bronchoalveoläre Lavage (BAL) genannt wird – um die Flüssigkeit und Zellen tief aus der Lunge für eine detaillierte Analyse zu sammeln.
Ein Proteinzensus in der Lungenflüssigkeit
Statt nur wenige bekannte Marker zu betrachten, nutzte das Team eine Hochdurchsatztechnologie (die SomaScan‑Plattform), die etwa 1.500 verschiedene Proteine gleichzeitig in der BAL‑Flüssigkeit messen kann. Sie verglichen Proben, die vor der Provokation, nach reiner Kochsalzlösung und nach LPS entnommen wurden. Wie zu erwarten war, sahen die Proben vor der Provokation und die Kochsalzproben sehr ähnlich aus, was bestätigt, dass das Verfahren selbst keine Entzündung auslöste. Im Gegensatz dazu zeigten die LPS‑behandelten Segmente einen dramatischen Wandel: 599 Proteine waren signifikant erhöht und nur vier verringert. Viele der angestiegenen Proteine sind bekannte Entzündungsbotenstoffe, darunter IL‑6 und IL‑8, Enzyme wie Myeloperoxidase (MPO) und MMP9 sowie akute‑Phase‑Proteine wie C‑reaktives Protein (CRP) und von Willebrand‑Faktor (VWF). Hauptkomponenten‑ und Clusteranalysen zeigten, dass sich die LPS‑Proben klar abgrenzten, was unterstreicht, wie stark diese lokale Provokation das Lungenmilieu verändert.
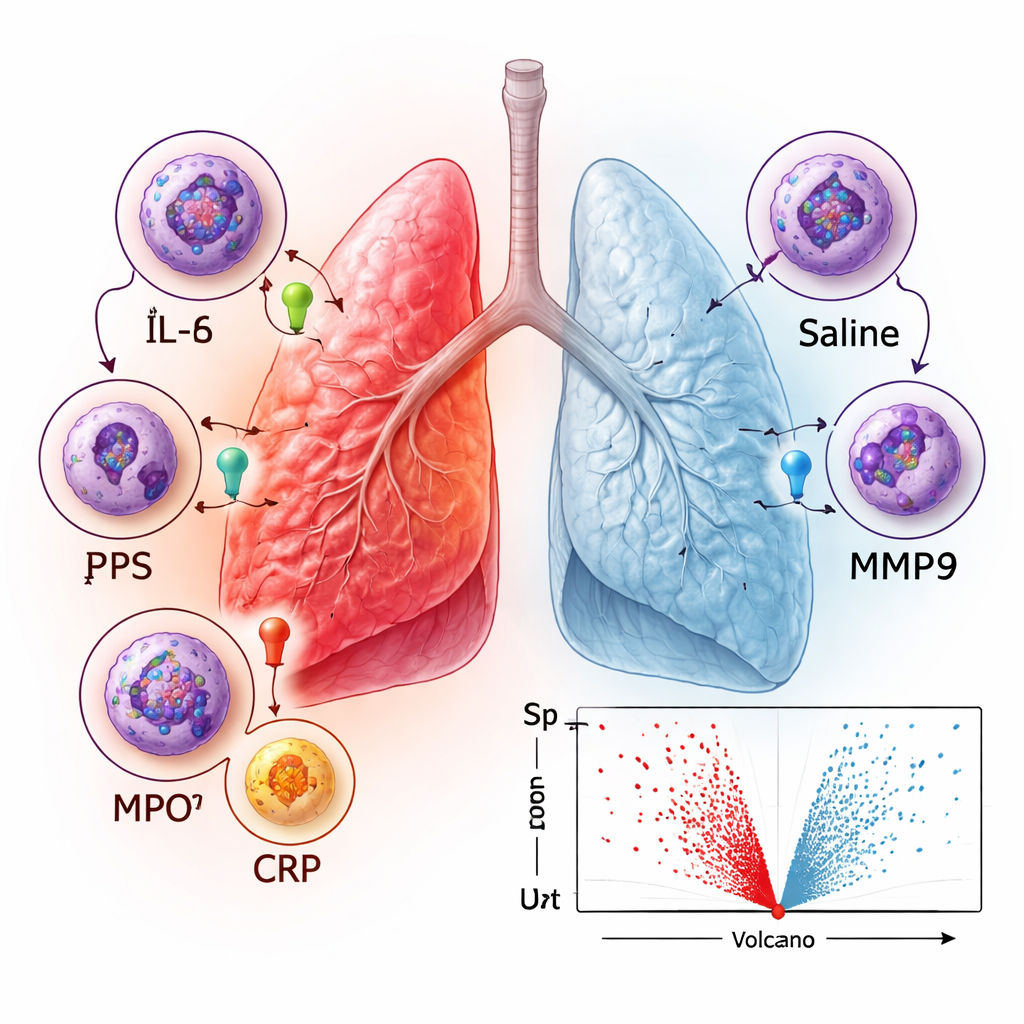
Was die Proteingemuster über die Lungenabwehr verraten
Um über Einzelmarker hinauszukommen, untersuchten die Forschenden, welche biologischen Prozesse bei den nach LPS angestiegenen Proteinen am stärksten angereichert waren. Die stärksten Signale betrafen allgemeine Immunaktivität und Reaktionen auf äußere oder chemische Stimuli sowie Prozesse, die mit Zellbewegung und programmiertem Zelltod verknüpft sind. Eine Netzwerk‑Analyse der Protein‑Interaktionen hob Cluster von Chemokinen (Moleküle, die Immunzellen anlocken), Gewebe‑umbauenden Enzymen namens Matrix‑Metalloproteinasen und Bestandteile des Immunoproteasoms hervor, einer zellulären Maschinerie, die hilft, fremde Proteine für die Immunerkennung aufzubereiten. Diese Muster stimmen mit dem überein, was über die Reaktion der Lunge auf Infektionen bekannt ist: Immunzellen wie Neutrophile werden in die Atemwege gezogen, schädliche Mikroben werden bekämpft und das umgebende Gewebe wird umgestaltet und gegebenenfalls repariert.
Verbindung des Modells mit realen COPD‑Schüben
Die Autorinnen und Autoren fragten anschließend, wie gut dieses kurzfristige LPS‑Modell reale COPD‑Exazerbationen widerspiegelt. Sie verglichen ihre Lungenflüssigkeitsdaten mit einer publizierten Liste von Blut‑Biomarkern, die bei COPD‑Schüben ansteigen. Von 17 auswertbaren Markern waren 16 – darunter IL‑6, IL‑8, CRP, Fibrinogen und mehrere Chemokine – auch in der BAL nach LPS erhöht. Nur einer (sTREM‑1) veränderte sich nicht, was mit früheren uneinheitlichen Ergebnissen zu seiner Aussagekraft übereinstimmt. Diese starke Überlappung deutet darauf hin, dass viele der gleichen Entzündungswege aktiviert werden, wenn eine gesunde Lunge kurz mit LPS gereizt wird und wenn eine anfällige COPD‑Lunge eine schwere Exazerbation durchläuft. Gleichzeitig weisen die Autorinnen und Autoren darauf hin, dass die LPS‑Reaktion vorübergehend ist und nicht die chronischen, strukturellen Schäden vollständig reproduziert, die bei langfristiger Erkrankung auftreten.
Was das für zukünftige Therapien bedeutet
Einfach ausgedrückt zeigt diese Studie, dass eine kontrollierte, kurz anhaltende Reizung eines Lungenbereichs bei gesunden Freiwilligen einen chemischen Sturm auslösen kann, der dem bei COPD‑Schüben sehr ähnlich ist. Durch die Kartierung hunderter Proteine, die während dieser Antwort ansteigen oder sinken, erhalten Forschende ein detailliertes Bild davon, welche Signale und Signalwege am wichtigsten sein könnten, um sie gezielt anzugehen. Da das Modell sicher, reproduzierbar und bereits in frühen Arzneimittelstudien verwendet wird, bietet es ein leistungsfähiges Prüfmodell für neue entzündungshemmende Wirkstoffe und zur Identifizierung präziserer Biomarker, die eines Tages Ärzten helfen könnten, das plötzliche Verschlimmern chronischer Lungenerkrankungen besser vorherzusagen, zu erkennen und zu behandeln.
Zitation: Gress, C., Müller, M. & Hohlfeld, J.M. Proteomic profiling of bronchoalveolar lavage following human segmental endotoxin challenge—a potential exacerbation model. Sci Rep 16, 6145 (2026). https://doi.org/10.1038/s41598-026-39528-x
Schlüsselwörter: Lungenentzündung, COPD‑Exazerbation, bronchoalveoläre Lavage, Endotoxin‑Provokation, Proteomik