Clear Sky Science · de
Strukturelle Modellierung und Docking-Analyse kanonischer und neuartiger, resistenzassoziierter Missense-Mutationen in sudanesischen Escherichia coli
Warum das für die Gesundheit im Alltag wichtig ist
Antibiotikaresistente Infektionen sind keine seltenen medizinischen Kuriositäten mehr; sie bedrohen zunehmend Routinebehandlungen bei Harnwegsinfektionen, Operationen und auf Intensivstationen. Diese Studie untersucht Escherichia-coli-Bakterien aus dem Sudan und stellt eine sehr konkrete Frage: Wie verändern winzige genetische Veränderungen in bakteriellen Proteinen die Wirkung gängiger Antibiotika? Durch den Einsatz computerbasierter Strukturmodellierung statt teurer Laborexperimente decken die Autorinnen und Autoren verborgene Resistenzmuster auf, die Standardtests und globale Datenbanken übersehen können – besonders in ressourcenarmen Regionen, in denen die Resistenz am schnellsten zunimmt. 
Ein Blick in das Werkzeugkasten der Bakterien
Die Forschenden konzentrierten sich auf „Missense“-Mutationen – einzelbasige DNA-Veränderungen, die einen Baustein eines Proteins gegen einen anderen austauschen. Sie analysierten komplette Genomsequenzen von 55 E.-coli-Isolaten aus dem Sudan und fokussierten sich auf bakterielle Proteine, die direkte Ziele wichtiger Antibiotikaklassen sind, darunter Fluorchinolone, Makrolide und Rifampicin. Zu diesen Zielen gehören DNA-windende Enzyme (Gyrase und Topoisomerase IV), das Proteinsynthese-Ribosom und die RNA-Polymerase. Von 71 in diesen Proteinen gefundenen Mutationen wurden 19 von mehreren Vorhersagewerkzeugen als wahrscheinlich funktionsschädigend eingestuft, und auffällig war, dass die meisten davon offenbar neuartige Varianten sind, die in globalen Resistenzdatenbanken noch nicht katalogisiert sind.
Neue Problemstellen in vertrauten Zielstrukturen
Einige der wichtigsten Veränderungen konzentrierten sich in einem ribosomalen Protein namens L22, das an der Bildung des Tunnels beteiligt ist, durch den neu synthetisierte Proteine das Ribosom verlassen. Diese Region dient zugleich als Andockstelle für Makrolid-Antibiotika wie Erythromycin. Die Studie identifizierte eine dichte Reihe bisher nicht berichteter L22-Mutationen, viele davon innerhalb eines einzelnen Stamms, die genau entlang dieses Tunnels und an Kontaktstellen mit ribosomaler RNA liegen. Computationale Analysen deuteten darauf hin, dass mehrere dieser Veränderungen die lokale Struktur destabilisieren oder flexibler machen und so den Tunnel umformen könnten, wodurch Makrolid-Moleküle weniger bündig passen. Gleichzeitig traten bekanntere „kanonische“ Resistenzmutationen in DNA-verarbeitenden Proteinen ParC und ParE sowie in der RNA-Polymerase auf, was bestätigt, dass sudanesische Stämme einige globale Resistenzmerkmale teilen, gleichzeitig aber eigene lokale Varianten besitzen.
Wie Formveränderungen den Antibiotika-Griff schwächen
Das Team ging über reine Sequenzlisten hinaus und fragte, wie diese Mutationen die dreidimensionale Passung zwischen Antibiotika und ihren Zielproteinen verändern könnten. Mithilfe molekularer Docking-Simulationen verglichen sie, wie verschiedene Wirkstoffe an normale und mutierte Proteine binden. Für das Topoisomerase-IV-Protein ParC schwächten Schlüsselmutationen in der Nähe der Wirkstoffkontaktstelle die vorhergesagte Bindung des Fluorchinolons Trovafloxacin deutlich, was einen lockereren Griff an der Enzym–DNA–Wirkstoff-Schnittstelle widerspiegelt. Im verwandten ParE-Protein reduzierten Mutationen die Bindung von Novobiocin moderat. Im Gegensatz dazu schien eine neuartige Mutation im Gyrase-Protein GyrA die Struktur des Enzyms zu destabilisieren, ohne die Bindungsstärke des Fluorchinolons Moxifloxacin merklich zu verändern, was darauf hindeutet, dass Resistenz manchmal dadurch entsteht, dass die Enzymfunktion subtil gestört wird, statt das Wirkstoffmolekül einfach zu verdrängen. 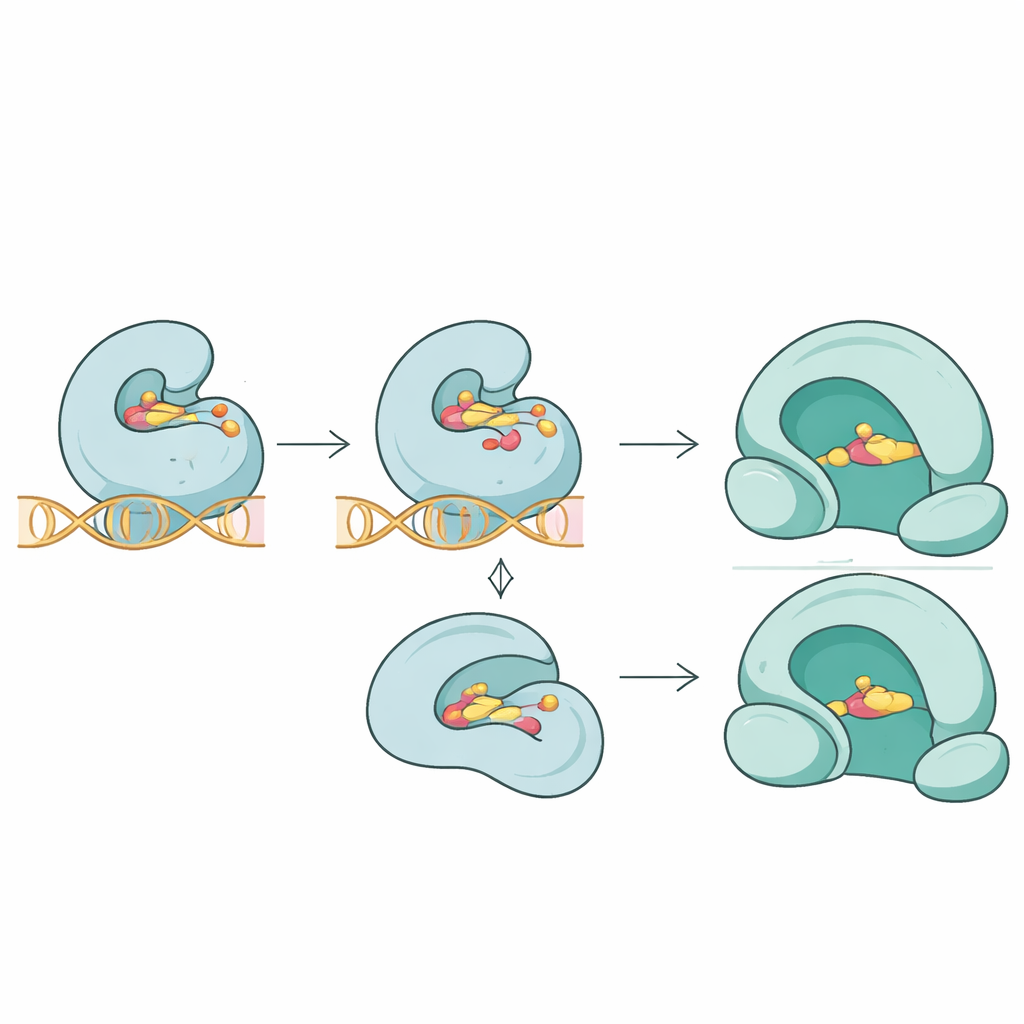
Gemischte Effekte bei verschiedenen Wirkstoffen
Nicht alle Mutationen zeigten denselben Effekt. Klassische Rifampicin-Resistenzveränderungen im RNA-Polymerase-Protein RpoB beeinträchtigten die Bindung eines neueren, strukturell anders gearteten Inhibitors, der eine benachbarte Stelle angreift, nur wenig – was nahelegt, dass künftige Wirkstoffe so gestaltet werden könnten, dass sie bestehende Resistenzmechanismen umgehen. Für das ribosomale Protein L22 zeigten Docking-Studien mit Erythromycin ein Flickwerk von Ergebnissen: Manche Mutationen schwächten die Bindung, manche hatten kaum Einfluss, und eine verbesserte sogar leicht die vorhergesagte Passung. Diese Befunde unterstreichen, dass Resistenz selten absolut ist; vielmehr verändert jede Mutation die Stabilität, Flexibilität und Wirkstoffbindung eines Proteins in unterschiedliche Richtungen, und die Gesamtwirkung auf die Behandlung hängt davon ab, wie sich diese Veränderungen in einer lebenden Bakterienzelle kombinieren.
Was das für Patientinnen, Patienten und Überwachung bedeutet
Aus laienverständlicher Sicht lautet die zentrale Botschaft, dass Bakterien in Regionen wie dem Sudan über sowohl bekannte als auch weniger bekannte Wege Resistenzen entwickeln. Die bekannten Wege umfassen klassische Mutationen, die bereits von internationalen Programmen überwacht werden, doch zeigt diese Studie, dass zahlreiche zusätzliche, lokal angereicherte Mutationen Antibiotika auf subtilere Weise abschwächen können. Indem die Veränderungen auf detaillierte Proteinstrukturen abgebildet werden, liefern die Autorinnen und Autoren eine Shortlist von Mutationen, die im Labor getestet und in regionale Diagnostik-Panels aufgenommen werden sollten. Praktisch argumentiert ihre Arbeit, dass intelligente Computermodelle Ländern mit begrenzter Laborkapazität helfen können, entstehende Resistenz besser zu überwachen, was letztlich zuverlässigere Behandlungsentscheidungen unterstützt und die Entwicklung von Wirkstoffen anregen kann, die der bakteriellen Evolution einen Schritt voraus sind.
Zitation: Sage, E.E., Ibrahim, S.A.E., Firdaus-Raih, M. et al. Structural modeling and docking analysis of canonical and novel resistance-associated missense mutations in Sudanese Escherichia coli. Sci Rep 16, 8995 (2026). https://doi.org/10.1038/s41598-026-39491-7
Schlüsselwörter: antimikrobielle Resistenz, Escherichia coli, Missense-Mutationen, strukturelle Bioinformatik, Sudan