Clear Sky Science · de
Die Integration von Deep Learning mit physikbasiertem Modellieren ermöglicht hochpräzise Vorhersagen der Antikörper‑Antigen‑Schnittstelle
Warum das für zukünftige Medikamente wichtig ist
Antikörper sind die gelenkten Lenkwaffen unseres Immunsystems und bilden die Grundlage vieler moderner Therapeutika. Um bessere Antikörper zu entwerfen, müssen Forschende genau wissen, wie ein Antikörper sein Zielmolekül — das Antigen — greift. Experimentelle Bestimmungen dieser Strukturen sind zeitaufwändig und teuer. Diese Studie zeigt, dass die Kombination von Deep Learning mit klassischem, physikähnlichem Modellieren die computergestützten Vorhersagen, wo Antikörper und Antigen in Kontakt treten, deutlich verbessern kann und so die Entwicklung und das Screening von Antikörpern beschleunigen könnte.
Die Zone des Händedrucks finden
Antikörper erkennen ihre Ziele mithilfe kleiner, flexibler Schleifen an ihren Spitzen, den Binderegionen, die zusammen eine Kontaktfläche bilden. Diese Schleifen können sich biegen und verdrehen, und die passende Zone auf dem Antigen ist oft ausgedehnt und flach statt in einer tiefen Tasche konzentriert zu sein. Genau diese Flexibilität und Feinheit machen das Docking‑Problem — herauszufinden, wie die beiden Formen zusammenpassen — für Computer extrem schwierig. Traditionelle Docking‑Programme probieren viele relative Positionen der beiden Proteine aus und bewerten sie mit physikalischen Regeln wie elektrostatischer Anziehung und Verdrängung von Wasser; ohne biologische Hinweise landen sie jedoch häufig auf falschen Treffern.
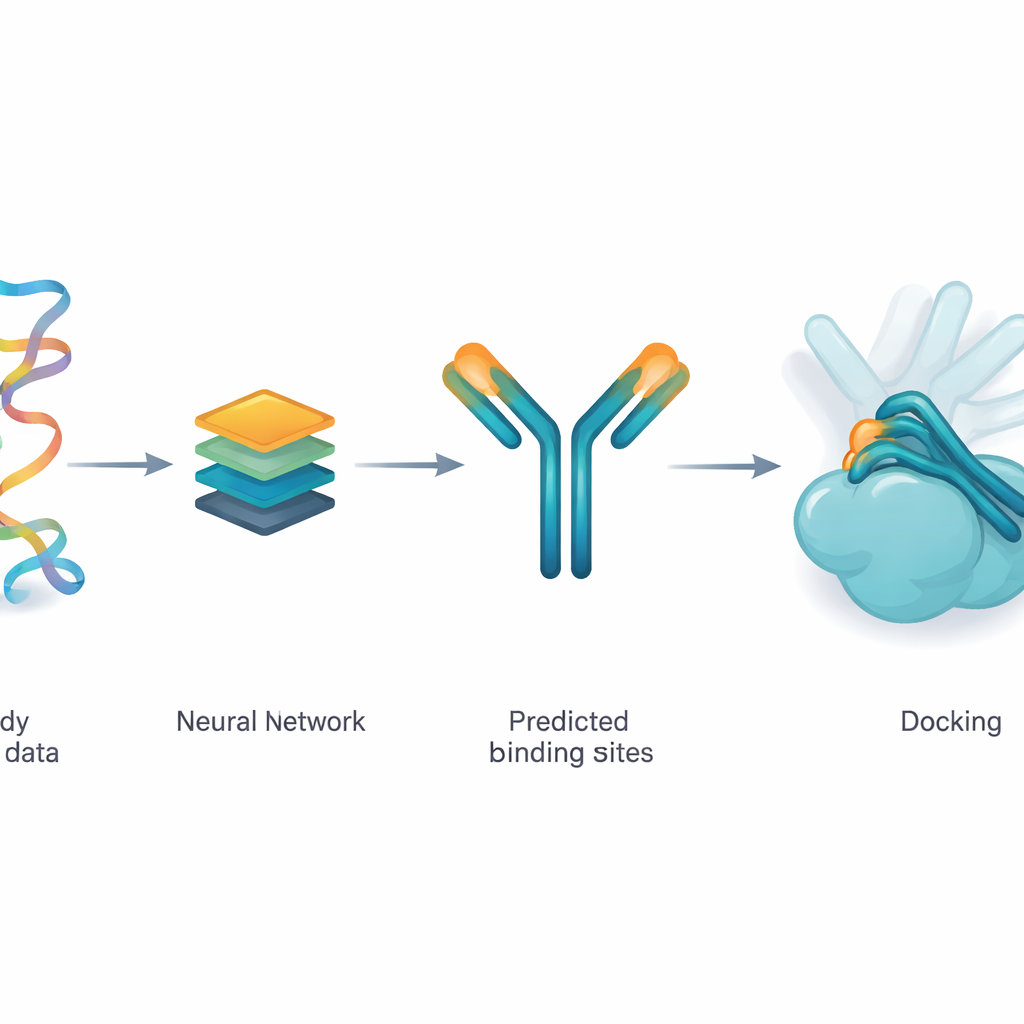
Ein Netzwerk beibringen, wahrscheinliche Kontaktstellen vorzuschlagen
Die Autorinnen und Autoren verwenden ein Deep‑Learning‑Modell namens ParaDeep, um vorherzusagen, welche Aminosäuren eines Antikörpers am ehesten das Antigen berühren. ParaDeep arbeitet allein anhand der Antikörpersequenz — der Abfolge seiner Bausteine — und benötigt keine vollständige 3D‑Struktur. Es liest die Sequenzen der schweren und leichten Kette zusammen, kodiert deren chemische und positionsbezogene Merkmale und nutzt Aufmerksamkeitsmechanismen, um Rückstände hervorzuheben, die als gute Bindekandidaten erscheinen. Jede Position erhält eine Wahrscheinlichkeitsbewertung; jene oberhalb einer Schwelle werden als vorhergesagte Kontaktzone behandelt, die auf die Antikörperstruktur zurückprojiziert werden kann.
Eine Physik‑Engine leiten statt ersetzen
Anstatt Deep Learning zu verwenden, um komplette Antikörper–Antigen‑Komplexe von Grund auf zu erzeugen, speist das Team die von ParaDeep vorhergesagten Kontaktresiduen in eine bestehende physikbasierte Docking‑Engine namens PyDockWEB. Dieses Docking‑Programm sampelt Tausende möglicher Begegnungsweisen von Antikörper und Antigen und bewertet sie mit einer Energiefunktion. Im neuen Rahmen fungieren die vorhergesagten Kontaktresiduen als weiche Zwänge: Sie lenken die Suche so, dass viele der gesampelten Orientierungen diese Residuen in die Nähe der Antigenoberfläche bringen. Wichtig ist, dass die zugrundeliegende physikalische Bewertung und die Behandlung der Proteine als starre Körper unverändert bleiben, wodurch der Prozess transparent und relativ ressourcenschonend bleibt.
Wie viel besser werden die Vorhersagen?
Die Forschenden testeten ihren hybriden Ansatz an 50 bekannten Antikörper–Antigen‑Komplexen aus einer kuratierten Datenbank. Für jeden Fall verglichen sie das standardmäßige, „blinde“ Docking mit dem durch ParaDeep‑Zwänge geführten Docking. Sie maßen die lokale Schnittstellen‑Genauigkeit (wie eng die vorhergesagte Kontaktregion der Realität entsprach), die allgemeine Formähnlichkeit und eine kombinierte Qualitätsmetrik, die häufig zur Bewertung von Docking‑Modellen verwendet wird. In diesem Datensatz reduzierte die geführte Methode die Fehler an der Bindungsstelle deutlich, brachte die Gesamtstrukturen näher an die tatsächlichen Komplexe und verschob viele Vorhersagen von klar falsch in mittel- oder hochqualitative Kategorien. Fast die Hälfte der geführten Modelle erreichte den Hochqualitätsbereich, gegenüber etwa einem Viertel beim blinden Docking.
Was manche Treffer leichter macht als andere
Das Team untersuchte auch, warum einige Komplexe stärker profitierten als andere. Sie stellten fest, dass das einfache Vorhersagen einer größeren Anzahl von Kontaktresiduen keinen Erfolg garantiert; entscheidend war das Platzieren der Zwänge im richtigen Bereich, nicht deren Anzahl. Schnittstellen, die stärker hydrophil waren und mehr flexible Coil‑Segmente enthielten, ließen sich tendenziell besser docken — vermutlich weil sie gut zu PyDockWEBs Betonung auf Elektrostatik passten und sich leichter ausrichten ließen, ohne große Formänderungen zu erfordern. Als die Forschenden einige gescheiterte Fälle mit „Orakel“-Kontaktinformationen aus experimentellen Strukturen wiederholten, verbesserten sich die meisten dieser Fälle, was bestätigt, dass die genaue Lokalisierung der Kontaktfläche ein Schlüsselelement ist — aber starres Docking stößt an seine Grenzen, wenn große Formanpassungen nötig sind.
Welche Folgen das für die Zukunft hat
Anschaulich zeigt diese Arbeit, dass ein physikbasiertem Docking‑Programm ein intelligenter Hinweis darauf, wo ein Antikörper sein Ziel wahrscheinlich greift, seine Trefferquote erheblich verbessern kann, ohne den Prozess in eine undurchsichtige Black‑Box zu verwandeln. Die kombinierte ParaDeep–PyDockWEB‑Pipeline ersetzt nicht fortgeschrittenere flexible oder generative Methoden, bietet aber einen praktikablen Weg, Sequenz‑basierte Deep‑Learning‑Signale zur Steuerung vertrauter, interpretierbarer Docking‑Werkzeuge zu nutzen. Da in der Antikörperforschung und -entwicklung immer größere Sequenzbibliotheken entstehen, könnten solche hybriden Ansätze Forschenden helfen, Kandidaten schnell herauszufiltern, die strukturell mit einem gewünschten Ziel konsistent sind, und so den Weg von der Sequenz zum einsatzfähigen Antikörper schneller und fundierter zu gestalten.
Zitation: Kodchakorn, K., Udomwong, P., Pamonsupornwichit, T. et al. Integrating deep learning with physics based modeling enables high precision antibody antigen interface prediction. Sci Rep 16, 8134 (2026). https://doi.org/10.1038/s41598-026-39466-8
Schlüsselwörter: Antikörper‑Docking, Deep Learning, Paratop‑Vorhersage, Protein‑Protein‑Interaktionen, Antikörper‑Design