Clear Sky Science · de
Auswirkungen einer neoadjuvanten Chemotherapie auf die Funktionalität von aus Fett gewonnenen mesenchymalen Stromazellen und ihre modulierenden Effekte auf Fibroblasten bei onkologischen Patienten
Warum das für Krebsüberlebende wichtig ist
Viele Menschen, die eine Krebstherapie durchlaufen, haben später mit langsam heilenden Wunden und Komplikationen nach Operationen zu kämpfen. Gleichzeitig erforschen Ärzte zunehmend Wege, körpereigene, aus Fett gewonnene Reparaturzellen zu nutzen, um Gewebe die Erholung zu erleichtern. Diese Studie stellt eine praktische und dringende Frage: Sind diese Reparaturzellen nach einer Chemotherapie noch gut genug einsetzbar, und falls nicht, welche Zellen sind besonders betroffen?
Die verborgenen Helfer des Körpers
Unser Fettgewebe ist mehr als nur Energiespeicher. Es beherbergt eine vielfältige Population von vielseitigen Reparaturzellen, die als adipose mesenchymale Stromazellen (AD-MSCs) bezeichnet werden. Diese Zellen bleiben nicht passiv; sie setzen ein Gemisch aus Signalstoffen frei, das Entzündungen dämpfen, neue Blutgefäße anregen und benachbarte Zellen zum Wachstum und Wiederaufbau geschädigten Gewebes anregen kann. Direkt über dem Fett, in der Haut, leben Fibroblasten — Arbeitstiere, die in Wunden einwandern und Kollagen ablagern, das Proteingerüst, das neuem Gewebe Festigkeit verleiht. Gemeinsam bestimmen AD-MSCs und Fibroblasten maßgeblich, wie gut die Haut nach Verletzung oder Operation wiederhergestellt wird.
Untersuchung von Fett-Reparaturzellen vor und nach der Behandlung
Die Forschenden entnahmen kleine Haut- und Fettproben von 66 operierten Patienten, von denen einige zuvor eine Chemotherapie erhalten hatten und andere nicht. Aus dem Fett isolierten sie AD-MSCs und bestätigten, dass diese Zellen weiterhin wie echte Reparaturzellen aussahen und sich verhielten: Sie trugen die erwarteten Oberflächenmarker und konnten im Labor zu knochen-, knorpel- und fettähnlichen Zellen differenzieren. Aus der Haut isolierten sie Fibroblasten. Anschließend verglich das Team, wie AD-MSCs und Fibroblasten aus chemoexponierten und nicht-exponierten Patienten wuchsen, sich durch den Zellzyklus teilten, Signalstoffe freisetzten und Gene exprimierten, die mit Wundheilung und Regeneration verknüpft sind.
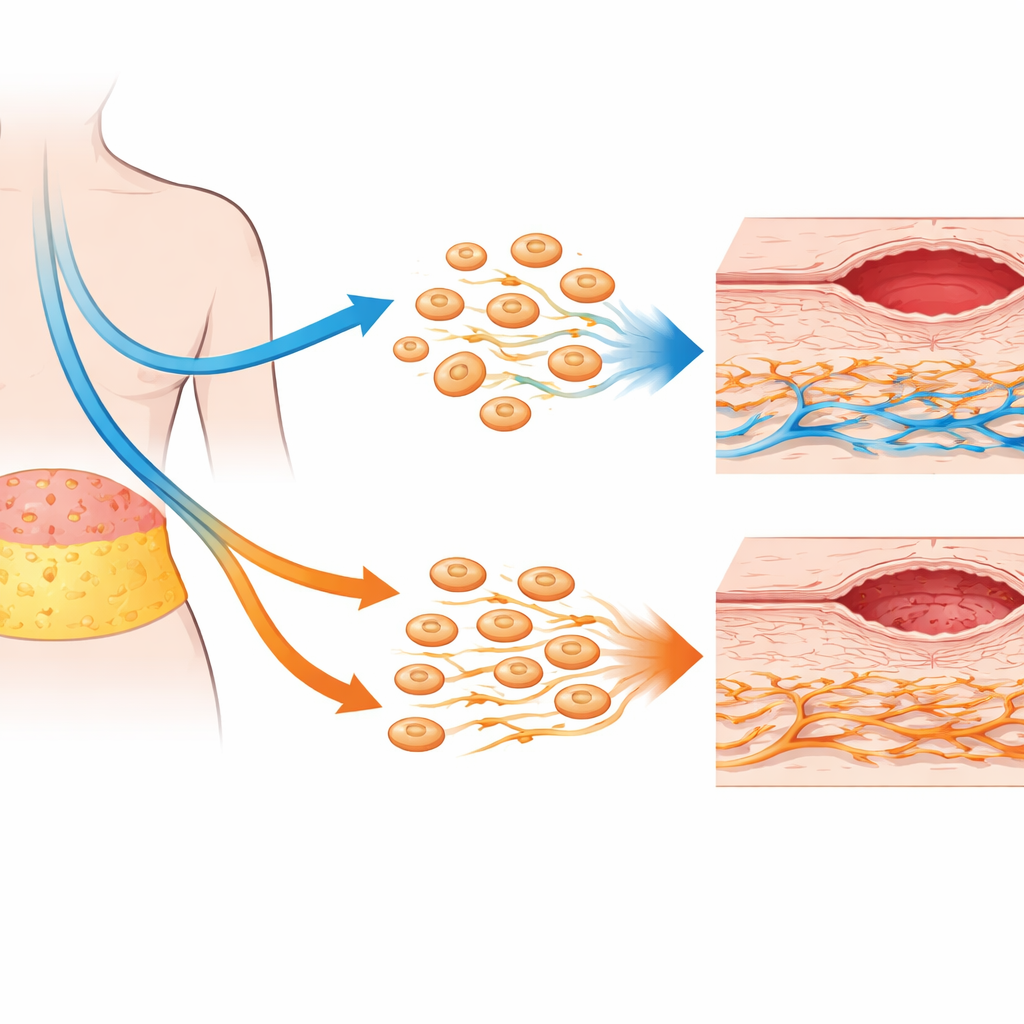
Fett-Reparaturzellen bleiben überraschend robust
Entgegen der Befürchtung, die Chemotherapie könnte die Leistungsfähigkeit von AD-MSCs schwächen, zeigte die Studie, dass diese aus Fett gewonnenen Reparaturzellen bemerkenswert widerstandsfähig sind. Ihre grundlegenden Identitätsmarker, ihr Wachstumsmuster und das Profil der sekretorischen Signalmoleküle blieben durch die vorherige Chemotherapie weitgehend unverändert. Die Genaktivität, die mit Wachstum, Selbsterneuerung und Wundheilung in Verbindung steht, zeigte nur kleine, nicht signifikante Veränderungen. Tatsächlich wiesen AD-MSCs aus chemo-behandelten Patienten eine leicht erhöhte mitochondriale Aktivität auf, was eher auf einen robusteren Stoffwechsel als auf Schäden hindeutet. In Kokkultur-Experimenten — bei denen AD-MSCs und Fibroblasten dasselbe Medium, aber keinen direkten Kontakt teilten — förderten AD-MSCs weiterhin bestimmte fibroblastische Verhaltensweisen, etwa die gerichtete Bewegung zu Reparatursignalen, besonders in Proben von Patienten ohne Chemotherapie.
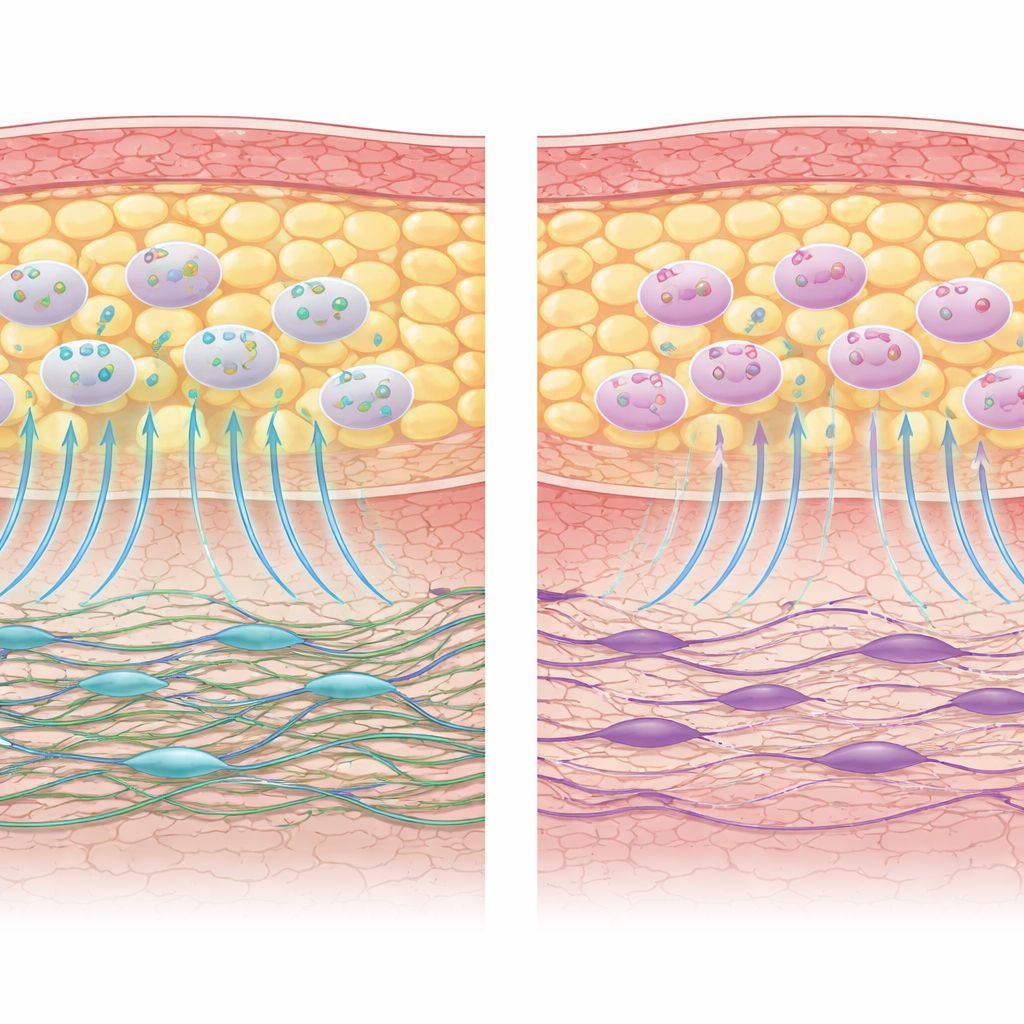
Die Hautbauer tragen die Hauptlast der Chemotherapie
Für Fibroblasten zeichnete sich ein deutlich anderes Bild ab. Aus der Haut entnommene Zellen von chemo-behandelten Patienten zeigten klare Anzeichen reduzierter biologischer Vitalität. Ihre Fähigkeit, in eine kratzähnliche „Wunde“ auf einer Kulturplatte einzuwandern, war deutlich beeinträchtigt, und ihre Kollagenproduktion war tendenziell geringer. Das Muster der freigesetzten Signalstoffe verschob sich hin zu einem stärker entzündlichen und weniger regenerativen Profil, und viele Gene, die mit Wachstumsfaktoren, deren Rezeptoren und regenerativem Potenzial zusammenhängen, waren herunterreguliert. Selbst wenn diese Fibroblasten mit ihren eigenen AD-MSCs in Kokkultur gebracht wurden, blieben die meisten ihrer Funktionen — Bewegung, Kollagenbildung und hilfreiche Genaktivität — im Vergleich zu Fibroblasten von nicht chemo-behandelten Patienten gedämpft.
Welche Bedeutung das für künftige Heiltherapien hat
Für Laien lautet die Botschaft dieser Arbeit, dass die Chemotherapie offenbar nicht die körpereigene Reserve an fettbasierten Reparaturzellen zerstört, wohl aber die vordersten Hautbauer — die Fibroblasten — weniger fähig zurücklässt, schnell in Wunden einzuspringen und starkes Gewebe wiederaufzubauen. Da AD-MSCs funktionell intakt bleiben, sind sie weiterhin vielversprechende Kandidaten für den Einsatz in Rekonstruktionsverfahren, Wundversorgung und Fetttransplantationen nach einer Krebstherapie. Der geschädigte Zustand der Fibroblasten könnte jedoch begrenzen, wie viel Nutzen diese stammzellähnlichen Zellen allein bringen können. Die Autorinnen und Autoren schlagen vor, dass künftige Therapien beide Seiten der Reparaturpartnerschaft unterstützen sollten: die Erhaltung oder Wiederherstellung der Fibroblasten-Gesundheit und zugleich die Nutzung robuster AD-MSCs, idealerweise in komplexeren, körperähnlichen Modellen, die die tatsächliche Heilungsumgebung bei Krebsüberlebenden besser abbilden.
Zitation: Skoniecka, A., Słonimska, P., Tymińska, A. et al. Impact of neoadjuvant chemotherapy on the functionality of adipose-derived mesenchymal stromal cells and their modulatory effects on fibroblasts in oncology patients. Sci Rep 16, 8614 (2026). https://doi.org/10.1038/s41598-026-39457-9
Schlüsselwörter: Chemotherapie, Wundheilung, aus Fett gewonnene Stammzellen, Fibroblasten, Regenerative Medizin