Clear Sky Science · de
Rolle der Rasterkraftmikroskopie bei der Charakterisierung heterotypischer Tumorsphäroide und ihrer Wechselwirkung mit Mikroplastikpartikeln
Warum das Gefühl von Tumorgewebe wichtig ist
Krebs wird gewöhnlich mit Genen und entarteten Zellen erklärt, doch auch das physische Gefühl — wie weich oder steif ein Gewebe ist — beeinflusst, wie ein Tumor wächst und auf seine Umgebung reagiert. Diese Studie betrachtet winzige dreidimensionale Ansammlungen von Lungenkrebszellen, sogenannte Sphäroide, und stellt zwei praktische Fragen: Kann ein hochauflösendes, tastbasiertes Mikroskop zuverlässig messen, wie steif diese Mini‑Tumoren sind, und beeinflusst diese Steifigkeit ihre Wechselwirkung mit luftgetragenen Mikroplastikpartikeln, die in die Lunge gelangen könnten?
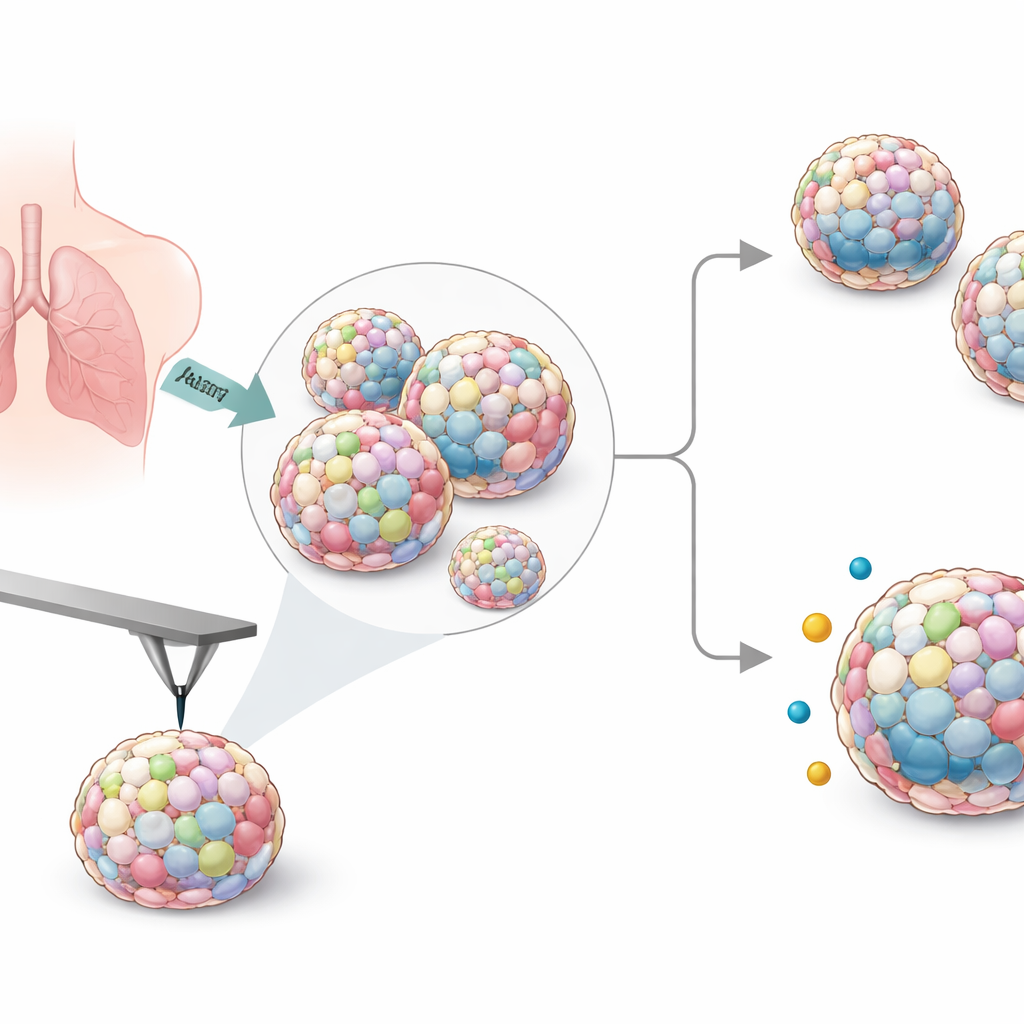
Mini‑Lungentumoren im Labor herstellen
Um die komplexe Zusammensetzung realer Tumoren nachzuahmen, züchteten die Forschenden gemischte Sphäroide aus sechs humanen Lungenkrebszelllinien zusammen mit stützenden Fibroblasten und gelegentlich immunähnlichen Makrophagen. Sie testeten mehrere Verfahren zur Bildung dieser Klumpen und entschieden sich für spezielle Niedrig‑Adhäsions‑Platten, die zuverlässig runde, stabile Sphäroide erzeugten, die groß genug zum Umgang sind. Durch Anpassung von Zellzahl und Verhältnissen erzeugten sie sowohl kleine als auch größere Sphäroide und wählten schließlich ein Standardprotokoll, das bei allen Krebszelltypen konsistent funktionierte.
Ins Innere blicken und Zellgesundheit prüfen
Sobald die Sphäroide gebildet waren, untersuchte das Team deren innere Struktur und Zellverhalten mit verschiedenen Färbungen und Schnittmethoden. Dünne Schnitte zeigten, dass einige Zellkombinationen sehr kompakte Kugeln bildeten, während andere lockerer mit mehr offenen Räumen waren. Fibroblasten neigten dazu, sich eher in der Mitte anzusammeln, besonders bei den meisten Zelllinienkombinationen, während sich die Krebszellen eher außen konzentrierten. Live‑Dead‑Färbungen zeigten ein vertrautes Muster, das auch in echten Tumoren zu sehen ist: gut ernährte, lebende Zellen am Rand und stärker geschädigte oder absterbende Zellen im sauerstoffarmen Kern. Ein DNA‑Markierungstest für Zellteilung ergab, dass sich in den meisten Sphäroiden Zellen im gesamten Aufbau noch teilen konnten, wobei eine Zelllinie (Calu‑3) hauptsächlich am äußeren Rand proliferierte.
Steifigkeit mit einer nanoskaligen Sonde messen
Um Textur in Zahlen zu überführen, verwendeten die Forschenden Rasterkraftmikroskopie, bei der eine winzige, scharfe Sonde sanft auf die Sphäroidoberfläche drückt und aufzeichnet, wie stark sie eindringt. Daraus berechneten sie den Youngschen Modul, eine standardisierte Messgröße für Steifigkeit. Obwohl die Sphäroide in ihrer Größe ähnlich waren, variierte ihre Steifigkeit deutlich je nach enthaltener Lungenkrebszelllinie. Sphäroide mit A549‑Zellen gehörten zu den weicheren, während solche mit H23‑ oder HCC827‑Zellen spürbar steifer waren. Das Einbringen von Makrophagen erhöhte bei mehreren Krebsarten im Allgemeinen die Steifigkeit. Beim Vergleich dieser Werte mit der Wachstumsrate der ursprünglichen Krebszellen in flacher Kultur stellte das Team fest, dass langsamer teilende Zellen tendenziell steifere Sphäroide bildeten, was Wachstumseigenschaften mit mechanischen Eigenschaften verknüpft.
Kontakt mit Mikroplastik testen
Da mikroskopisch kleine Kunststofffragmente in Lungentumoren nachgewiesen wurden, setzten die Forschenden ihre Sphäroide fluoreszierenden Polystyrolpartikeln von etwa einem Mikrometer Durchmesser aus, in Konzentrationen, die denen im menschlichen Blut ähneln. Unter unbewegten Bedingungen verklumpten die Partikel und hafteten ungleichmäßig an einer Seite der Sphäroide, weshalb die Gruppe zu sanftem Kippen der Proben überging, um bewegte Körperflüssigkeiten besser zu simulieren. Unter diesen dynamischen Bedingungen hefteten sich nur wenige einzelne Partikel an oder drangen in die äußeren Zellschichten ein — zu wenige für eine präzise Zählung. Stattdessen griff das Team erneut auf Steifigkeitsmessungen zurück. Nach der Exposition wurden viele Sphäroidtypen leicht steifer, was mit dem Anhaften oder Festsetzen starrer Plastikkügelchen an der Oberfläche übereinstimmt, doch diese Veränderung zeigte keine klare, einfache Abhängigkeit von der ursprünglichen Steifigkeit des Sphäroids.
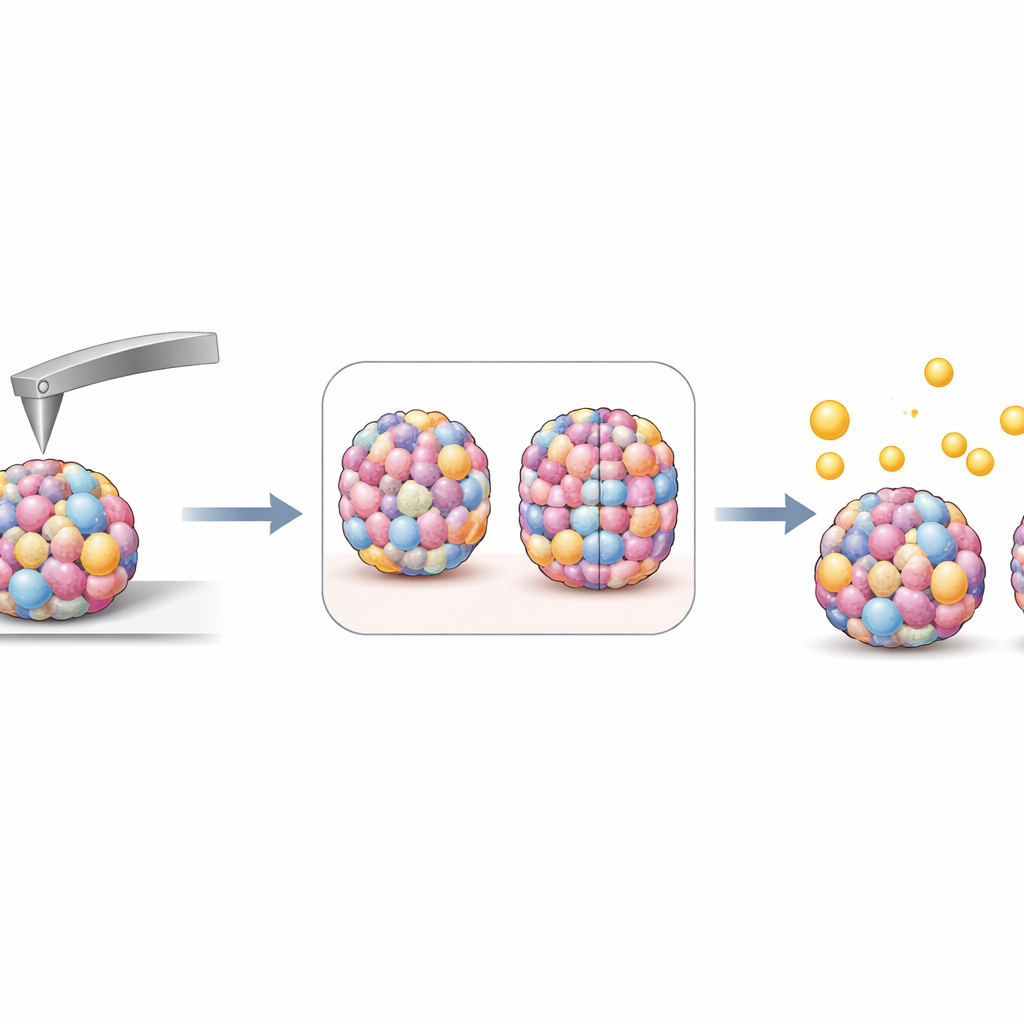
Was das für zukünftige Krebs‑ und Umweltstudien bedeutet
Die Arbeit zeigt, dass Steifigkeit ein aufschlussreicher zusätzlicher Parameter zur Beschreibung dreidimensionaler Krebsmodelle ist, die sonst in Größe und Form ähnlich erscheinen. Die Art, wie sich Zellen innerhalb des Sphäroids anordnen, und ihre Teilungsrate erklären diese mechanischen Unterschiede nur zum Teil, was darauf hindeutet, dass Steifigkeit verborgene Aspekte der Tumorbiologie erfasst. Obwohl die Studie keine direkte Regel fand, die Sphäroidsteifigkeit mit der Aufnahme von Mikroplastik bei realistischen Partikelmengen verknüpft, macht sie deutlich, dass unter sanften, bewegten Bedingungen wahrscheinlich nur wenige dieser Partikel an tumorähnlichem Gewebe haften. Langfristig könnten detaillierte Steifigkeitsmessungen kombiniert mit empfindlicheren Partikelverfolgungsmethoden Forschenden helfen, besser vorherzusagen, wie Tumoren sowohl auf Krebsmedikamente als auch auf Umweltkontaminanten reagieren, die die Lunge erreichen.
Zitation: Kolesnik, T., Öhlinger, K., Absenger-Novak, M. et al. Role of atomic force microscopy in characterization of heterotypic cancer spheroids and their interaction with microplastic particles. Sci Rep 16, 8303 (2026). https://doi.org/10.1038/s41598-026-39445-z
Schlüsselwörter: Lungentumor‑Sphäroide, Rasterkraftmikroskopie, Zellsteifigkeit, Mikroplastik, Tumormikroumgebung