Clear Sky Science · de
Entdeckung potenzieller antiviraler Verbindungen und Beschleunigung der Wirkstoffforschung gegen das Affenpockenvirus
Warum diese Forschung gerade jetzt wichtig ist
Affenpocken, inzwischen oft als mpox bezeichnet, haben sich von einer seltenen tropischen Erkrankung zu einem globalen Problem entwickelt, mit Ausbrüchen auf mehreren Kontinenten in den letzten Jahren. Im Gegensatz zu COVID-19 gibt es noch kein speziell zur Hemmung dieses Virus entwickeltes Medikament. Diese Studie nutzt fortgeschrittene Computerwerkzeuge, um nach neuen kleinen Molekülen zu suchen, die das Virus an seiner empfindlichsten Stelle treffen könnten: seiner Fähigkeit, sich vor unserem Immunsystem zu verbergen. Wenn sich diese Kandidaten im Labor bestätigen, könnten sie den Ausgangspunkt für eine neue Klasse antiviraler Wirkstoffe bilden.
Wie das Virus sich vor unseren Abwehrkräften versteckt
Affenpocken gehören zur selben größeren Familie wie die Pocken und nutzen einen raffinierten Trick, um dem Immunsystem zu entgehen. Unsere Zellen setzen ein Signalmolekül namens Interferon‑gamma frei, das normalerweise benachbarte Zellen warnt und antivirale Abwehrmechanismen aktiviert. Das Virus produziert jedoch ein eigenständiges sekretorisches Protein, genannt B8R, das außerhalb infizierter Zellen zirkuliert. B8R ahmt unseren eigenen Interferon‑gamma‑Rezeptor nach und bindet diese Immun‑Signale, bevor sie ihr eigentliches Ziel erreichen können. Effektiv wirkt es wie ein Schwamm, der die Alarmbotschaften des Körpers aufsaugt und eine vollständige antivirale Antwort verhindert.
Mit Computern schlauere Behandlungen entwerfen
Traditionelle Wirkstoffforschung kann viele Jahre und enorme Ressourcen in Anspruch nehmen. Die Forscher setzten hier auf computergestützte Wirkstoffentwicklung, um den Prozess zu beschleunigen. Da keine experimentelle 3D‑Struktur des B8R‑Proteins vorlag, nutzten sie zunächst AlphaFold‑basierte Werkzeuge, um seine atomare Gestalt vorherzusagen, und überprüften das Modell sorgfältig auf Qualität. Mit einer verlässlichen 3D‑Struktur in der Hand durchsuchten sie virtuell eine chemische Bibliothek von 5000 kleinen Molekülen. Regeln, die beschreiben, was ein „pillenähnliches“ Arzneimittel ausmacht (wie Größe, Form und Löslichkeit), wurden angewandt, um ungeeignete Kandidaten herauszufiltern, sodass 2890 vielversprechende Verbindungen für detailliertere Tests gegen das B8R‑Proteinmodell übrig blieben.
Ein vielversprechender chemischer „Schlüssel“
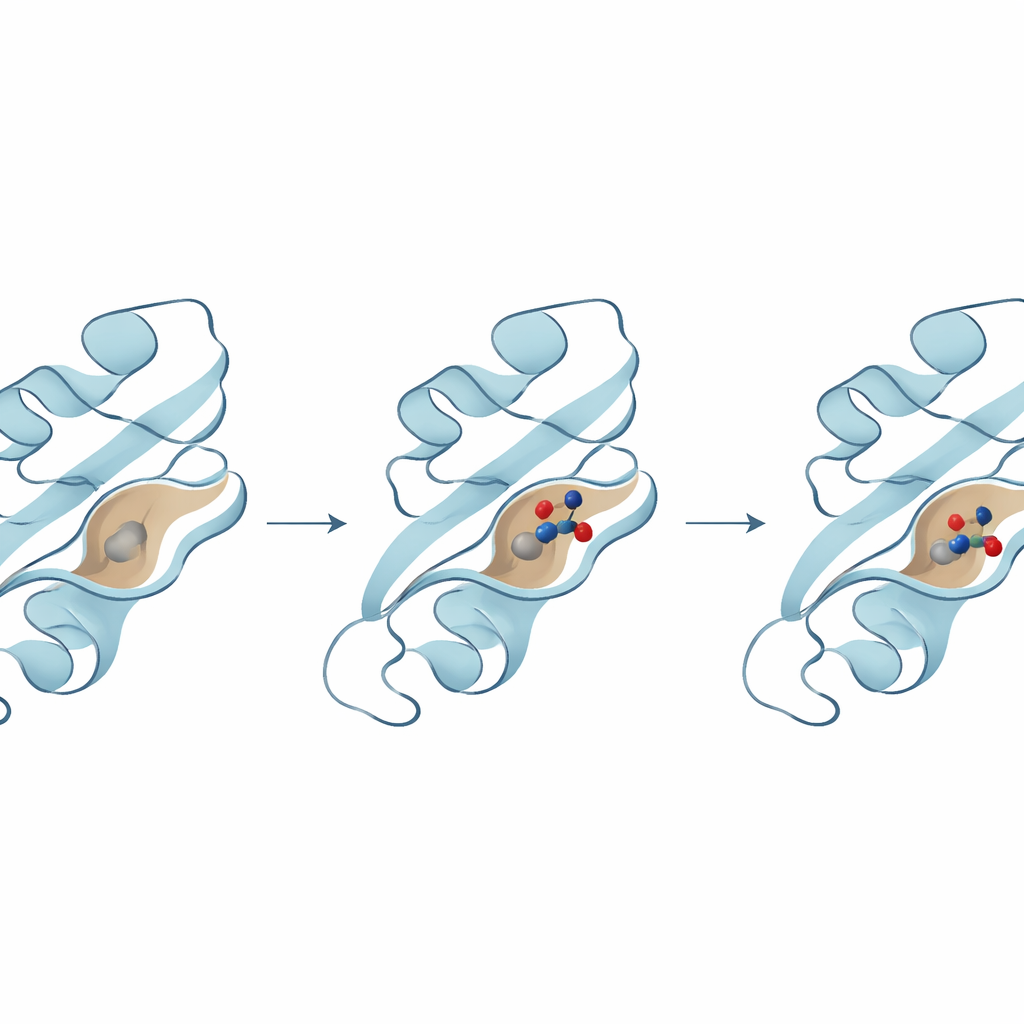
Als Nächstes prüften die Forscher, welche Moleküle sich passgenau in eine wichtige Tasche auf der B8R‑Oberfläche einfügen könnten, an der normalerweise die Wechselwirkung mit Interferon‑gamma erfolgt. Das Team verwendete molekulares Docking, eine Methode, die Milliarden möglicher Anordnungen eines Moleküls in einer Proteintasche durchspielt und bewertet, wie fest es binden würde. Drei Spitzenkandidaten traten hervor, von denen jeder starke Wechselwirkungen mit Schlüsselaminosäuren in der Tasche zu bilden vorgab. Ein bestimmter Wirkstoff zeigte dabei die stärkste Bindungsenergie und mehrere stabilisierende Kontakte mit kritischen Resten, die ihn verankern — ein Hinweis darauf, dass er besonders effektiv die Aktivität von B8R blockieren könnte.
Beobachtung der Molekülbewegungen über die Zeit
Proteine und Wirkstoffmoleküle sind nicht starr; sie bewegen sich, biegen sich und „atmen“ in wässriger Umgebung. Um dies zu erfassen, führten die Forscher lange Molekulardynamik‑Simulationen — virtuelle Filme über hunderte Nanosekunden — durch, um zu sehen, wie sich jedes Protein‑Verbindungs‑Paar im Zeitverlauf verhielt. Diese Simulationen zeigten, dass die leistungsfähigste Verbindung tief in der B8R‑Tasche verankert blieb, während sich das Protein leicht um sie herum anpasste und strukturell stabil blieb. Im Gegensatz dazu wanderten die anderen beiden Verbindungen mehr, verschoben sich in alternative Taschen oder zeigten stärkere Schwankungen, was auf eine schwächere oder weniger verlässliche Bindung hindeutet. Zusätzliche Analysen zu Flexibilität, Energie und großskaligen Bewegungen zeigten alle in dieselbe Richtung: ein Wirkstoff, der durchweg den stabilsten und energetisch günstigsten Komplex bildete.
Was das für künftige Therapien bedeuten könnte
Die Studie beansprucht nicht, ein fertiges Medikament entdeckt zu haben, und es wurden noch keine Experimente in Zellen oder Tieren durchgeführt. Stattdessen liefert sie einen starken, datenbasierten Ausgangspunkt: ein spezifisches kleines Molekül, das offenbar ideal geformt ist, um sich in das Affenpocken‑Protein B8R einzuschließen und möglicherweise das Interferon‑Alarm‑System des Körpers wiederherzustellen. Indem man die Immunevasionsstrategie des Virus statt seiner Replikationsmaschinerie angreift, bietet dieser Ansatz einen neuen Blickwinkel für antivirale Therapien. Die Autoren empfehlen, ihren Leitkandidaten nun im Labor zu testen, um seine Fähigkeit zu prüfen, B8R zu blockieren und eine mpox‑Infektion direkt zu dämpfen. Gelingen diese Tests, könnte das den Weg für eine gezielte Behandlung ebnen, die dem Immunsystem hilft, das Virus besser zu erkennen und zu stoppen.
Zitation: Ahmad, F., Navid, A., Irfan, M. et al. Discovery of potential antiviral compounds and accelerating the therapeutic discovery against monkeypox virus. Sci Rep 16, 8306 (2026). https://doi.org/10.1038/s41598-026-39427-1
Schlüsselwörter: Affenpocken antiviral, Immunevasion, Wirkstoffforschung, computationale Modellierung, Interferon-Signalgebung