Clear Sky Science · de
Verlust mechanischer Belastung verursacht Synovitis, Fibrose und degenerativen Knorpelabbau über unterschiedliche Synovialzell-Subsets
Warum ausgeruhte Gelenke riskant sein können
Viele von uns haben gehört, dass übermäßige Belastung die Gelenke abnutzen kann, doch diese Studie zeigt, dass auch zu wenig Nutzung schädlich sein kann. Forschende nutzten ein Mausmodell, um zu untersuchen, was im Kniegelenk passiert, wenn Bewegung und Gewichtstragung über Wochen stark reduziert werden – ähnlich wie nach langem Gipsverband, Lähmung oder ausgedehnter Bettruhe. Durch die Verfolgung mikroskopischer Gewebeveränderungen und der Genaktivität auf Einzelzellebene entdeckten sie, wie der Verlust mechanischer Belastung eine Kaskade in der Gelenkinnenhaut auslöst, die schließlich den glatten Knorpel schädigt, der für schmerzfreie Bewegung notwendig ist.
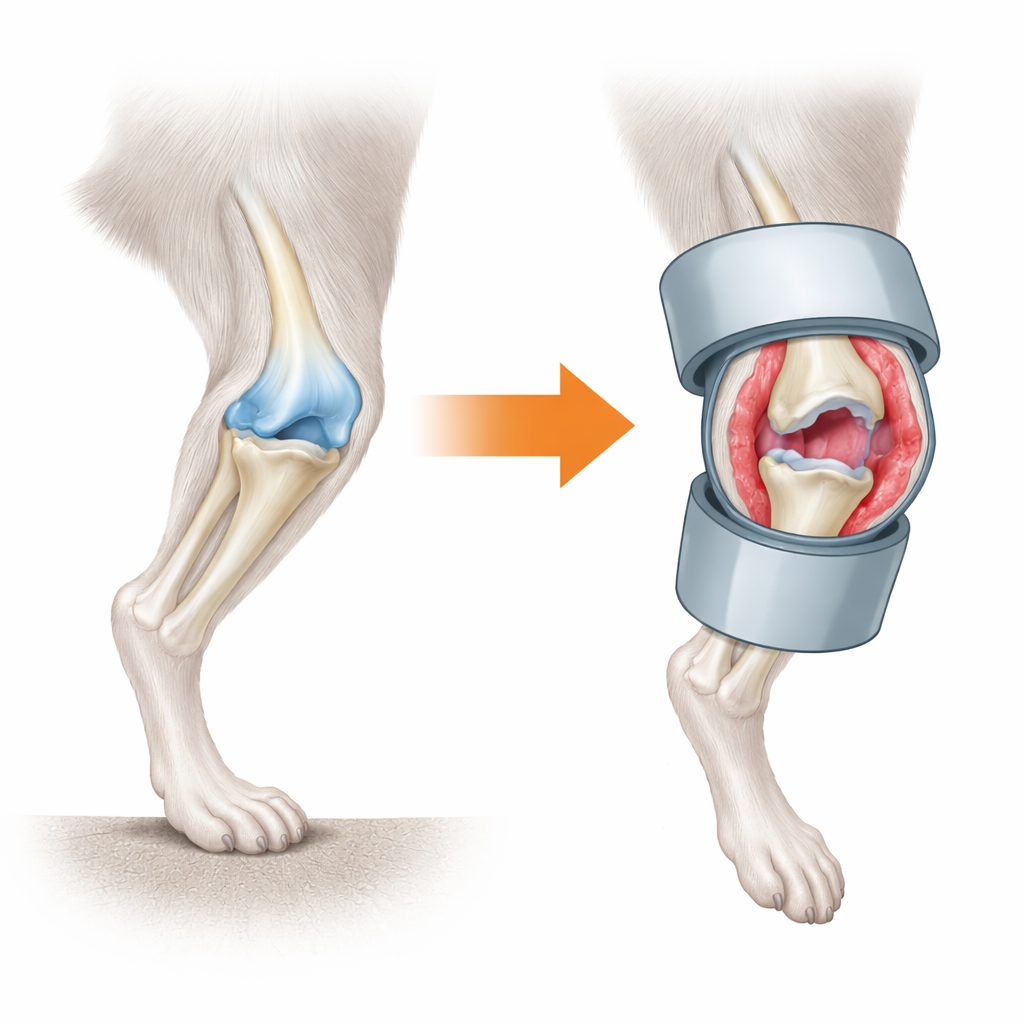
Was passiert, wenn ein Knie aufhört sich zu bewegen
Das Team erzeugte ein Modell der „minimierten mechanischen Belastung“, indem sie Mausknie mit kleinen Kunststoffzylindern immobilisierten und die Schwänze der Tiere so aufhängten, dass die Hintergliedmaßen kein Gewicht trugen. Bereits nach drei Tagen entzündete sich die Gelenkinnenhaut, die Synovialis: Ihre Zellschichten verdickten sich, neue Blutgefäße bildeten sich und Immunzellen sammelten sich an. In den folgenden zwei Wochen entwickelte die Innenhaut faseriges, narbenähnliches Gewebe und das Gelenk wurde steif. Der Knorpel – das gleitfähige Gewebe, das die Knochenenden überzieht – brach nicht sofort zusammen. Stattdessen zeigte er erst dann Rauhigkeit und Oberflächenverlust, als die synovialen Veränderungen bereits weit fortgeschritten waren, und diese Schäden verschlechterten sich über sechs Wochen hinweg.
Bewegung und Druck als Gelenkmedizin
Die Forschenden fragten dann, ob sich diese Veränderungen rückgängig machen lassen. Nach zwei Wochen Immobilisierung und Entlastung wurden bei einigen Mäusen nur die Gelenkbewegungen wiederhergestellt, während die Belastungsfreiheit bestehen blieb; andere Tiere bekamen sowohl Bewegung als auch Gewichtstragung zurück. In beiden Gruppen ließ die synoviale Entzündung nach und die Innenhaut dünnte sich wieder in Richtung Normalzustand – ein Hinweis darauf, dass einfache Bewegung die Gesundheit der Gelenkinnenhaut stark beeinflusst. Der Knorpel erholte sich jedoch am besten, wenn sowohl Bewegung als auch Belastung wiederhergestellt wurden. Auf molekularer Ebene waren Gene, die mit Knorpelaufbau und -erhalt verbunden sind, während der Nichtbenutzung stark reduziert, stiegen aber größtenteils wieder an, wenn die Gelenke wieder Bewegung und Belastung ausgesetzt wurden. Das deutet darauf hin, dass Knorpel sowohl auf gleitende Bewegung als auch auf sanften Druck angewiesen ist, um seine Struktur zu erhalten.
Wie Zellen der Gelenkinnenhaut Knorpelschäden antreiben
Bei tiefergehenden Untersuchungen analysierten die Wissenschaftler, welche Gene in der Synovialis während des Schadensprozesses aktiviert wurden. Sie fanden zunehmende Aktivität von Genen, die mit Fibrose, Gewebsumgestaltung und Enzymen verbunden sind, die Knorpel abbauen können. Viele dieser Signale stammten von immunvermittelten Botenstoffen, wie entzündlichen Zytokinen und Wachstumsfaktoren, die benachbarte Knorpelzellen beeinflussen können. Single-Cell-RNA-Sequencing zeigte, dass die Nichtbenutzung die Zellzusammensetzung in der Synovialis veränderte. Zwei ungewöhnliche Zellgruppen vermehrten sich in immobilisierten Gelenken: myofibroblastähnliche Zellen, spezialisiert auf die Produktion faseriger Matrix, und eine Subgruppe von Makrophagen, die hohe Mengen entzündlicher Moleküle und knorpelabbauender Enzyme exprimierten. Gemeinsam bildeten diese Zellen ein ausgeprägtes, schädigungsförderndes Mikroumfeld rund um das Gelenk.
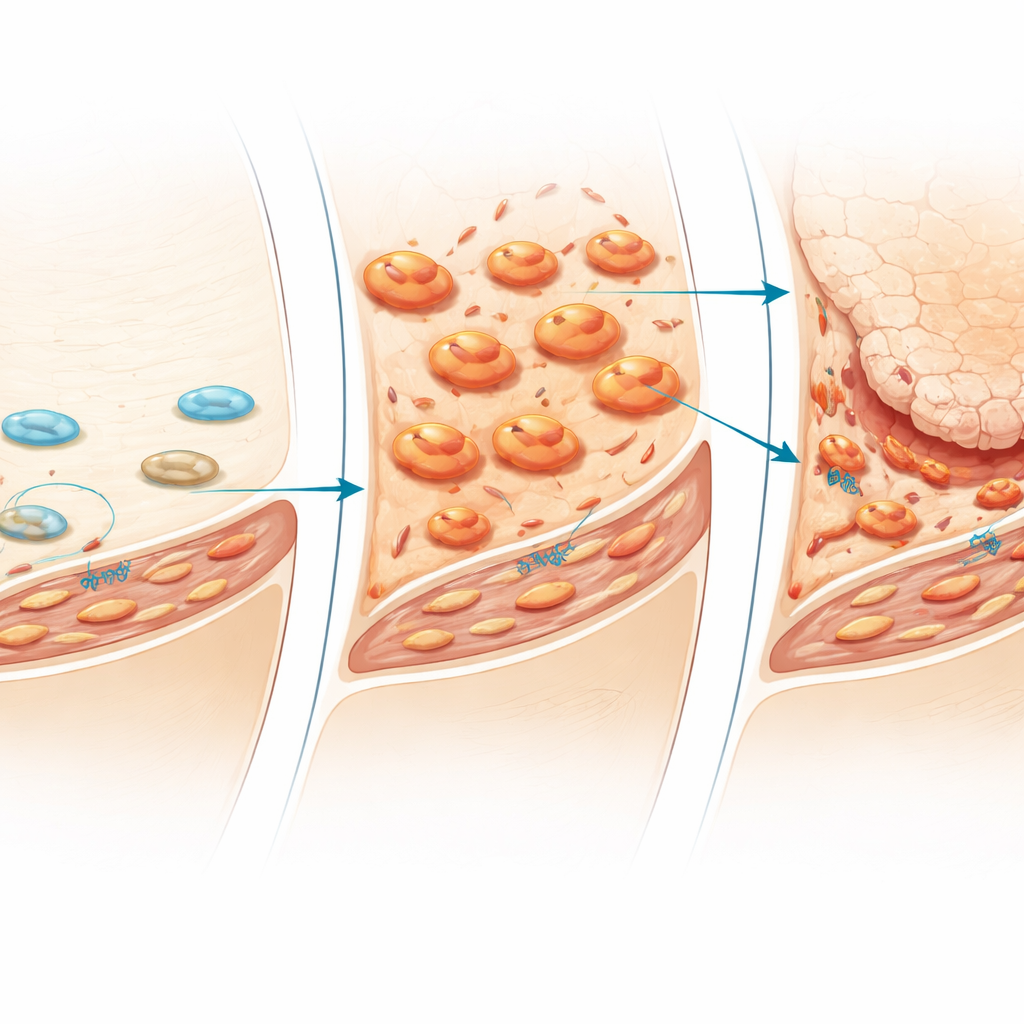
Die frühe Rolle der Immunzellen
Das Timing erwies sich als entscheidend. In Gewebeschnitten, die in verschiedenen Stadien entnommen wurden, strömten Makrophagen bereits Tage nach Entzug mechanischer Belastung zuerst in die dünne synoviale Schicht ein und breiteten sich dann tiefer ins Gewebe aus. Erst danach proliferierten Fibroblasten und es erschien dickes fibröses Gewebe. Als das Team selektiv synoviale Makrophagen durch Injektion von Liposomen, die diese Zellen eliminieren, entfernte, änderte sich die Kaskade dramatisch: Entzündung und Fibrose der Gelenkinnenhaut wurden stark reduziert und der Knorpelabbau war deutlich weniger schwerwiegend. Marker der myofibroblastären Subpopulation sanken ebenfalls. Diese Befunde deuten auf Makrophagen als frühe Organisatoren der schädlichen Reaktion auf Nichtbenutzung hin, die Fibroblasten aktivieren und die Basis für späteren Knorpelabbau legen.
Was das für den Schutz der Gelenke bedeutet
Insgesamt zeigt die Studie, dass Gelenke auf regelmäßige Bewegung und angemessene mechanische Belastung angewiesen sind, um Synovialis und Knorpel im Gleichgewicht zu halten. Wenn diese mechanische Einwirkung entfällt, schalten spezialisierte Immun- und Fibroblastenzellen in der Synovialis auf einen entzündlichen, fibrotischen Zustand um, der den Knorpel allmählich zerstört. Wichtig ist, dass die Wiederherstellung von Bewegung und Gewichtstragung diesen Prozess zurückdrehen kann, insbesondere wenn sie vor dem Fortschreiten der Schäden erfolgt. Für Menschen, die mit langen Phasen der Immobilität konfrontiert sind – durch Gipse, Lähmung oder ausgedehnte Bettruhe – unterstreichen diese Ergebnisse den Wert früher, angeleiteter Gelenkbewegung und sicherer Belastung sowie die Möglichkeit zukünftiger Medikamente, die die Makrophagen–Fibroblasten-Achse gezielt ansprechen, um bleibende Gelenkschäden zu verhindern.
Zitation: Ishikura, H., Okada, H., Kin, Y. et al. Loss of mechanical stress induces synovitis, fibrosis and articular cartilage degeneration via distinct synovial cell subsets. Sci Rep 16, 8007 (2026). https://doi.org/10.1038/s41598-026-39416-4
Schlüsselwörter: Gelenkimmobilität, Synovitis, Knorpeldegeneration, mechanische Belastung, Makrophagen