Clear Sky Science · de
Aufbau eines belastbaren präklinischen Modells zur Untersuchung frühzeitiger und spät auftretender strahleninduzierter Hautreaktionen
Warum das für Menschen mit Krebs wichtig ist
Moderne Strahlentherapie rettet Leben, kann aber die Haut stark belasten und schmerzhafte Rötungen, Abschuppung sowie langanhaltende Verhärtungen oder Narbenbildung verursachen. Ärztinnen und Ärzte wissen, dass diese Reaktionen mit der Strahlendosis zusammenhängen, doch in der Praxis war es schwierig, sie detailliert zu untersuchen oder neue Behandlungen sicher zu testen. Diese Studie beschreibt ein sorgfältig konzipiertes Mausmodell, das sowohl die frühen als auch die späten Hautprobleme nachahmt, die bei Patientinnen und Patienten beobachtet werden, und bietet damit eine praktikable Versuchsanordnung für schonendere Strahlenschemata und schützende Therapien. 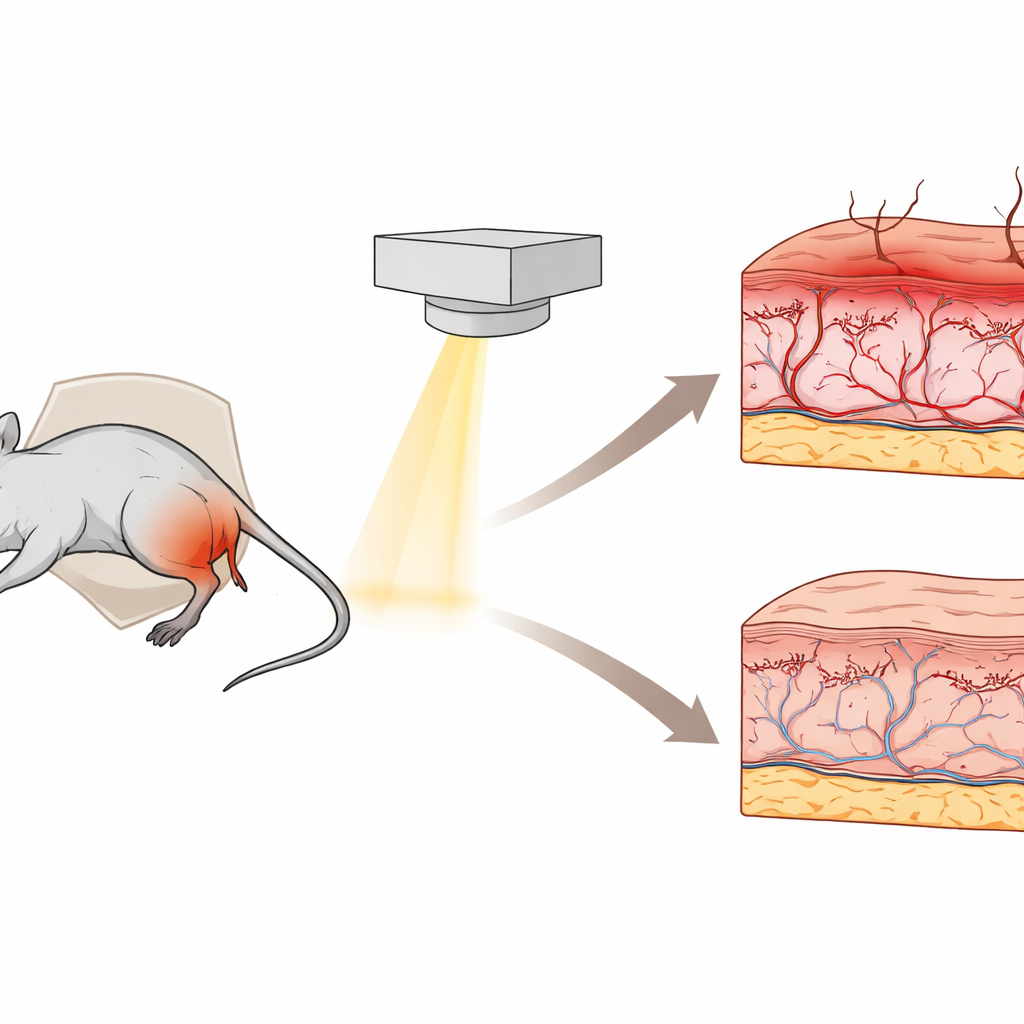
Eine häufige Nebenwirkung in den Fokus der Forschung rücken
Wenn ein Tumor bestrahlt wird, leidet oft auch die benachbarte gesunde Haut. Frühe Veränderungen können innerhalb von Tagen bis Wochen als Rötung, Schwellung und Abschuppung auftreten, während späte Veränderungen—Monate oder Jahre später—Haarausfall, Verhärtung oder Narbenbildung der Haut zeigen können. Diese Probleme können Behandlungsverzögerungen verursachen und die Lebensqualität mindern, doch existierende Tierstudien betrachten meist nur kurzzeitige Schäden oder verwenden einzelne, sehr hohe Strahlendosen, die der klinischen Praxis nicht entsprechen. Die Autorinnen und Autoren wollten ein realistischeres Modell entwickeln, das sowohl frühe als auch späte Hautschäden über die Zeit verfolgt und dafür fraktionierte Bestrahlung nutzt, denselben Grundansatz wie in der humanen Radiotherapie.
Wie das neue Mausmodell aufgebaut wurde
Die Forschenden arbeiteten mit männlichen Swiss-Albino-Mäusen und konzentrierten die Strahlung auf einen kleinen Bereich der rechten Hintergliedmaße, während der Rest des Körpers mit Blei abgeschirmt wurde. Diese Anordnung erlaubte es, eine klar abgegrenzte Hautregion zu schädigen, ohne lebenswichtige Organe zu beeinträchtigen—ähnlich wie bei der gezielten Bestrahlung eines Tumors bei gleichzeitiger Schonung des umliegenden Gewebes. Eine Gruppe von Mäusen erhielt insgesamt 30 Dosis‑Einheiten verteilt auf drei tägliche Sitzungen; eine andere Gruppe erhielt 50 Einheiten über fünf Sitzungen, was die wiederholten Expositionen in der Klinik besser widerspiegelt. Im Verlauf des nächsten Monats bewertete eine Dermatologin bzw. ein Dermatologe, der nicht wusste, welche Dosis die einzelnen Tiere erhalten hatten, sichtbare Hautveränderungen mithilfe einer standardisierten klinischen Skala, und an den Tagen 15 und 30 wurden kleine Hautproben zur mikroskopischen Analyse entnommen.
Wie die frühen Hautreaktionen aussahen
Die sichtbaren Scores zeigten eine klare Dosis‑Wirkungs‑Beziehung. Die Niedrigdosisgruppe entwickelte typischerweise moderate Reaktionen, die um Tag 10 ihren Höhepunkt erreichten und bis Tag 30 abheilten. Dagegen zeigte die Hochdosisgruppe stärkere Reaktionen, die etwas später ihren Gipfel hatten und etwa fünf zusätzliche Tage bis zur vollständigen Erholung benötigten. Mikroskopisch wies die bestrahlte Haut eine verdickte Oberhaut, eine erhöhte Zahl entzündlicher Zellen und einen deutlichen Rückgang der Haarfollikel im Vergleich zur unbelasteten Haut des anderen Beins auf. Die höhere Dosis führte zu intensiverer Entzündung, Oberflächenzerfall und einem charakteristischen Muster von Veränderungen an der Oberfläche, das auf eine schnelle, gestresste Hauterneuerung hinweist. Diese Merkmale ähneln stark dem, was Klinikerinnen und Kliniker bei Patientinnen und Patienten mit ausgeprägten frühen Hautreaktionen auf Strahlung beobachten. 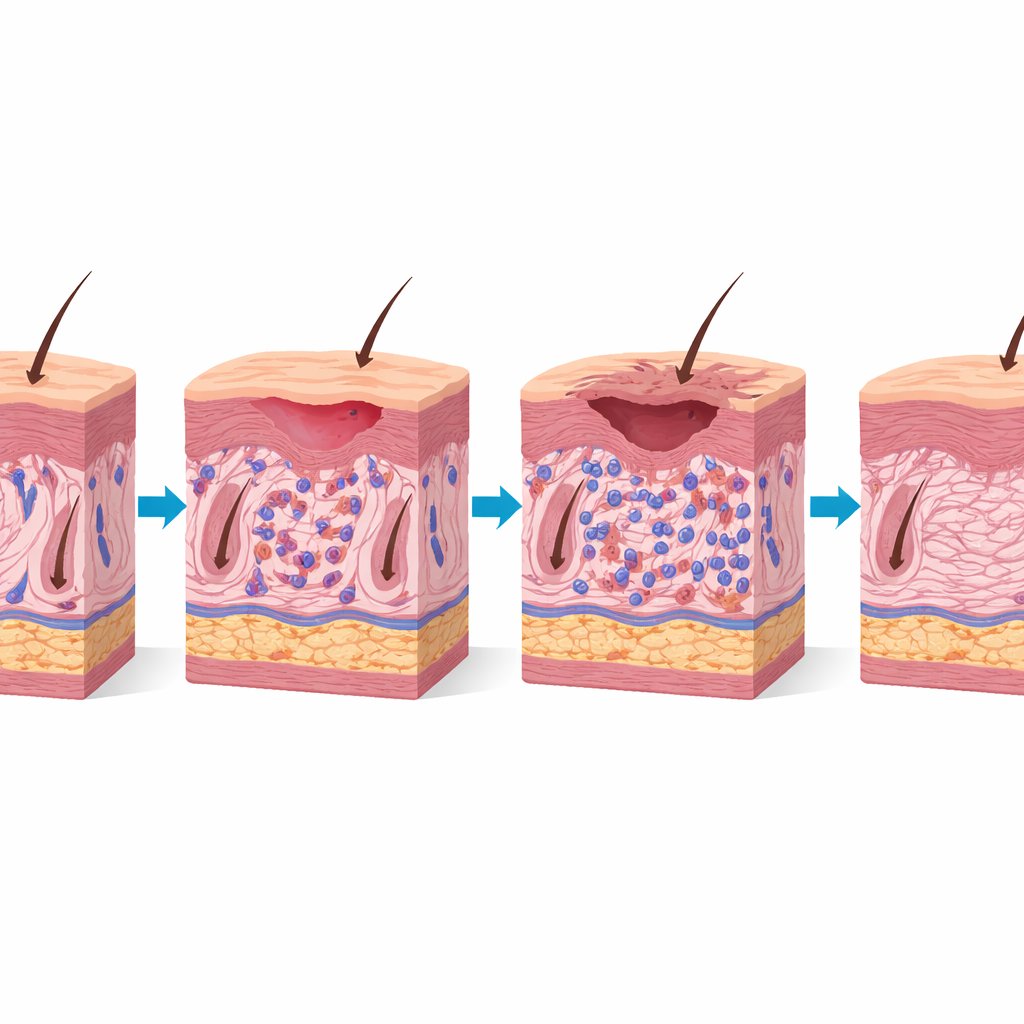
Nachverfolgung von langfristiger Narbenbildung und Haarausfall
Um späte Effekte zu erfassen, wurden die Mäuse, die die höhere Dosis erhalten hatten, über vier Monate beobachtet. Äußerlich verlor die behandelte Haut nach und nach Haare und erhielt eine festere, leicht eingezogene Beschaffenheit, was auf eine beginnende Fibrose—narbenartige Verhärtung—deutet. Gewebsfärbungen, die Kollagenfasern hervorheben, bestätigten diesen Eindruck: Die behandelte Haut wies dichtere, dickere und unorganisiertere Kollagenbündel in der tieferen Schicht sowie einen anhaltenden Verlust von Haarfollikeln auf. Die Bewertung durch eine Pathologin bzw. einen Pathologen zeigte höhere Werte für Entzündung, Fibrose und zelluläre Störung in der behandelten Haut im Vergleich zur unbehandelten Haut, während das tiefere Muskelgewebe nur mildere Veränderungen aufwies. Insgesamt deuten diese Befunde darauf hin, dass dieselben Tiere zunächst eine frühe, reversible Reaktion und später einen dauerhafteren, narbenähnlichen Zustand entwickelten—ein Verlauf, der dem beim Menschen entspricht.
Was dieses Modell für die künftige Versorgung bedeutet
Indem es kurzzeitige Reizungen und langfristige Narbenbildung in einem einzigen, kontrollierten Mausmodell nachbildet, das klinisch relevante Bestrahlungspläne verwendet, bietet diese Studie ein leistungsfähiges Werkzeug für künftige Forschung. Forschende können nun untersuchen, wie Hautzellen, Immunzellen und das Stützgewebe über die Zeit reagieren, und sie können systematisch Medikamente, Verbände oder lichtbasierte Therapien testen, die die Haut schützen oder die Heilung beschleunigen sollen. Letztlich könnten Erkenntnisse aus diesem Modell dazu beitragen, die Strahlentherapie nicht nur tumorwirksam, sondern auch hautschonender zu machen, Schmerzen zu verringern, Behandlungspausen zu vermeiden und die Lebensqualität von Menschen in der Krebsbehandlung zu verbessern.
Zitation: Pai, P.A.N., Mumbrekar, K.D., Mahato, K.K. et al. Establishing a robust preclinical model to investigate early and late radiation-induced skin reactions. Sci Rep 16, 9064 (2026). https://doi.org/10.1038/s41598-026-39414-6
Schlüsselwörter: strahleninduzierte Hautreaktionen, Nebenwirkungen der Strahlentherapie, Hautfibrose, präklinisches Mausmodell, Toxizität bei Krebsbehandlung