Clear Sky Science · de
Optimierung von THP-1-CAR-Monozyten durch CD32a-vermittelte phagozytische Signalgebung zur antigen-spezifischen T-Zell-Aktivierung
Dem Immunsystem neue Tricks beibringen
Moderne Zelltherapien programmieren Immunzellen bereits so um, dass sie Krebs aufspüren, doch die meisten setzen auf T-Zellen, die in der rauen Umgebung solider Tumoren an ihre Grenzen stoßen können. Diese Studie wendet sich stattdessen einer anderen kraftvollen Verteidigerzelle zu — Makrophagen, den professionellen "Fressern" des Körpers — und untersucht, wie man sie so umgestalten kann, dass sie nicht nur schädliche Zellen oder Viren effizienter aufnehmen, sondern auch T-Zellen zur anhaltenden, zielgerichteten Abwehr herbeirufen. Die Arbeit legt Gestaltungsprinzipien für den Bau besserer chimärer Antigenrezeptor-(CAR-)Makrophagen offen, die sowohl bei Infektionen wie COVID-19 als auch bei schwer zu behandelnden soliden Tumoren anwendbar sein könnten.
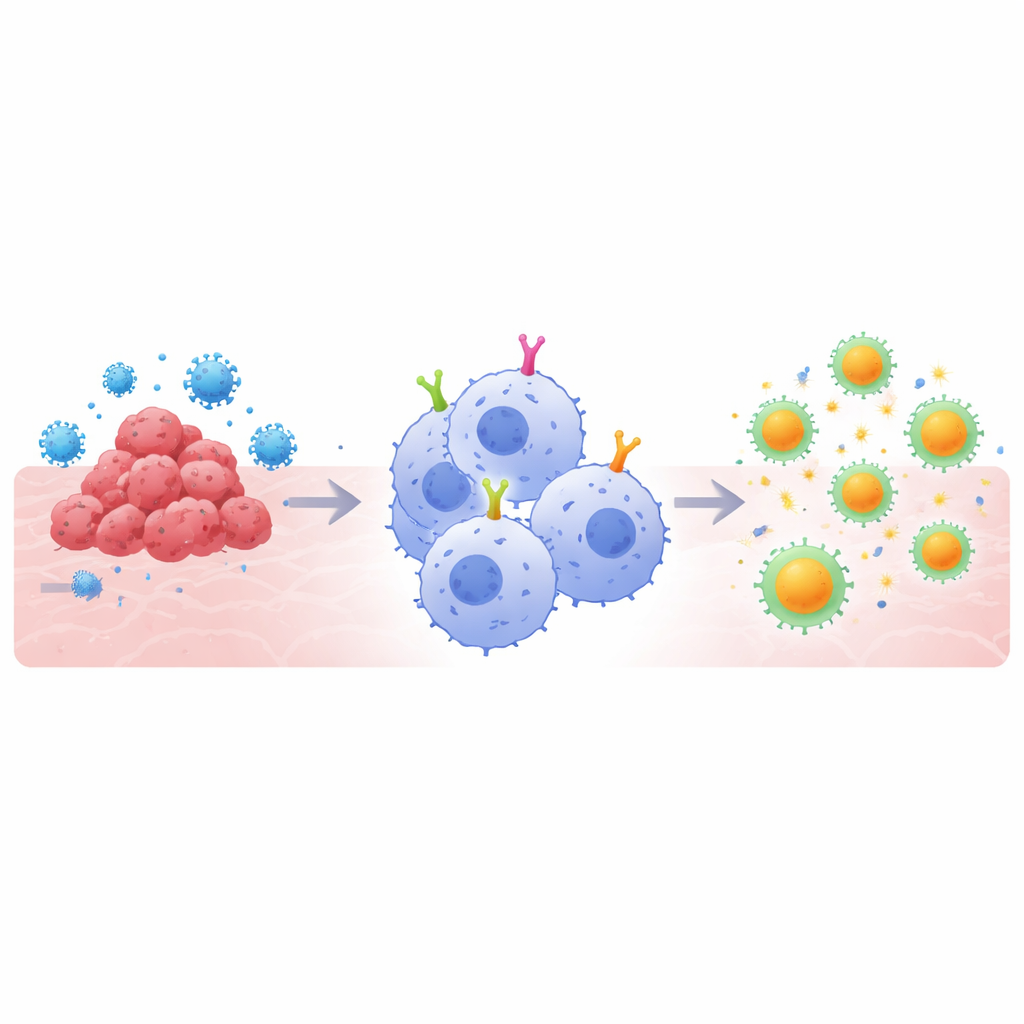
Warum Super-Fresser wichtig sind
CAR-basierte Therapien rüsten Immunzellen mit maßgeschneiderten Oberflächenrezeptoren aus, die ein bestimmtes Ziel erkennen, etwa ein Tumorprotein oder ein virales Spike-Protein. T-Zell-Versionen haben die Behandlung bestimmter Blutkrebserkrankungen revolutioniert, doch sie stoßen bei soliden Tumoren und manchen Infektionen auf Hindernisse. Makrophagen bieten einen anderen Ansatz: Sie nehmen Bedrohungen natürlicherweise auf und zerlegen sie in Stücke, die dann T-Zellen präsentiert werden können, wodurch die angeborene und die adaptive Immunantwort verbunden werden. Die meisten CAR-Designs wurden jedoch ursprünglich für T-Zellen entwickelt, nicht für Makrophagen. Die Autoren vermuteten, dass man, um die Stärken der Makrophagen vollständig auszunutzen, die internen Signalbestandteile der CARs — die Segmente, die der Zelle sagen, was zu tun ist, sobald ein Ziel gebunden ist — speziell für diese Fresszellen anpassen müsste.
Die beste interne Verdrahtung finden
Das Team verglich systematisch mehrere interne Signaldomänen innerhalb von CARs, die in eine humane Monozytenzelllinie (THP-1) eingebracht wurden, die zu Makrophagen differenziert werden kann. Im Fokus standen Domänen aus Rezeptoren, die normalerweise Phagozytose und Entzündungsreaktionen antreiben: CD3ζ (das klassische T-Zell-Modul), CD32a (ein Rezeptor, der antikörperbeschichtete Ziele bindet), CR3-Komponenten CD11b und CD18 (wichtige Komplementrezeptoren) sowie TLR4 (ein Sensor für mikrobiellen Schaden). Mit Kügelchen und Pseudoviren, die mit dem SARS-CoV-2-Spike beschichtet waren, maßen sie, wie gut jedes CAR-Design Zellen befähigte, Ziele aufzunehmen, entzündliche Moleküle zu produzieren und anschließend menschliche CD8-T-Zellen zu aktivieren, die dem Virus bereits begegnet waren. Die vielversprechendsten Designs übertrugen sie anschließend auf CARs, die Mesothelin anvisieren — ein in vielen soliden Tumoren überexprimiertes Protein — um zu prüfen, ob dieselben Regeln auch im Krebssetting gelten.
Bessere Fresser und Signalverstärker bauen
Ein klares Muster zeigte sich: CARs auf Basis von CD32a förderten konsequent stärkere und schnellere Phagozytose als solche mit der herkömmlichen CD3ζ-Domäne, obwohl CD3ζ mehr der üblichen Aktivierungsdomänen enthält. Anders gesagt, die "Passung" zwischen dem Signal und der Makrophagenmaschinerie war wichtiger als bloße Signalstärke. Das Hinzufügen von CR3-abgeleiteten Teilen (CD11b oder CD18) zusätzlich zu CD32a steigerte in den meisten Bedingungen die Aufnahmekapazität nicht weiter, erhöhte aber die Produktion wichtiger entzündlicher Zytokine wie TNF-α und IL-1β. Kombinationen mit TLR4 verstärkten die entzündlichen Signale und den Oberflächenmarker CD86, der mit T-Zell-stimulierender Kapazität verbunden ist, gingen jedoch mit Kompromissen einher: geringere CAR-Level auf der Zelloberfläche und etwas reduzierte Phagozytose.
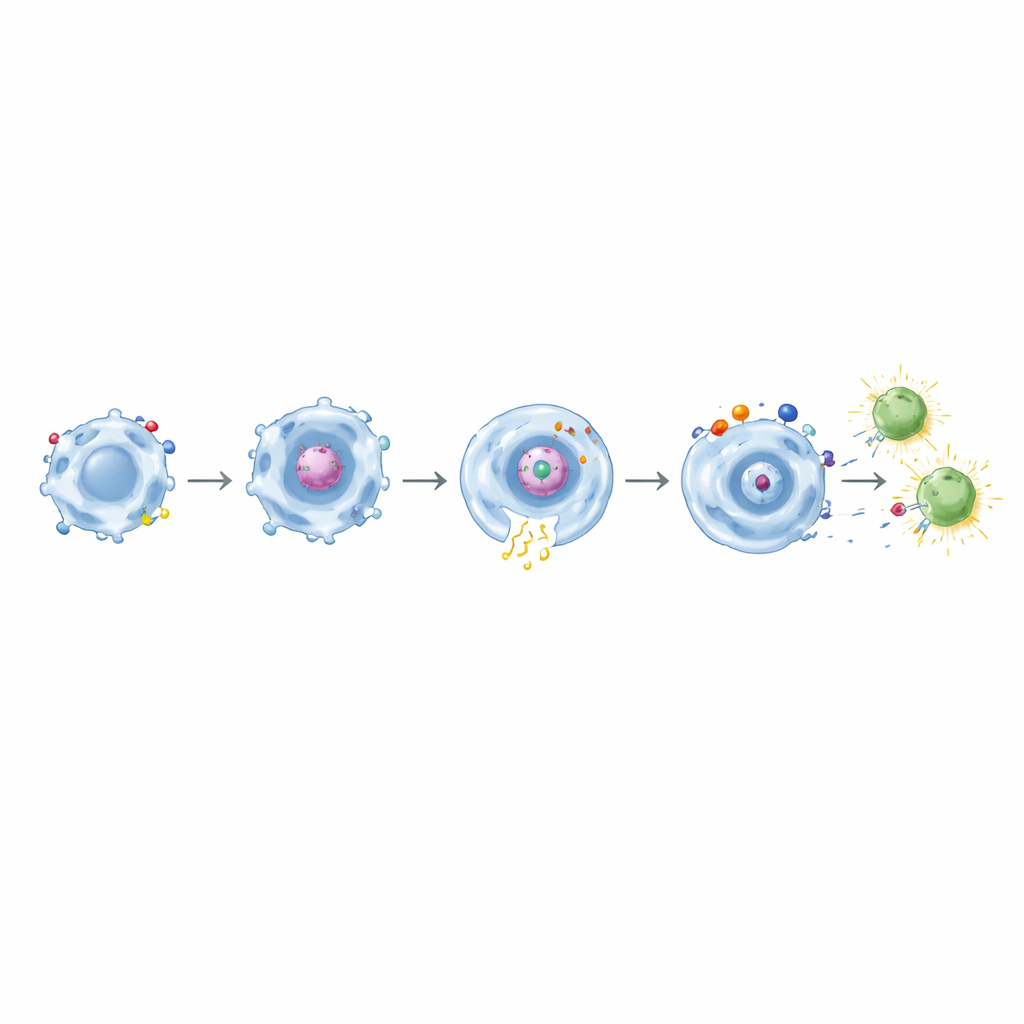
Vom Fressen zum T-Zell-Unterrichten
Wesentlich ist, dass Makrophagen mit CD32a-basierten CARs nach der Aufnahme des Spike-Proteins in der Lage waren, Gedächtnis-CD8-T-Zellen von zuvor gegen COVID-19 geimpften Personen zu aktivieren. Diese T-Zellen zeigten frühe Aktivierungsmarker und produzierten Effektormoleküle wie Interferon-γ und TNF-α. Der Effekt wurde noch stärker bei dualen CAR-Domänen, die CD32a mit CD11b, CD18 oder TLR4 kombinierten. Als ähnliche Konstrukte, die Mesothelin anvisieren, gegen gentechnisch veränderte Tumorzellen getestet wurden, zeigten sie erneut präzise, zielabhängige Phagozytose kombiniert mit verstärkter entzündlicher Signalgebung. Besonders die Kombination CD32a+TLR4 fiel als mächtiger "Gewebealarm" auf: Sie steigert am effektivsten die Zytokinsekretion und CD86 und bewahrt dabei dennoch die spezifische Tumoraufnahme.
Was das für künftige Behandlungen bedeuten könnte
Für Laien zeigt diese Studie, dass das Engineering von Makrophagen kein Einheitsproblem ist. Durch das Austauschen und Kombinieren interner Signalmodule können Forscher Zellen formen, die entweder auf effiziente Beseitigung krankhafter Zellen fokussiert sind oder eher wie Immunverstärker wirken, die das unterdrückende Tumorumfeld umgestalten und T-Zellen rekrutieren. CD32a-basierte CARs erwiesen sich als starke Grundlage für solche Entwürfe, übertrafen traditionelle T-Zell-Module in Makrophagen und funktionierten sowohl gegen virale als auch gegen Tumorziele. Obwohl diese Ergebnisse aus Labor-Modellen stammen und in primären menschlichen Zellen sowie im Tiermodell bestätigt werden müssen, liefern sie eine Blaupause für die nächste Generation von CAR-Makrophagen-Therapien, die durch die Verbindung von schneller Aufnahme und präziser T-Zell-Aktivierung solidere Tumoren und persistierende Infektionen besser bekämpfen könnten.
Zitation: Hong, J., Lee, S., Kim, Y. et al. Optimization of THP-1-CAR monocytes utilizing CD32a signaling phagocytosis for antigen-specific T cell activation. Sci Rep 16, 8175 (2026). https://doi.org/10.1038/s41598-026-39406-6
Schlüsselwörter: CAR-Makrophagen, CD32a-Signalgebung, Phagozytose, Immuntherapie solider Tumoren, T-Zell-Aktivierung