Clear Sky Science · de
Integration von Multi-Omics-Analysen identifiziert das DNA-Schadens-assoziierte Gen CLSPN als Biomarker bei Magenkrebs
Warum diese Forschung wichtig ist
Magenkrebs bleibt eine der weltweit tödlichsten Krebserkrankungen, vor allem weil er häufig spät entdeckt wird und verlässliche Frühwarnzeichen fehlen. Diese Studie untersucht die genetischen „Kratzspuren“, die bei DNA-Schäden entstehen, und identifiziert ein Gen namens CLSPN als vielversprechenden Marker, der Ärzten helfen könnte, Magenkrebs früher zu erkennen, seine Aggressivität besser einzuschätzen und Behandlungen gezielter anzupassen.
Auf der Suche nach Gefahrensignalen in Magen-Tumoren
Die Forschenden gingen von einer einfachen Annahme aus: Wenn DNA-Schäden zur Entstehung von Magenkrebs beitragen, könnten Gene, die mit dem Umgang solcher Schäden befasst sind, wichtige Hinweise darauf geben, wer erkrankt und wie sich die Krankheit entwickelt. Um das zu prüfen, kombinierten sie mehrere große Datensätze. Dazu gehörten Bulk-RNA-Sequenzdaten, die die durchschnittliche Genaktivität in Tumorproben messen; Einzelzell-RNA-Sequenzdaten, die Tausende einzelner Zellen separat untersuchen; und Spatial Transcriptomics, die Genaktivität auf dem Gewebeschnitt räumlich abbildet. Zusätzlich nutzten sie eine umfangreiche Liste von Genen, die bereits mit DNA-Schäden verknüpft sind. Mit diesen Ressourcen fragten sie, welche DNA-Schadens-assoziierten Gene am stärksten mit Magenkrebs und dem Überleben der Patienten korrelieren.
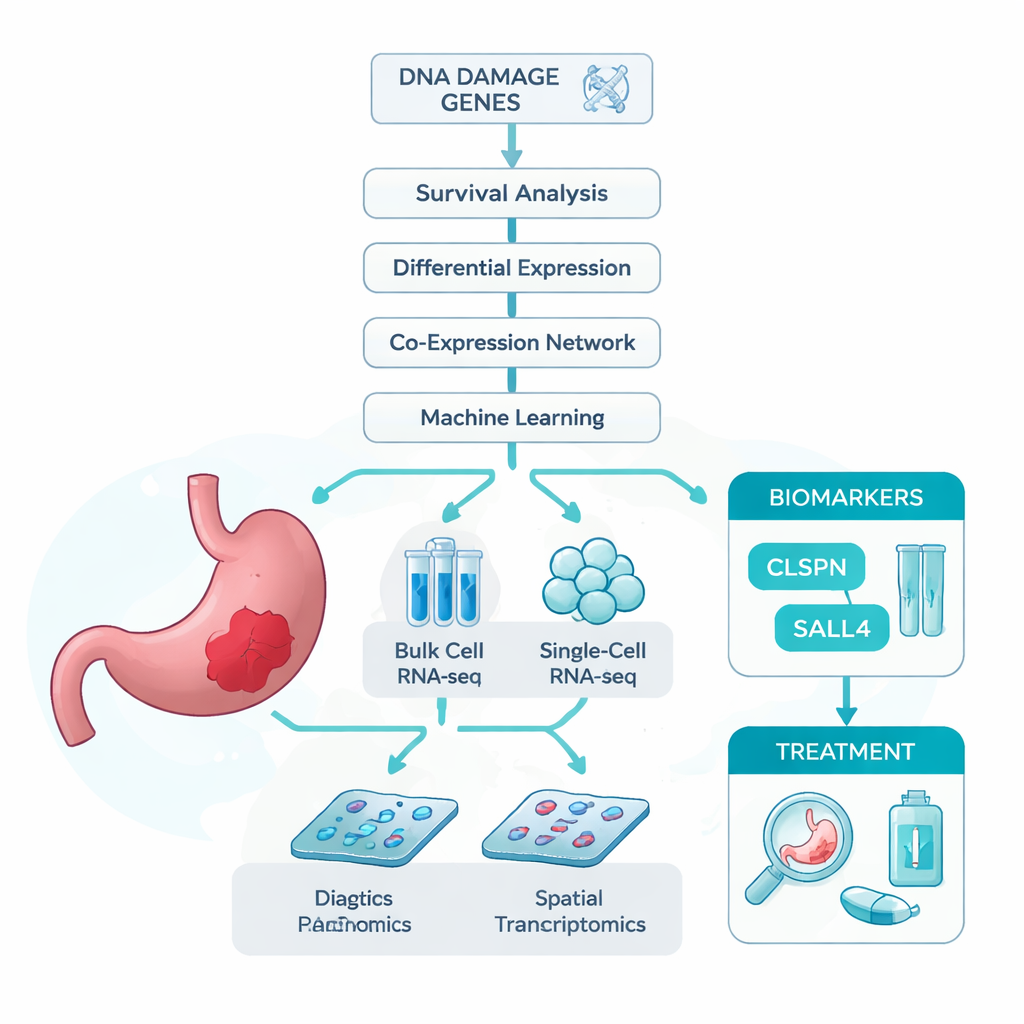
Mit klugen Algorithmen Schlüsselgene finden
Da in Krebs tausende Gene verändert sind, wandte das Team eine Reihe statistischer und Machine-Learning-Methoden an, um die Kandidatenliste einzuschränken. Zunächst filterten sie Gene, die sowohl in Tumoren fehlreguliert waren als auch klar mit der Überlebenszeit der Patienten zusammenhingen. Dann gruppierten sie Gene nach ähnlichen Expressionsmustern und verglichen diese Gruppen mit der Liste der DNA-Schadens-Gene. Dieser mehrstufige Auswahlprozess ergab 13 vielversprechende Kandidaten. Um zu ermitteln, welche davon am besten Tumor- von Normalgewebe unterscheiden, trainierten sie sieben verschiedene Machine-Learning-Modelle, die jeweils Gene nach ihrem Klassifikationsnutzen bewerteten. Über alle Modelle hinweg stachen zwei Gene — CLSPN und SALL4 — konstant hervor, mit Genauigkeiten nahe oder über 97 % und Flächen unter der ROC-Kurve über 0,96, was auf ein exzellentes diagnostisches Potenzial hindeutet.
Fokussierung auf CLSPN im Tumor
Unter den beiden Spitzenkandidaten erwies sich CLSPN als insgesamt am aufschlussreichsten, weshalb die Autoren dieses Gen detaillierter untersuchten. In Einzelzelldaten von mehr als 30.000 Zellen war CLSPN in Tumorzellen deutlich stärker exprimiert als in benachbarten normalen oder stützenden Zellen, was auf eine tumorspezifische Rolle hinweist. Die räumliche Kartierung von Gewebeschnitten zeigte ein ähnliches Bild: CLSPN-Expression konzentrierte sich in Bereichen, die Pathologen als Krebs erkannten. Teilt man Tumorzellen in „hohe CLSPN“- und „niedrige CLSPN“-Gruppen, zeigen die hohen Gruppen eine stärkere Aktivität in Signalwegen, die mit DNA-Replikation, Zellteilung und Reparatur verknüpft sind — Prozesse, die bei Über- oder Fehlregulierung unkontrolliertes Wachstum fördern können. Pseudotime-Analysen, die die Veränderung von Zellen entlang einer hypothetischen Zeitachse rekonstruieren, deuteten darauf hin, dass CLSPN-Werte mit dem Fortschreiten der Tumorzellen tendenziell ansteigen, was nahelegt, dass die Hochregulierung von CLSPN Teil der Entwicklung hin zu einem maligneren Zustand sein könnte.
Verbindungen zum Immunsystem und zur Therapieantwort
Die Studie untersuchte außerdem, wie CLSPN mit dem Tumorumfeld und möglichen Therapien zusammenhängt. Tumoren mit höherer CLSPN-Expression zeigten unterschiedliche Zusammensetzungen von Immunzellen, insbesondere Makrophagen sowie bestimmte T- und NK-Zell-Subtypen, was darauf hindeutet, dass CLSPN zur Ausbildung eines immunsuppressiven Umfelds beitragen könnte. Modellierungen der Arzneimittelempfindlichkeit legten nahe, dass Tumoren mit höherem CLSPN gegenüber mehreren Chemotherapie- und zielgerichteten Wirkstoffen empfindlicher sein könnten, da höhere CLSPN-Werte mit niedrigeren vorhergesagten Dosen zur Wachstumshemmung korrelierten. Wichtig ist, dass bei Färbungen realer Gewebeproben von 70 Patientinnen und Patienten die CLSPN-Proteinlevel in Krebsgewebe deutlich höher waren als im normalen Magengewebe und mit größeren Tumoren, tieferer Invasion, Lymphknotenbefall und kürzerem Gesamtüberleben verbunden waren.
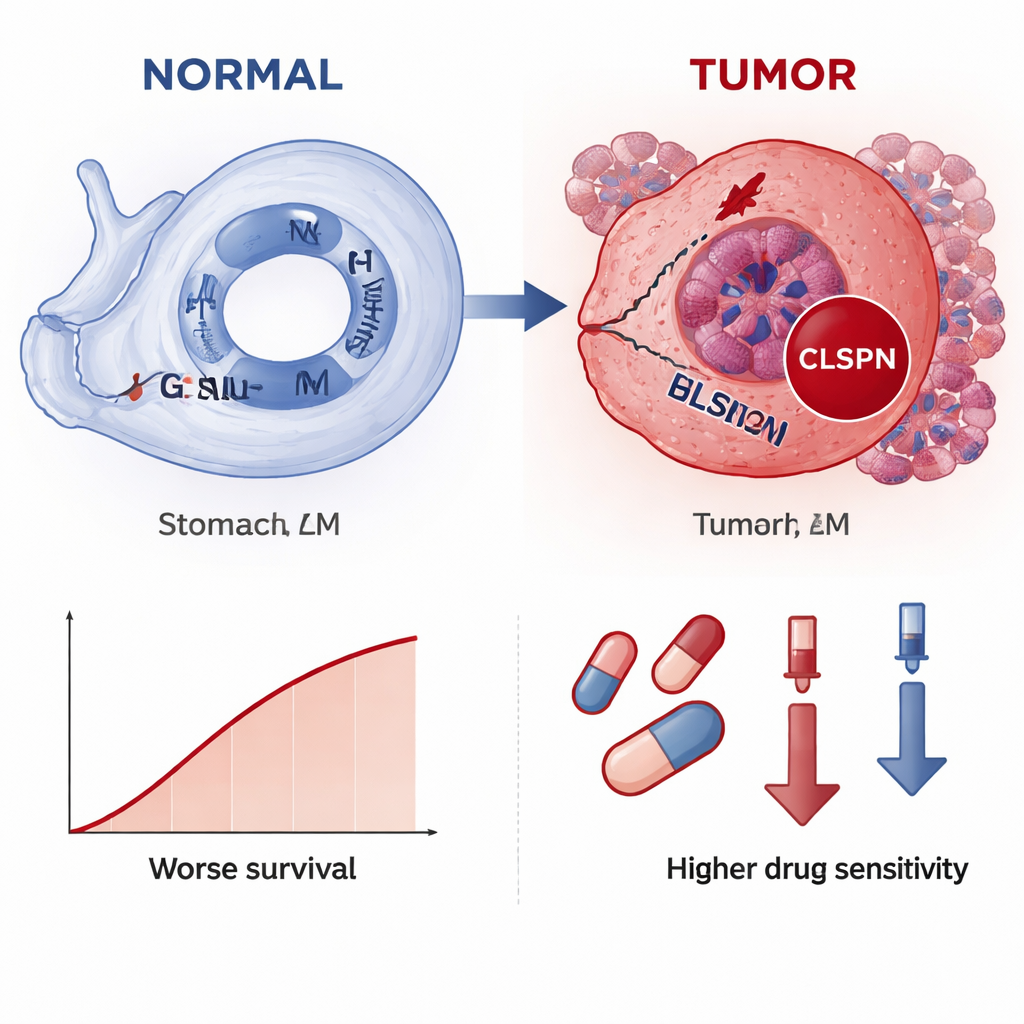
Was das für Patientinnen und Patienten bedeuten könnte
Vereinfacht gesagt legt die Studie nahe, dass CLSPN wie eine rote Warnleuchte für Magenkrebs wirkt: Es wird vor allem in Tumorzellen eingeschaltet, leuchtet bei fortgeschrittener Erkrankung stärker und signalisiert ein höheres Risiko für ungünstige Verläufe. Da CLSPN sowohl auf RNA-Ebene als auch mit standardmäßigen immunhistochemischen Färbemethoden nachweisbar ist, könnte CLSPN zu einem praktikablen Biomarker werden, um Pathologinnen und Pathologen bei der Bestätigung von Magenkrebs zu helfen, Patientengruppen nach Risiko zu stratifizieren und möglicherweise Therapieentscheidungen zu leiten. Obwohl vor einer routinemäßigen Anwendung noch weitere klinische Tests nötig sind, zeigt diese Arbeit, wie das Auslesen der Spuren von DNA-Schäden über mehrere Datenschichten hinweg neue Werkzeuge für eine frühere Diagnose und eine personalisiertere Behandlung von Magenkrebs zutage fördern kann.
Zitation: Ma, Q., Yang, X., Sun, N. et al. Integrating multi-omics analysis identifies DNA damage-related gene CLSPN as a biomarker in gastric cancer. Sci Rep 16, 7789 (2026). https://doi.org/10.1038/s41598-026-39387-6
Schlüsselwörter: Magenkrebs, DNA-Schaden, CLSPN, Biomarker, Einzelzell-Analyse