Clear Sky Science · de
Exzitatorische GABA-Rezeptoren formen die Organisation des Lokomotionskreises in C. elegans
Wie ein winziger Wurm eine Lehrbuchregel umschreibt
In Biologieunterricht wird die Gehirnchemikalie GABA meist als Bremse vorgestellt: Sie dämpft Neurone und hilft, die Aktivität in Grenzen zu halten. Diese Studie an dem winzigen Fadenwurm Caenorhabditis elegans stellt diese Regel auf den Kopf. Die Autorinnen und Autoren zeigen, dass GABA in diesem einfachen Tier auch wie ein Gaspedal wirken kann und bestimmte Motoneurone anregt, um präzises Rückwärtskriechen zu steuern. Indem sie nachverfolgen, welche Zellen welche Rezeptoren produzieren und wie diese Zellen verschaltet sind, offenbaren sie eine unerwartet clevere Strategie, mit der ein kleines Nervensystem aus einem begrenzten Satz von Bausteinen mehr Flexibilität herausholt.
Ein reiches Ensemble von Kanälen in einem einfachen Nervensystem
C. elegans besitzt nur 302 Neurone, kann aber eine überraschende Vielfalt an Verhaltensweisen ausführen, vom Erkunden und Entkommen bis zur Koordination von Fressen und Eiablage. Ein wesentlicher Teil dieser Vielseitigkeit beruht auf ligandengesteuerten Ionenkanälen – winzigen Proteinporen, die sich öffnen, wenn sie an Moleküle wie GABA oder Acetylcholin binden. Im Vergleich zu Menschen hat der Wurm eine unverhältnismäßig große Sammlung dieser Kanäle: insgesamt 102 lgc-Gene. Viele davon sind ungewöhnlich, reagieren auf unerwartete Liganden oder lassen positive statt negative Ladungen fließen. Darunter finden sich seltene GABA-Rezeptoren, die die Zellen, auf denen sie sitzen, erregen statt zu stillen. Bisher war unklar, wo diese speziellen Rezeptoren innerhalb der motorischen Schaltkreise eingesetzt werden, die die Körperbeugungen des Wurms steuern.
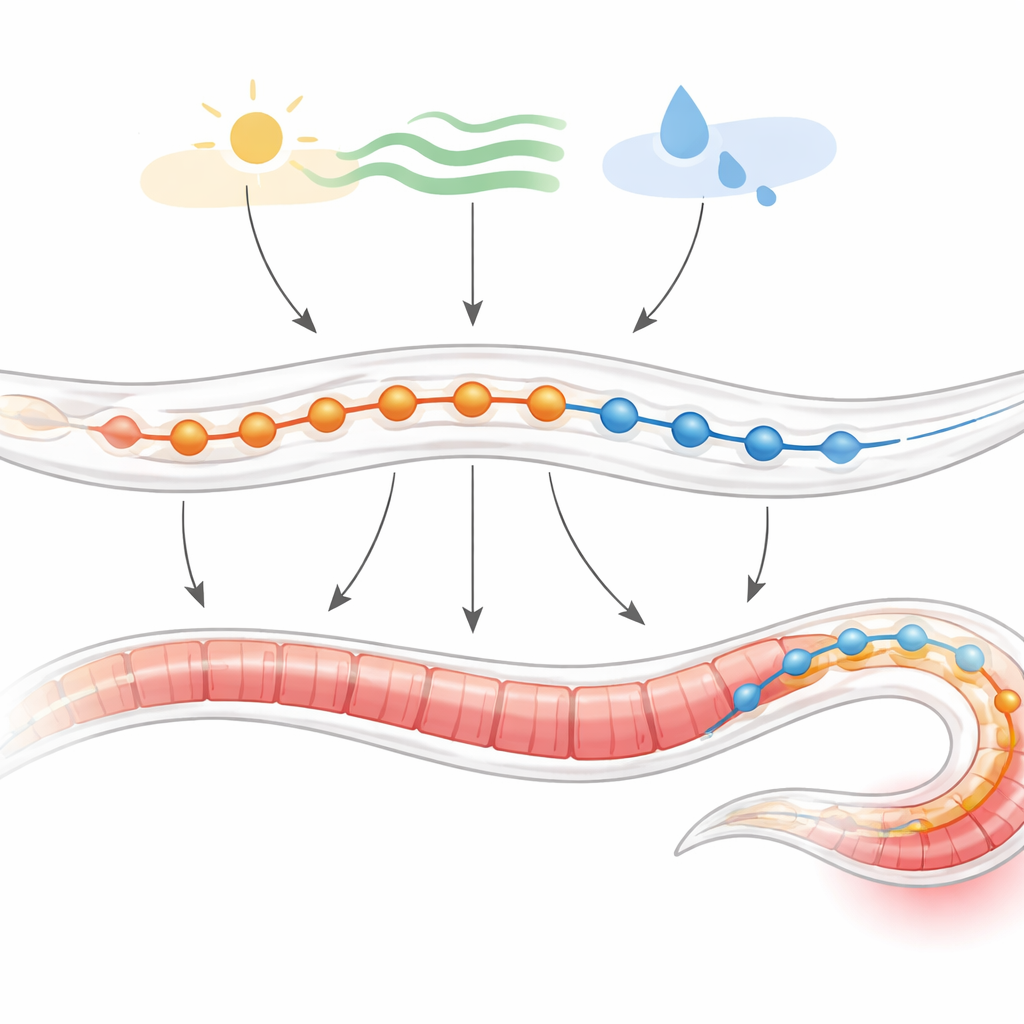
Die Hotspots der Bewegungssteuerung finden
Die Forschenden werteten große Einzelzell-RNA-Sequenzatlasse aus, die erfassen, welche Gene in einzelnen Neuronen des Wurm‑Nervensystems aktiv sind. Sie entdeckten, dass die lgc‑Familie insgesamt besonders in Motoneuronen aktiv ist und am stärksten in jenen, die rhythmische Körperwellen für das Kriechen erzeugen. Innerhalb dieser lokomotionsbezogenen Motoneurone stachen Gene für GABA‑Rezeptoren hervor. Ein genauerer Blick mit einer hochauflösenden Karte von Motoneuron‑Untertypen zeigte, dass GABA‑Rezeptoren in drei Schlüsselgruppen zu finden sind: A‑Typ‑Neurone, die Rückwärtsbewegung antreiben, B‑Typ‑Neurone, die Vorwärtsbewegung steuern, und D‑Typ‑Neurone, die GABA‑Signale liefern. Mehr als die Hälfte der Zellen in diesen Klassen trug mindestens ein GABA‑Rezeptor‑Gen, was darauf hindeutet, dass GABA eine breite und nuancierte Rolle bei der Formung der Bewegung spielt.
Exzitatorisches GABA konzentriert im Schwanz
Nicht alle GABA‑Rezeptoren verhalten sich gleich. Die meisten im Wurm sind klassische inhibitorische Rezeptoren, aber zwei, genannt EXP‑1 und LGC‑35, erlauben den Fluss positiver Ladung und erregen damit Neurone. Indem das Team jedes Motoneuron nach den exprimierten GABA‑Rezeptor‑Genen klassifizierte, fand es, dass viele A‑ und B‑Typ‑Neurone inhibitorische und exzitatorische Rezeptoren mischen, wodurch GABA je nach Kontext dämpfen oder verstärken kann. Ein auffälliges Muster zeigte sich bei den A‑Typ‑Neuronen, die das Rückwärtskriechen antreiben: Je weiter ein Neuron zum Schwanz hin liegt, desto wahrscheinlicher ist es, exzitatorische GABA‑Rezeptoren zu tragen. Besonders LGC‑35 und in den ganz hinteren Zellen EXP‑1 waren in diesen posterioren Neuronen angereichert, wobei sie sich häufig gegenseitig auszuweichen scheinen. Das erzeugt ein räumliches Gradientenmuster der Erregbarkeit entlang des Körpers, wobei der Schwanz darauf verdrahtet ist, besonders empfänglich für GABA zu sein.
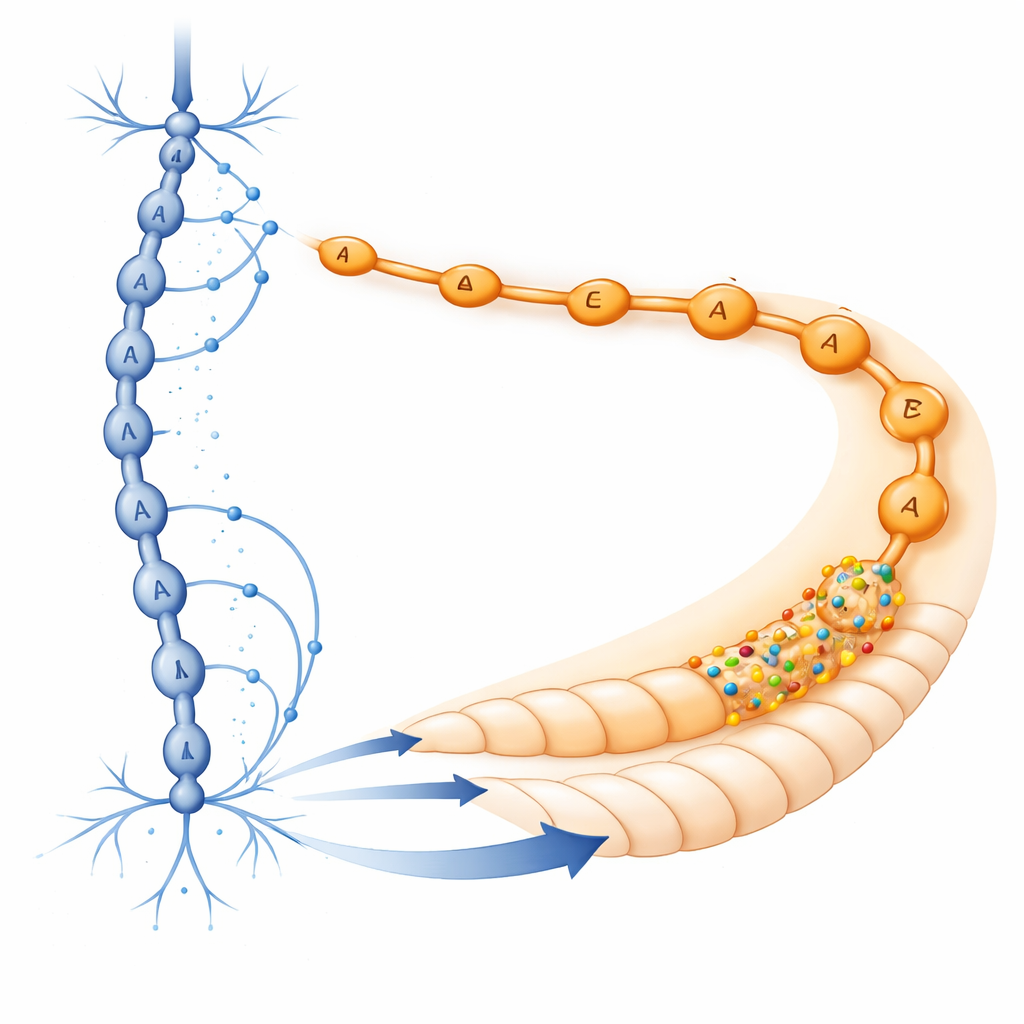
Das klassische Bild von GABA neu verdrahten
Um zu verstehen, wie dieses molekulare Muster in das tatsächliche Verschaltungsdiagramm des Wurms passt, griffen die Autorinnen und Autoren auf das vollständige, auf Elektronenmikroskopie basierende Connectom zurück. Sie konzentrierten sich auf die D‑Typ‑Neurone, die Hauptquellen der GABA‑Freisetzung im Lokomotionssystem. Diese Neurone bilden geordnete Ketten von Synapsen auf A‑ und B‑Typ‑Motoneuronen entlang des Körpers, wobei dorsale D‑Typ‑Zellen hauptsächlich mit A‑Typ‑Neuronen verbunden sind. Überlagert man diese anatomische Karte mit den Daten zur Rezeptorexpression, ergibt sich ein klares Bild: D‑Typ‑Neurone senden GABA an A‑Typ‑Neurone im Schwanzbereich, die mit exzitatorischen Rezeptoren vollgepackt sind. Frühere Arbeiten deuteten darauf hin, dass LGC‑35 auch GABA aufnehmen kann, das aus Synapsen diffundiert, wodurch seine Reichweite weiter vergrößert wird. Zusammengenommen deuten diese Befunde darauf hin, dass das lange als rein inhibitorisch betrachtete GABA‑System tatsächlich eine eingebaute exzitatorische Komponente trägt, die an spezifischen Orten eingesetzt wird.
Was das für die Richtungskontrolle der Bewegung bedeutet
Für Nicht‑Spezialistinnen und Nicht‑Spezialisten ist die Kernbotschaft, dass die Bewegungsrichtung dieses winzigen Wurms nicht durch simple Ein/Aus‑Schalter gesteuert wird, sondern durch ein sorgfältig angeordnetes Muster chemischer „Drehregler“ entlang des Körpers. Dasselbe Signalmolekül, GABA, kann einige Motoneurone verlangsamen und andere beschleunigen, je nachdem, welche Rezeptoren jede Zelle zeigt und wo sie entlang der Kopf‑Schwanz‑Achse sitzt. Indem exzitatorische GABA‑Rezeptoren in den rückwärtssteuernden Neuronen des Schwanzes konzentriert werden, scheint der Wurm seinen Schwanzbewegungen extra Schub und feine Kontrolle zu verleihen, beispielsweise bei schnellen Rückzugsbewegungen. Diese Arbeit legt ein allgemeineres Prinzip nahe: Selbst sehr kleine Nervensysteme können durch wiederholte Nutzung gängiger Chemikalien auf unterschiedliche Weise und durch Variation der Rezeptorplatzierung anspruchsvolle, richtungsspezifische Verhaltensweisen erreichen.
Zitation: Wang, X., Mizuguchi, K. & Hashimoto, K. Excitatory GABA receptors shape locomotor circuit organization in C. elegans. Sci Rep 16, 9407 (2026). https://doi.org/10.1038/s41598-026-39358-x
Schlüsselwörter: Fortbewegung von C. elegans, GABA-Rezeptoren, motorische Schaltkreise, Einzelzell-Transkriptomik, neuronales Connectom