Clear Sky Science · de
Mikrobiologische und rheologische Dynamik gemischter Biofilme, gebildet von Bakterien und eukaryotischen Viren
Verborgene Gemeinschaften an medizinischen Geräten
Viele Krankenhausinfektionen beginnen nicht mit einem einzelnen Erreger, sondern mit schleimigen, unsichtbaren Gemeinschaften, sogenannten Biofilmen, die Katheter und andere medizinische Geräte überziehen. Diese Studie stellt eine oft übersehene Frage mit großen Folgen für die Patientensicherheit: Was passiert, wenn sich nicht nur Bakterien, sondern auch für Menschen infektiöse Viren gemeinsam in solchen Biofilmen ansiedeln? Indem die Forschenden beobachten, wie sich ein verbreitetes Säugetiervirus in bakteriellen Biofilmen verhält, legen sie offen, wie diese klebrigen mikrobiellen Städte Viren heimlich schützen und ihr Verhalten verändern können.
Klebende Städte aus Mikroben
Biofilme sind wie mikroskopische Städte, die Mikroben auf feuchten Oberflächen errichten — Rohre, Steine, Zähne oder die in Patienten eingesetzten Plastikschläuche. Bakterien siedeln sich an, vermehren sich und produzieren eine klebstoffartige Matrix, die sie vor Austrocknung, Chemikalien und dem Immunsystem schützt. In Krankenhäusern bilden sich solche Biofilme häufig auf Harn- und intravenösen Kathetern, wo sie Blutbahninfektionen und Harnwegsinfektionen auslösen können, die schwer zu behandeln sind. Diese Biofilme enthalten meist viele verschiedene Arten und sogar verschiedene Reiche des Lebens, doch die meisten Untersuchungen konzentrieren sich allein auf Bakterien, sodass die Rolle von Viren weitgehend unerforscht bleibt.
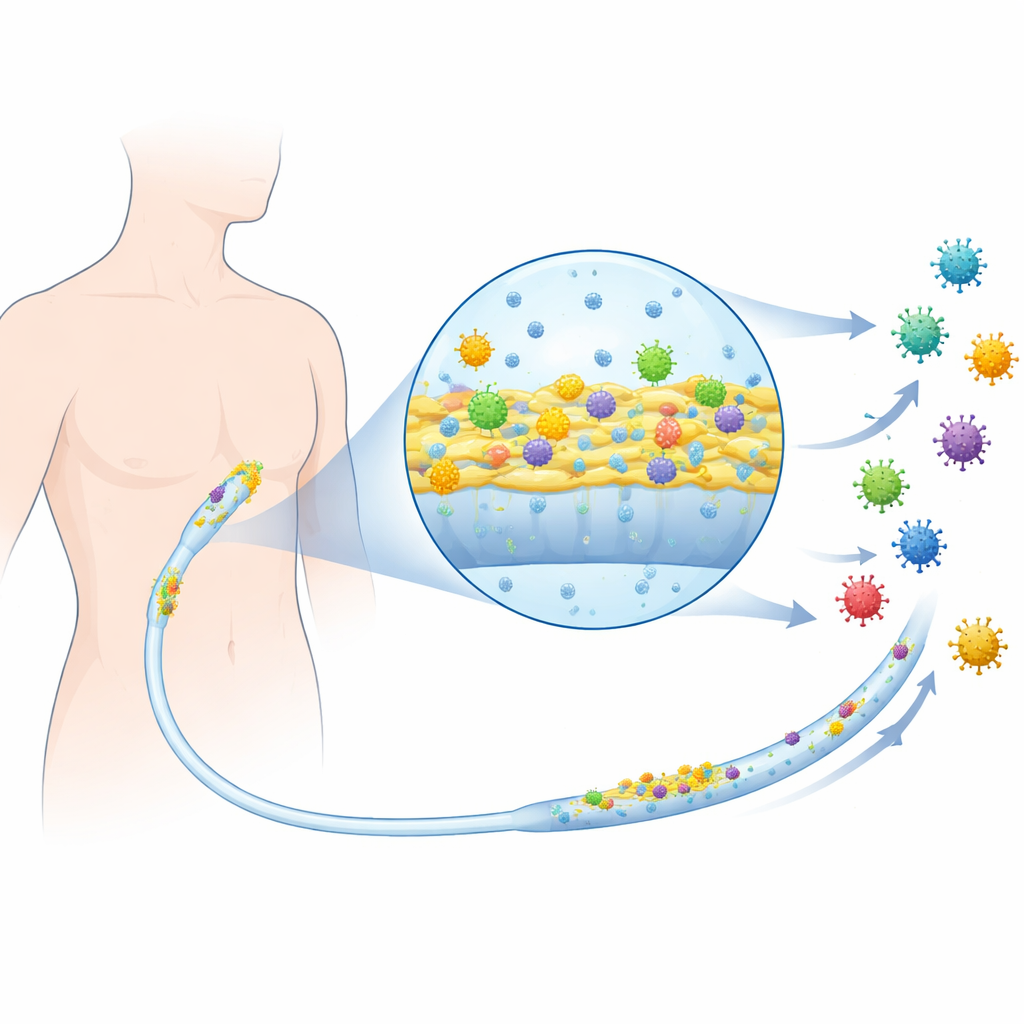
Ein Säugetiervirus in der Mischung
Das Team arbeitete mit klinischen Bakterienstämmen, die dafür bekannt sind, Katheter zu besiedeln, darunter uropathogene Escherichia coli aus Harnwegsinfektionen und andere Bakterien, die häufig bei zentralen Leitungsinfektionen vorkommen. Anschließend führten sie ein Säugetiervirus vom Typ Reovirus ein, ein gut untersuchtes, nicht umhülltes Virus, das tierische Zellen infiziert, als Stellvertreter für humane infektiöse Viren im weiteren Sinne. Zunächst überprüften sie, ob das Hinzufügen virushaltigen Materials das normale, frei schweifende bakterielle Wachstum beeinflusste. Bei vielen Stämmen wuchsen und überlebten die Bakterien genauso gut mit wie ohne Virus, was zeigte, dass das Virus die Bakterien nicht direkt tötete oder wie ein Antibiotikum wirkte.
Biofilme verändern die Beschaffenheit, nicht die Größe
Als sich Bakterien zu Biofilmen formten, wurde das Bild nuancierter. Bei den meisten Stämmen änderte sich die Gesamtmenge an Biofilm — gemessen mit einem Standardfarbstoff, der quantifiziert, wie viel Material eine Oberfläche überzieht — kaum in Anwesenheit des Virus. Einige Stämme produzierten jedoch leicht mehr oder weniger Biofilm, je nachdem, ob virale Präparate vorhanden waren, was auf stammspezifische Effekte hindeutet. Um über einfache Mengenmessungen hinauszugehen, entliehen sich die Forschenden Werkzeuge aus der Materialwissenschaft und maßen, wie „weich“ oder „steif“ jeder Biofilm war, ähnlich wie man die Textur eines Gels prüft. Sie fanden, dass jeder Bakterienstamm sein eigenes mechanisches Profil bildet. Wichtig ist, dass das Hinzufügen des Virus diese Biofilme je nach Stamm entweder versteifen oder aufweichen konnte: In einem E.-coli-Stamm machte das Virus die Matrix starrer, während bei einem Staphylococcus-epidermidis-Stamm das Virus zu einer schwächeren, nachgiebigeren Struktur führte.
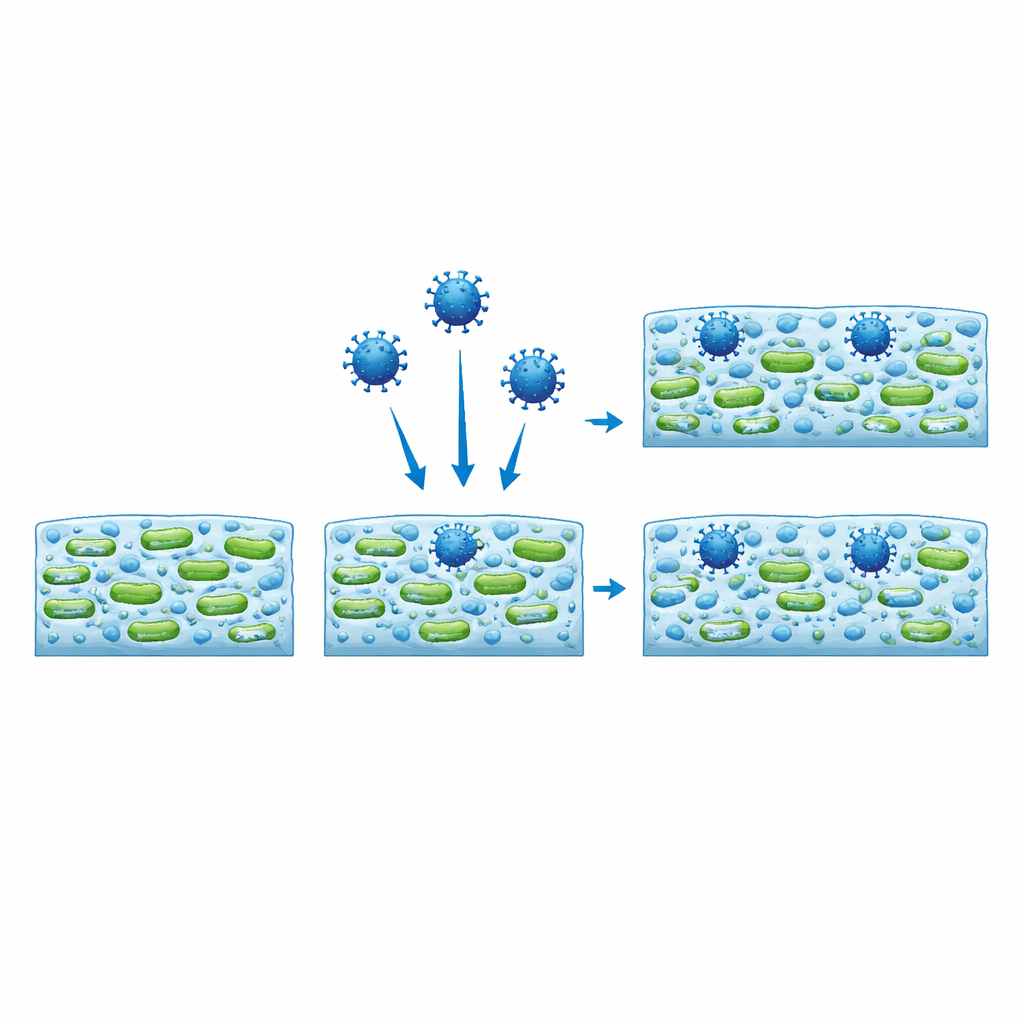
Viren finden Unterschlupf und behalten ihre Infektiosität
Mithilfe der Fluoreszenzmikroskopie markierten die Wissenschaftler Viruspartikel so, dass sie leuchteten, und verfolgten, wo sie innerhalb des Biofilms landeten. Anders als inerte, ähnlich große Kunststoffkügelchen, die überwiegend in dünn besiedelten Bereichen blieben und ausgespült wurden, drangen die Viren tief in die Matrix ein und gruppierten sich tendenziell dort, wo bakterielle Zellen am dichtesten waren. In einigen Fällen veränderte die Präsenz des Virus sogar die Gesamtgestalt des Biofilms, indem kompakte Klumpen in netzartige Strukturen verwandelt wurden oder umgekehrt — wiederum abhängig vom Bakterienstamm. Um zu testen, ob diese eingeschlossenen Viren noch gefährlich waren, gewannen die Autorinnen und Autoren Viren aus den Biofilmen zurück und setzten sie Säugetierzellen aus. Die zurückgewonnenen Viren blieben infektiös, obwohl sie zwei Tage lang in der bakteriellen Schleimschicht eingebettet gewesen waren.
Warum das für Patientinnen, Patienten und darüber hinaus wichtig ist
Für Laien lautet die Kernbotschaft: Biofilme auf medizinischen Geräten schützen nicht nur Bakterien vor Behandlung — sie können auch Viren verbergen und konservieren, die menschliche oder tierische Zellen infizieren. Die Studie zeigt, dass Viren sich in der bakteriellen Matrix einnisten, die Struktur des Biofilms subtil verändern und gleichzeitig voll dazu in der Lage bleiben, neue Zellen zu infizieren, sobald sie freigesetzt werden. Das legt nahe, dass Katheter und andere von Biofilmen überzogene Oberflächen als stille Reservoirs dienen könnten, in denen Viren persistieren, geschützt vor Austrocknung, Desinfektionsmitteln und immunologischer Abwehr. Das Verständnis dieser gemischten mikrobiellen Gemeinschaften könnte entscheidend sein, um bessere Materialien, Reinigungsstrategien und Therapien zu entwickeln, die sowohl bakterielle als auch virale Partner ansprechen, um hartnäckige, geräteassoziierte Infektionen zu reduzieren.
Zitation: Gao, J., Abriat, C., Laekas-Hameder, M. et al. Microbiological and rheological dynamics of mixed biofilms formed by bacteria and eukaryotic virus. Sci Rep 16, 8315 (2026). https://doi.org/10.1038/s41598-026-39314-9
Schlüsselwörter: Biofilme, Katheterinfektionen, Virus–Bakterien-Interaktionen, Reovirus, mikrobielle Gemeinschaften