Clear Sky Science · de
Identifizierung gemeinsamer Gene und ihrer zugehörigen microRNAs, Metaboliten und Signalwege bei ischämischem Schlaganfall und Epilepsie
Warum Schlaganfall und Anfälle zur gleichen Geschichte gehören
Schlaganfall und Epilepsie werden meist als getrennte Erkrankungen betrachtet: die eine unterbricht die Durchblutung des Gehirns, die andere verursacht plötzliche Ausbrüche abnormaler Hirnaktivität. Dennoch entwickeln viele Menschen, die einen ischämischen Schlaganfall überleben, später Anfälle — eine Komplikation, die als post-ischämische Epilepsie bezeichnet wird. Diese Studie stellt eine einfache, aber wichtige Frage: Teilen Schlaganfall und Epilepsie gemeinsame biologische Grundlagen in unseren Genen und der Blutchemie, und könnten diese geteilten Signale Ärzten helfen, Anfälle nach Schlaganfall vorherzusagen und womöglich zu verhindern?
Auf der Suche nach gemeinsamen Signalen im Blut
Um diese Verbindung zu untersuchen, nutzten die Forscher große öffentliche Datenbanken mit Blutproben von Menschen mit ischämischem Schlaganfall und von Menschen mit Epilepsie und verglichen diese mit gesunden Kontrollen. Statt sich auf einzelne Gene zu konzentrieren, verwendeten sie netzwerkartige Analysen, die Gene gruppieren, die dazu neigen, gemeinsam an- oder abgeschaltet zu werden. Aus Tausenden von Genen, die sich bei Patienten gegenüber Kontrollen unterschiedlich verhielten, bauten sie Cluster, die mit jeder Erkrankung verknüpft waren, und suchten dann nach Überschneidungen der beiden Karten. Das zeigte 38 Gene, die sich bei Schlaganfall und Epilepsie in ähnlicher Weise veränderten und auf gemeinsame Krankheitsmechanismen statt isolierte Zufälle hinweisen. 
Einschränkung auf einen potenziellen Schlüsselakteur
Dutzende gemeinsamer Gene zu finden, ist nur der erste Schritt; die Herausforderung besteht darin, diejenigen zu identifizieren, die am wichtigsten sind. Das Team untersuchte, wie diese 38 Gene mit anderen Proteinen in der Zelle interagieren, baute ein Protein‑Protein‑Netzwerk und nutzte mehrere mathematische Werkzeuge, um die einflussreichsten "Hub"‑Gene zu markieren. Drei traten hervor: IL10RA, CD2 und C3AR1. Als die Forscher testeten, wie gut die Aktivität jedes Gens Patienten von gesunden Personen in mehreren Datensätzen unterscheiden konnte, zeigten alle drei vielversprechende diagnostische Aussagekraft. Nur eines jedoch, C3AR1, war in unabhängigen Patientengruppen sowohl beim Schlaganfall als auch bei der Epilepsie konsistent erhöht und markiert damit das robusteste gemeinsame Signal.
Von Genen zu kleinen RNAs und Gehirnchemikalien
Gene wirken selten allein, daher fragte die Studie als Nächstes, was C3AR1 reguliert und wie es die Gehirnchemie beeinflussen könnte. Das Team betrachtete microRNAs — winzige RNA‑Fragmente, die die Genaktivität feinjustieren — und identifizierte eine bestimmte microRNA, genannt let‑7b‑5p, die mit sowohl Schlaganfall als auch Epilepsie verknüpft ist und voraussichtlich C3AR1 steuert. Parallel dazu führten sie eine ungerichtete Untersuchung kleiner Moleküle im Blut (Metabolomik) mit Proben von Kindern mit Epilepsie durch. Dabei fanden sie 139 Moleküle, die sich zwischen Kindern mit Epilepsie und gesunden Gleichaltrigen unterschieden. Als diese metabolischen Veränderungen auf bekannte biochemische Signalwege abgebildet wurden, tauchte C3AR1 wiederholt in Netzwerken auf, die mit der neuronalen Signalübertragung verbunden sind, insbesondere solchen, die den Neurotransmitter Acetylcholin betreffen, welcher die Kommunikation von Nervenzellen steuert.
Wie veränderte Gehirnsignale Anfälle fördern könnten
Indem sie Gen- und Metabolitendaten kombinierten, bauten die Forscher ein breiteres Netzwerk, das C3AR1 mit mehreren neuronalen Signalwegen verknüpft, darunter der synaptische Vesikelzyklus (wie Nervenzellen chemische Botenstoffe verpacken und freisetzen), cholinerge Signalweiterleitung (Wegstrecken, die von Acetylcholin gesteuert werden), geschmacksbezogene Signalwege und Wege, die mit Nikotin assoziiert sind. In Blutproben von Kindern mit Epilepsie waren die Acetylcholinspiegel reduziert, und C3AR1 lag an strategischen Stellen in den Signalwegen, an denen dieses Molekül wirkt. Die Autoren schlagen vor, dass Veränderungen der C3AR1‑Aktivität, möglicherweise gesteuert durch let‑7b‑5p, cholinerge Signalübertragung und die Freisetzung von Neurotransmittern an Synapsen stören könnten. Im Laufe der Zeit könnten solche Ungleichgewichte Hirnschaltkreise nach einem Schlaganfall reizbarer machen und sie in Richtung Anfällen treiben. 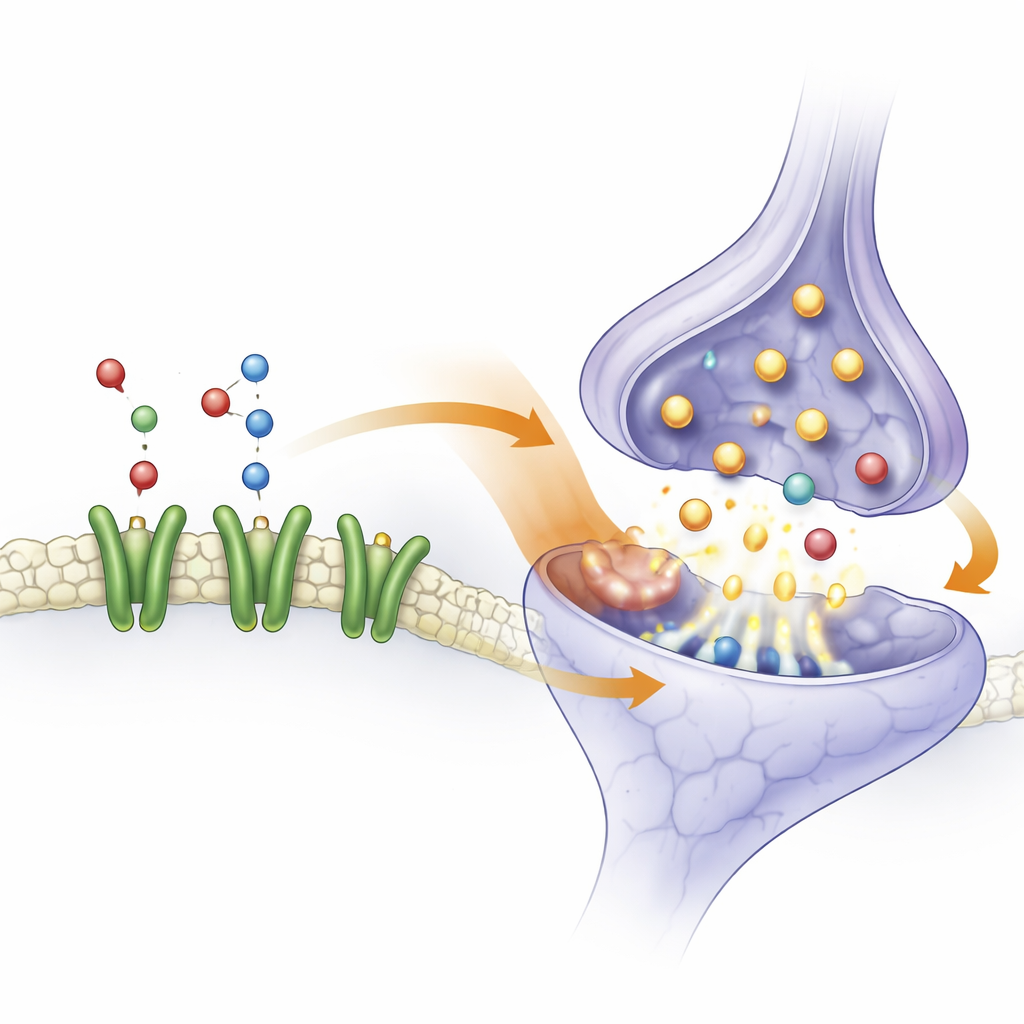
Was das für Patientinnen und Patienten bedeuten könnte
In der Summe deuten die Ergebnisse darauf hin, dass Schlaganfall und Epilepsie nicht nur klinisch verknüpft sind, sondern auch ein gemeinsames biologisches Gerüst teilen, zu dem das Gen C3AR1, seine regulatorische microRNA let‑7b‑5p und der Neurotransmitter Acetylcholin gehören. Obwohl diese Resultate hauptsächlich aus Datenanalysen und einer relativ kleinen Gruppe von Kindern mit Epilepsie stammen, eröffnen sie die Möglichkeit, dass blutbasierte Marker eines Tages helfen könnten, Schlaganfallüberlebende mit hohem Risiko für die Entwicklung von Anfällen zu identifizieren. Die Autoren warnen, dass C3AR1 allein wahrscheinlich kein perfekter Prädiktor ist; stattdessen könnten Panels aus Genen, microRNAs und Metaboliten die zuverlässigsten diagnostischen Werkzeuge liefern. Dennoch weist diese Arbeit in Richtung einer Zukunft, in der ein einfacher Bluttest personalisierte Überwachungs- und Behandlungsstrategien für Menschen ermöglichen könnte, die im Schatten von Schlaganfall und Epilepsie leben.
Zitation: Chen, Y., Man, S., Li, Q. et al. Identifying the shared genes and their related microRNAs, metabolites, and pathways in ischemic stroke and epilepsy. Sci Rep 16, 8166 (2026). https://doi.org/10.1038/s41598-026-39299-5
Schlüsselwörter: ischämischer Schlaganfall, post-ischämische Epilepsie, Biomarker, C3AR1, Metabolomik