Clear Sky Science · de
Integrativer Rahmen für Krebserkennung über integro-differenzielle Gleichungen mit Deep‑Learning‑Techniken
Warum intelligentere Untersuchungen wichtig sind
Krebs früh zu entdecken kann Leben retten, doch das Lesen medizinischer Aufnahmen wie Mammographien ist schwierig, zeitaufwendig und fehleranfällig. Ärztinnen und Ärzte müssen schwache Krankheitsmuster von normalem Gewebe und Bildrauschen unterscheiden, oft unter hohem Zeitdruck. Dieses Paper stellt einen neuen Ansatz vor, der helfen soll: Es verwandelt komplexe Brustbilder in einfachere eindimensionale Signale und kombiniert dann Mathematik und künstliche Intelligenz, um zu entscheiden, ob wahrscheinlich Krebs vorliegt. Ziel ist es nicht, Ärztinnen und Ärzte zu ersetzen, sondern ihnen klarere, verlässlichere Hinweise zu geben, die in jeder Aufnahme verborgen sind.
Bilder in Signale umwandeln
Die Autoren beginnen damit, die Repräsentation eines medizinischen Bildes neu zu denken. Statt eine Mammographie als großes Pixelraster zu behandeln, wandeln sie sie in ein einzelnes, linienähnliches Signal um, das zusammenfasst, wie sich die Helligkeit über die Brust verändert. Zuerst wird das Bild bereinigt: in Graustufen konvertiert, entrauscht und die Intensität ausgeglichen, sodass dunkle und helle Bereiche vergleichbar sind. Kanten und Texturen werden mit Standardfiltern betont, und das Gesamtmuster von Hell und Dunkel wird hinsichtlich seiner Frequenzen analysiert (ähnlich der Aufteilung von Audio in Bass und Höhen). Dann werden Pixelwerte zeilen- oder spaltenweise gemittelt, um eine glatte eindimensionale Kurve zu erzeugen. Spitzen in dieser Kurve spiegeln dichte Gewebsbereiche oder verdächtige Regionen wider; Täler entsprechen leereren Bereichen. Zwar gehen einige feine Details verloren, doch entsteht ein kompaktes Signal, das die für die Diagnose wichtigsten großräumigen Strukturen bewahrt. 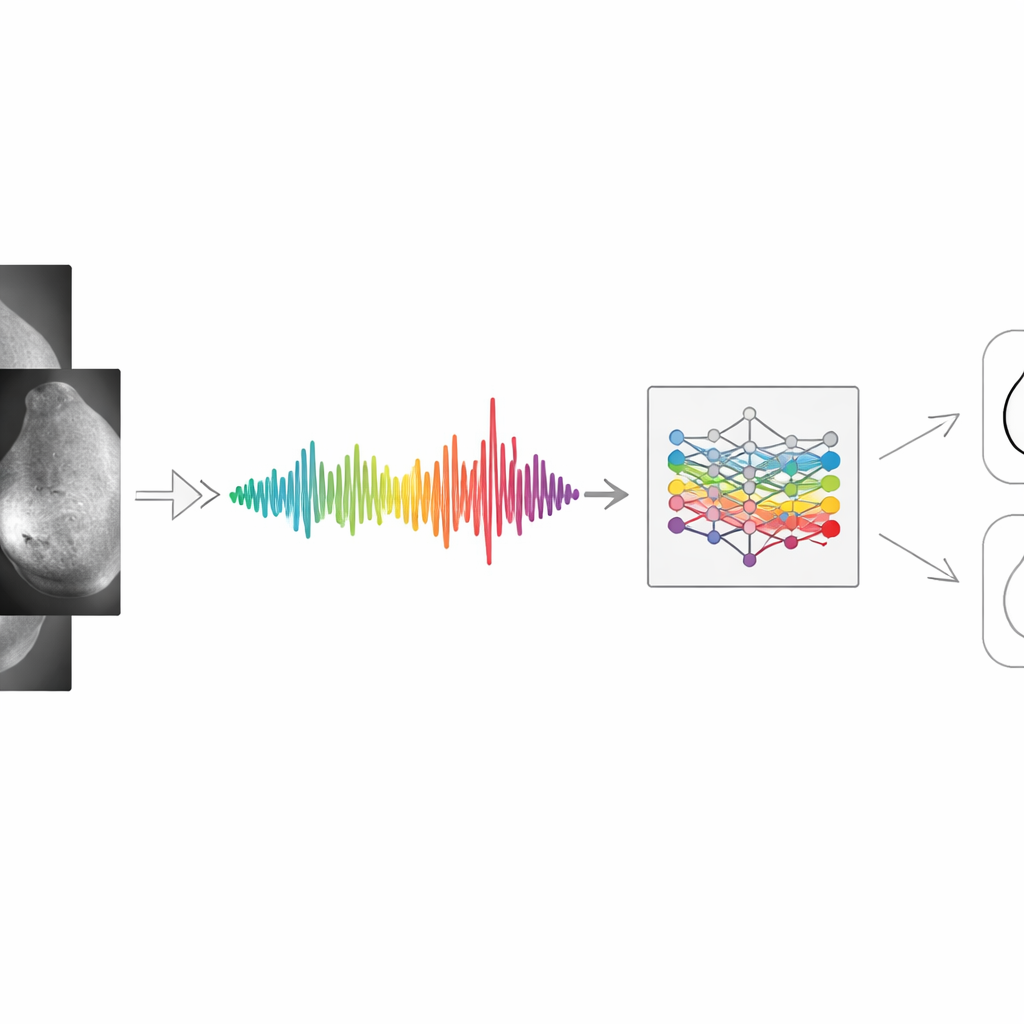
Ein biologischer Layer mit Gleichungen
Viele aktuelle Deep‑Learning‑Systeme arbeiten direkt auf Bildern und werden oft als „Black Boxes“ kritisiert, weil sie wenig Einsicht darin geben, wie Tumore tatsächlich reagieren oder wachsen. Um dem entgegenzuwirken, integrieren die Autoren mathematische Modelle des Tumorwachstums in ihre Signal‑Pipeline. Sie verwenden integro‑differenzielle Gleichungen — Gleichungen, die beschreiben, wie sich etwas über die Zeit verändert und gleichzeitig seine Vergangenheit berücksichtigt —, um nachzuahmen, wie Krebszellen sich vermehren, ausbreiten und Blutversorgung anziehen. Diese Gleichungen enthalten Terme für Wachstumsraten, Raumbegrenzungen durch Crowding, Zellbewegung und die Bildung neuer Blutgefäße. Indem sie simulieren, wie sich ein Tumor entwickeln und das Helligkeitsmuster in einer Mammographie beeinflussen könnte, erzeugt das Framework zusätzliche Merkmale, die in bekannter Biologie verankert sind und nicht nur in reiner Mustererkennung. Diese angereicherten Signale sollen die abschließenden Vorhersagen für Klinikpersonal interpretierbarer machen.
Ein kompaktes neuronales Netz zum Entscheiden
Sobald das Bild in ein mathematisch angereichertes Signal überführt ist, übernimmt ein schlankes eindimensionales Faltungsnetzwerk (CNN) die eigentliche Klassifikation. Dieses Netz schiebt kleine Filter entlang des Signals, um aussagekräftige Formen zu erkennen — scharfe Sprünge, sanfte Rampen oder wiederkehrende Wellen —, die auf abnormales Gewebe hindeuten können. Das Modell wird mit öffentlich verfügbaren Mammographie‑Datensätzen (INbreast und MIAS) trainiert; die Daten werden in Trainings-, Validierungs- und Test‑Teilmengen aufgeteilt, um Overfitting zu vermeiden. Die Autoren augmentieren die Signale und stimmen die Modelleinstellungen sorgfältig ab, um die Robustheit zu erhöhen. Um die Black Box weiter zu öffnen, wenden sie Erklärbarkeits‑Werkzeuge an, die hervorheben, welche Teile des Signals die Entscheidung am stärksten beeinflusst haben, und verknüpfen diese zurück zu Regionen im Originalbild, in denen sich Gewebedichte oder Kanten auffällig verändert haben. 
Wie gut es in der Praxis funktioniert
Bei Tests an diesen realen Mammographie‑Sammlungen unterschied das integrative Framework krebsartige von nicht krebsartigen Fällen in etwa 96,4 % der Fälle korrekt und übertraf damit Standard‑CNNs, Support‑Vector‑Machines, Entscheidungsbäume und mehrere moderne Deep‑Learning‑Baselines. Es zeigte außerdem hohe Sensitivität, das heißt die meisten Krebserkrankungen wurden erfolgreich erkannt, sowie starke Spezifität, sodass gesunde Patientinnen seltener fälschlich markiert wurden. Da das System auf 1D‑Signalen statt auf kompletten Bildern arbeitet, benötigt es weniger Speicher und kann Vorhersagen schneller liefern als viele rechenintensive bildbasierte Netze — ein Vorteil für den Einsatz in vollen Kliniken oder auf bescheidener Hardware. Die zusätzliche mathematische Modellierung scheint die relevanten Merkmale zu schärfen und die Genauigkeit zu verbessern, ohne extreme Rechenkosten zu verursachen.
Wohin das als Nächstes führen könnte
Die Autoren schließen, dass die Kombination aus Bild‑zu‑Signal‑Umwandlung, mathematischen Tumorwachstumsmodellen und Deep Learning einen vielversprechenden Weg zu genaueren und besser verständlichen Screening‑Werkzeugen bietet. Ihr Ansatz befindet sich noch in einem frühen Stadium: Er wurde hauptsächlich an Brustaufnahmen validiert, und bei der Signal‑Transformation können manche feingranularen visuellen Details verloren gehen. Zukünftige Arbeiten werden die Methode an anderen Krebsarten testen, reichhaltigere Erklärungen für Ärztinnen und Ärzte hinzufügen und zusätzliche Daten wie Gewebeschnitte, klinische Marker und genetische Informationen integrieren. Mit breiterer Validierung könnte diese art von mathematisch informierter KI schließlich Echtzeit‑Entscheidungssysteme unterstützen, die Radiologinnen und Radiologen helfen, Krebs früher und mit größerer Sicherheit zu erkennen.
Zitation: Gopisairam, T., Thota, S. & Bikku, T. Integrative framework for cancer detection via integro-differential equations using deep learning techniques. Sci Rep 16, 9714 (2026). https://doi.org/10.1038/s41598-026-39283-z
Schlüsselwörter: Krebserkennung, medizinische Bildgebung, Deep Learning, mathematische Modellierung, Mammographie der Brust