Clear Sky Science · de
Ein Polymerphysik-Modell des Interphasenkernels für radiobiologische Simulationen
Warum die Form unserer DNA-Heimat wichtig ist
Strahlung ist in der Medizin ein zweischneidiges Schwert: Sie kann Krebszellen abtöten, aber auch gesundes Gewebe schädigen. Im Zentrum beider Risiken und Chancen steht unsere DNA, dicht verpackt im Zellkern. Dieser Artikel zeigt, wie ein detailliertes, physikbasiertes 3D-Modell dieser nukleären "DNA-Stadt" Forschern helfen kann, vorherzusagen, wie Strahlung Chromosomen bricht und fehlerhaft wieder zusammenfügt – mit potenziellen Vorteilen für Krebstherapie und Einschätzungen des Strahlenrisikos im Weltraum.
Das Genom als lebendige Struktur sehen
In jeder menschlichen Zelle sind zwei Meter DNA auf nur wenige Mikrometer im Kern aufgefaltet. Diese Faltung ist nicht zufällig: Jedes Chromosom besetzt tendenziell sein eigenes Territorium, das weiter in Nachbarschaften und Schleifen-Domänen unterteilt ist. Neue experimentelle Werkzeuge wie Super-Resolution-Mikroskopie und Hi-C-Kontaktkarten haben dieses komplexe 3D-Layout mit bemerkenswerter Detailtreue offenbart. Dennoch behandeln die meisten Strahlungsmodelle DNA weiterhin als vereinfachtes Geflecht von Linien oder idealisierte Schleifen und übersehen diese höher geordnete Organisation. Die Autoren wollten ein Ganzkern-Modell bauen, das respektiert, was Biologen über die reale Chromatin-Architektur wissen, und gleichzeitig schnell genug ist, um auf gewöhnlichen Laborrechnern zu laufen.
Aufbau eines virtuellen Kerns mit Polymerphysik
Das Team modellierte Chromosomen als flexible Ketten und griff auf Konzepte der Polymerphysik zurück, dem gleichen Fachgebiet, das zur Beschreibung von Kunststoffen und weichen Materialien dient. Sie teilten das Problem in drei Relaxationsstadien, um die enormen Rechenkosten zu bändigen. Zuerst verteilten sie große Bausteine, sogenannte Chromatin-Domänen, im Kern, ließen diese sich gegenseitig abstoßen, entlang ihrer Längen strecken und zu größeren Subkompartimenten clustern. Zweitens zoomten sie in jede Domäne hinein, um die feineren Chromatinfasern zu legen, einschließlich geschleifter Bereiche, die durch Bindungsproteine zusammengehalten werden. Drittens ließen sie alle Fasern erneut frei innerhalb der Kernbegrenzung interagieren, um eine realistische Endkonfiguration zu erreichen. Durch diese Aufteilung und den Einsatz hierarchischer Suchalgorithmen und paralleler Rechenverfahren reduzierten sie die Laufzeit von unrealistischen vier Monaten auf etwa drei Stunden pro virtuellem Kern auf einer 64-Kern-Workstation.
Von Strahlungsspuren zu DNA-Brüchen und Reparaturen
Sobald der virtuelle Kern aufgebaut war, legten die Autoren detaillierte Strahlungsspuren aus Geant4-DNA-Simulationen darüber. Sie nutzten eine hierarchische Suche, um für jedes Ionisationsereignis zu bestimmen, welche Chromatin-Domäne, welcher Faserabschnitt und schließlich welches Nukleotid am nächsten lag, ohne jemals alle zehn Milliarden Nukleotidpositionen im Speicher zu halten. Stattdessen behielten sie eine wiederverwendbare Chromatin-Vorlage und führten geschickte Koordinatentransformationen in Echtzeit durch. Ionisationen im DNA-Rückgrat wurden als Strangbrüche gewertet, und nahe beieinanderliegende Brüche auf gegenüberliegenden Strängen wurden zu Doppelstrangbrüchen zusammengefasst. Um die Reparaturmaschinerie der Zelle zu imitieren, führten die Autoren eine distanzbasierte Wiederverknüpfungsregel ein: freie DNA-Enden, die nahe beieinander liegen, reihenwahrscheinlich eher wieder zusammen. Wiederverknüpfungsentscheidungen wurden schrittweise getroffen, bis alle Enden entweder gepaart oder unrepariert verblieben waren, wodurch sowohl korrekte Reparaturen als auch fehlerhafte Verknüpfungen rekonstruiert wurden.
Beschädigte Chromosomen mit Netzwerklogik sortieren
Nach dieser virtuellen Reparatur enthielt der Kern eine Mischung aus wiederzusammengesetzten Chromosomen und übrig gebliebenen Fragmenten. Um zu klassifizieren, was geschehen war, übersetzten die Autoren das reparierte Genom in einen ungerichteten Graphen: Chromosomensegmente wurden zu Kanten, ihre Enden und Bruchpunkte zu Knoten. Mithilfe eines Standard-Algorithmus zur Bestimmung zusammenhängender Komponenten konnten sie automatisch jedes neue chromosomeähnliche Objekt rekonstruieren und wichtige Merkmale zählen, wie die Anzahl der Zentromere (Anheftungspunkte für die Zellteilung) und Telomere (natürliche Enden). Daraus identifizierten sie Dicentrics (Chromosomen mit zwei Zentromeren), Ringe und Deletionen. Sie verglichen ihre Simulationen mit klassischen Experimenten an menschlichen Hautzellen, die Gammastrahlung und Alphateilchen ausgesetzt waren, und fanden, dass die Gesamtzahl der Chromosomenaberrationen innerhalb von etwa 20 % der gemessenen Werte lag – eine erhebliche Verbesserung gegenüber früheren Modellen.
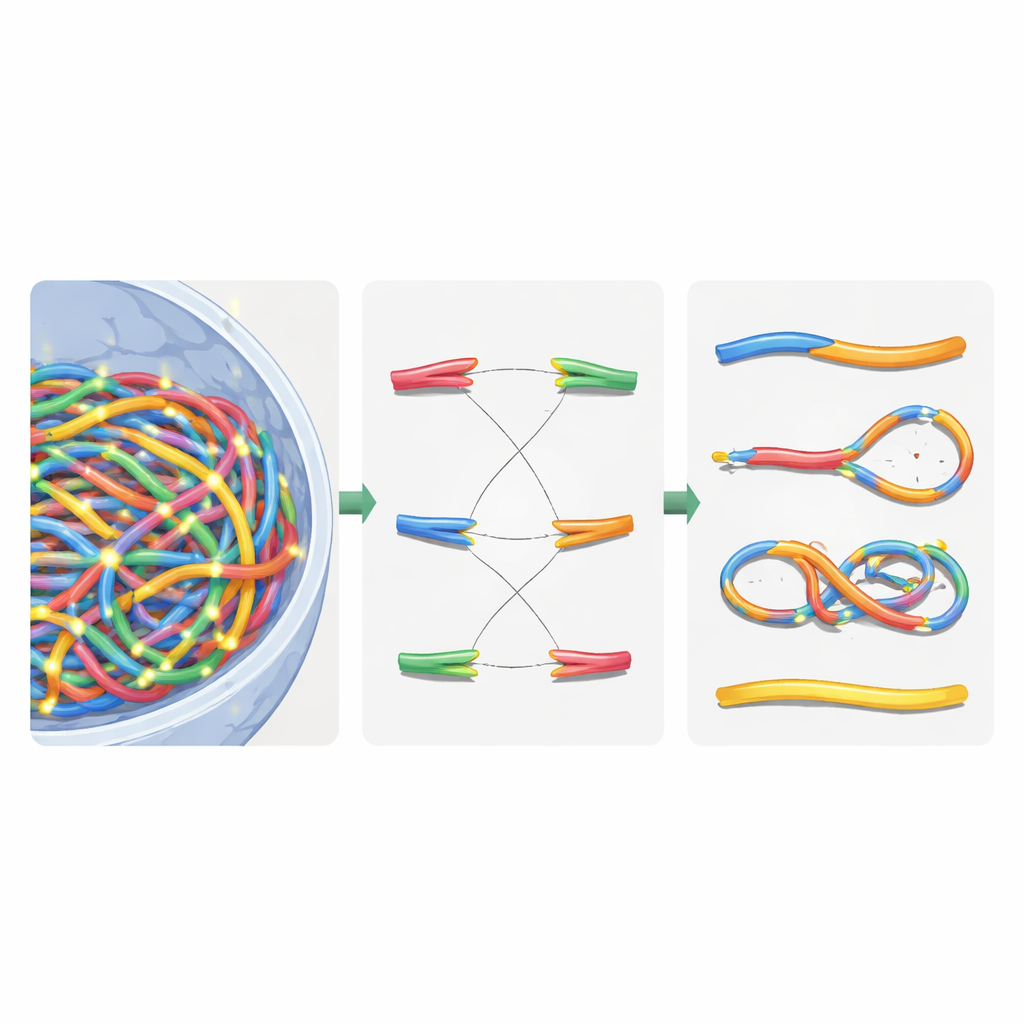
Was das für Patienten und Astronauten bedeutet
Vereinfacht gesagt zeigt diese Arbeit, dass der "Ort", an dem DNA im Kern liegt, und die Art ihrer Faltung stark beeinflussen, wie sich Strahlenschäden zu gefährlichen Chromosomenveränderungen aufsummieren. Durch die Kombination realistischer 3D-Genom-Architektur, effizienter physikbasierter Simulationen und graphbasierter Auswertung beschädigter Chromosomen schlagen die Autoren eine leistungsfähige Brücke zwischen Strukturbiologie und Radiobiologie. Sie argumentieren, dass zukünftige Verfeinerungen – etwa detaillierte Reparaturzeitpunkte und der Einsatz von Ganzgenom-Sequenzierungsdaten – diesen Ansatz noch besser darin machen könnten, die biologische Wirkung energiereicher Teilchen vorherzusagen, die in der Krebstherapie eingesetzt oder im tiefen Weltraum angetroffen werden. Letztlich könnten bessere Modelle der DNA-Heimat in unseren Zellen dazu beitragen, sicherere und wirksamere Strahlenbehandlungen zu entwickeln und unser Verständnis langfristiger Strahlenrisiken zu schärfen.
Zitation: Zhao, M., Huang, G., Xu, Z. et al. A polymer physics model of the interphase cell nucleus for radiobiological simulations. Sci Rep 16, 7913 (2026). https://doi.org/10.1038/s41598-026-39234-8
Schlüsselwörter: strahlungsinduzierte DNA-Schäden, 3D-Architektur des Chromatins, Chromosomenaberrationen, Polymerphysik-Modellierung, Teilchentherapie