Clear Sky Science · de
KI-gestützte Diagnose des akuten Aortensyndroms basierend auf multimodaler Informationsfusion
Warum das für Menschen mit Brustschmerzen wichtig ist
Das akute Aortensyndrom ist ein medizinischer Notfall, bei dem die Hauptschlagader des Körpers plötzlich einreißen kann und unbehandelt innerhalb weniger Stunden zum Tod führen kann. Seine Symptome ähneln jedoch oft einem Herzinfarkt, Muskelzerrung oder sogar Verdauungsbeschwerden, weshalb es notorisch leicht fehlzuinterpretieren ist. Diese Studie beschreibt ein neues System der künstlichen Intelligenz, das CT-Scans und Blutwerte kombiniert, um Ärzten zu helfen, diese stillen Arterienkatastrophen früher und genauer zu erkennen und Grenzfälle zu markieren, die eine zusätzliche Prüfung erfordern.
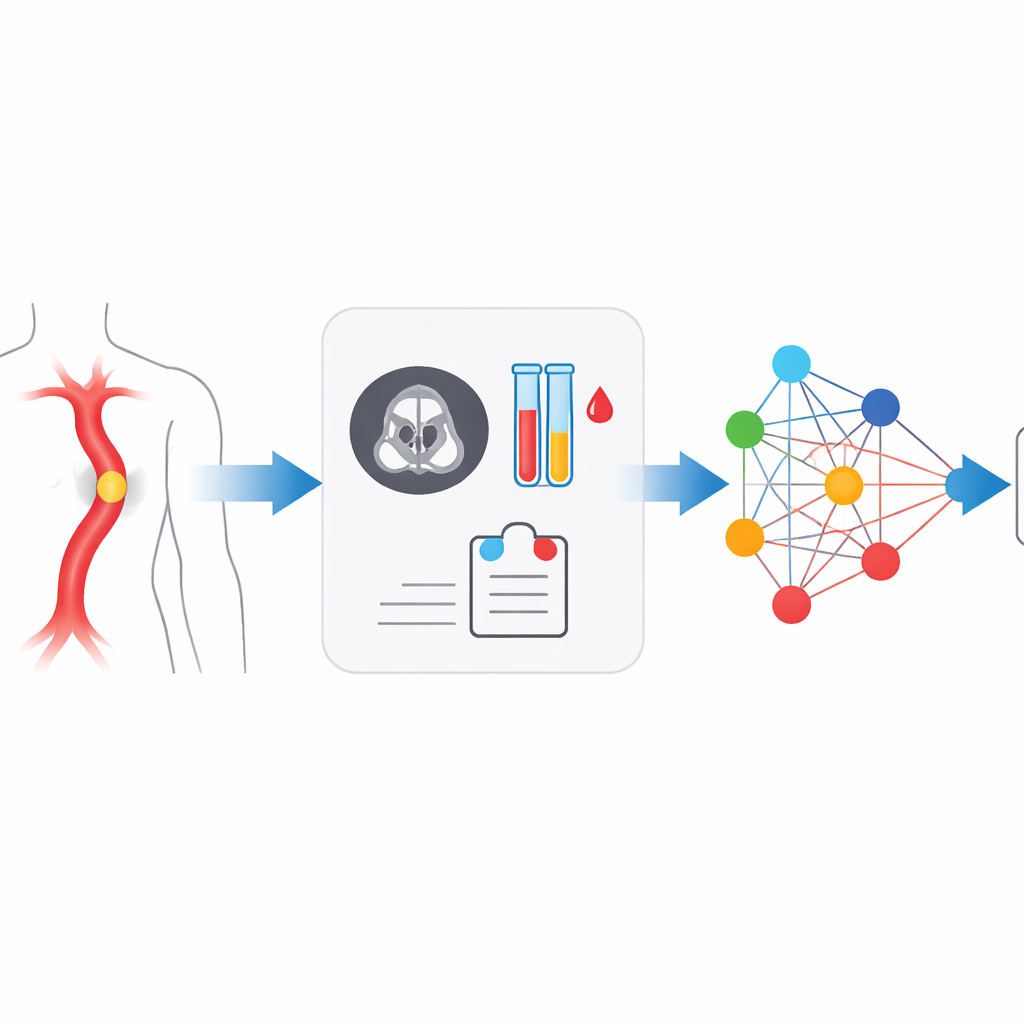
Ein gefährlicher Riss, der offen sichtbar bleibt
Das akute Aortensyndrom (AAS) umfasst mehrere verwandte Probleme in der Aortenwand, wie die klassische Dissektion, intramurales Hämatom und penetrierende Ulzera. Allen gemeinsam ist eine ähnliche Gefahr: Blut dringt in oder durch die Gefäßwand, was schnell zu Ruptur oder zum Verlust der Durchblutung lebenswichtiger Organe führen kann. Das Risiko ist in den ersten ein bis zwei Tagen nach Symptombeginn am höchsten, wenn die Sterblichkeit ohne rasche Behandlung bis zu etwa 70 % steigen kann. Ärzte nutzen CT-Angiographie zur Darstellung der Aorta und Bluttests wie D‑Dimer und Entzündungsmarker, um Gerinnung und Immunaktivität einzuschätzen. Doch die Beschwerden der Patienten sind oft unspezifisch, die körperliche Untersuchung kann täuschend normal sein und CT-Bilder können durch Bewegung oder Artefakte abgeschwächt sein, sodass etwa einer von drei Fällen in der Routine zunächst übersehen wird.
Was aktuelle KI‑Werkzeuge verpassen
In den letzten Jahren sind leistungsfähige Bilderkennungssysteme entstanden, die CT- oder Röntgenbilder auf Anzeichen von Aortenrissen durchsuchen können. Die meisten dieser Werkzeuge betrachten jedoch nur die Bilder und ignorieren Blutwerte, oder sie fügen separate Datenströme lediglich zusammen, ohne wirklich zu lernen, wie sie interagieren. Das steht im Widerspruch zur Denkweise von Klinikern: Sie verknüpfen visuell Gesehenes mit Laborwerten und der Anamnese des Patienten. Einfaches "Stapeln" von Bildmerkmalen und Laborzahlen kann die Situation sogar verschlechtern, weil Bluttestdaten rauschbehaftet, unvollständig und mathematisch verflochten sind. Viele KI‑Modelle arbeiten zudem als Blackboxen und liefern ein Urteil, ohne den zugrunde liegenden Denkprozess offen zu legen, was Notfallärzte zögern lässt, ihnen bei lebensbedrohlichen Entscheidungen zu vertrauen.
Ein neuer Weg, Scans und Blutwerte zu verschmelzen
Die Autoren entwickelten ein multimodales Multi-Skalen-Fusionsmodell (MMMF), das das Denken erfahrener Radiologen und Kardiologen nachahmen soll. Zuerst betrachtet ein zweigleisiger Bildencoder die CT-Angiographie auf zwei Detailebenen: Große Bildausschnitte erfassen die Gesamtform und den Verlauf der Aorta, während kleinere Ausschnitte feine Details wie winzige intimale Risse oder kleine Blutansammlungen in der Wand fokussieren. Parallel dazu werden zentrale Blutindikatoren — einschließlich D‑Dimer und einem Panel von Entzündungsmarkern, abgeleitet aus Leukozytenzahlen und Thrombozyten — in numerische Merkmalspunkte umgewandelt. Diese Bild‑ und Labormerkmale werden zu Knoten in einer graphähnlichen Struktur, in der ein fortschrittliches graphneuronales Netzwerk "Nachrichten" zwischen ihnen übermittelt und lernt, wie bestimmte Blutmuster subtile Bildbefunde verstärken oder widersprechen.
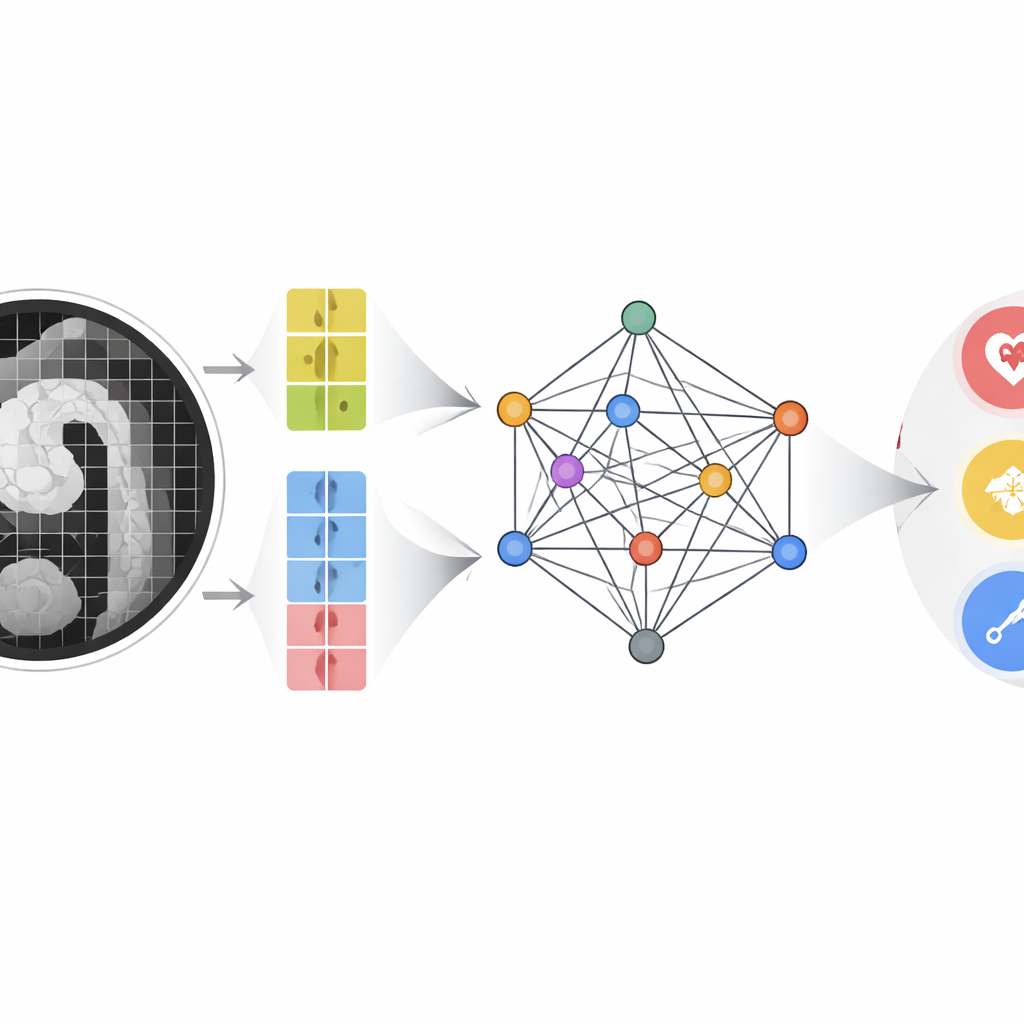
Wie gut das System abschneidet
Das Team trainierte und testete das MMMF‑Modell an CT‑Scans und zeitgleich erhobenen Bluttests von 493 Patientinnen und Patienten, die zwischen 2019 und 2024 untersucht wurden; dabei waren bestätigte AAS verschiedenster Typen sowie Nicht‑AAS‑Kontrollen vertreten. Sie verglichen ihren Ansatz mit bekannten reinen Bildmodellen, reinen Laborwertmodellen und mehreren modernen multimodalen Systemen, die ursprünglich für die Kombination von Bildern und Text entwickelt wurden. In Genauigkeit, Präzision, Sensitivität und F1‑Score lag das MMMF‑Modell vorn. Die Gesamtfläche unter der ROC‑Kurve überstieg 0,9, was eine starke Fähigkeit anzeigt, normale Aorten, klassische Dissekatioen mit Beteiligung der aufsteigenden oder absteigenden Aorta und atypische Formen zu unterscheiden. Bilddaten blieben die stärkste einzelne Informationsquelle, aber eine sorgfältig strukturierte Fusion mit Laborwerten brachte insbesondere bei schwierigen oder grenzwertigen Fällen einen messbaren Gewinn. Ablationsstudien zeigten, dass zwei Elemente entscheidend waren: der duale Skalen‑Bildpfad und der transformerbasierte Graph, der langreichweitige Beziehungen zwischen Merkmalen modelliert.
Auf dem Weg zu einer Partnerschaft zwischen Ärzten und Maschinen
Über die reinen Kennzahlen hinaus ist ein wesentlicher Beitrag dieser Arbeit die Betonung von Zusammenarbeit statt Ersatz. Das System ist besonders gut darin, offensichtliche Normalbefunde und klar erkrankte atypische Fälle schnell auszusortieren und fungiert damit als eine Art intelligenter Erstfilter. Ebenso wichtig: Es erkennt, wenn seine eigene Sicherheit gering ist — häufig bei Fällen, die auch menschliche Expertinnen und Experten als schwierig empfinden, etwa frühe oder mildere Formen einer Dissektion — und markiert diese Patienten zur dringenden Nachprüfung, für zusätzliche Bildgebung oder zur Rücksprache mit Seniorärztinnen und -ärzten. Im Kern zeigt die Studie, dass wenn Bilddetails und Blutkleinode in einer strukturierten, klinisch inspirierten Weise verflochten werden, KI sowohl die frühe Diagnose des akuten Aortensyndroms schärfen als auch ein Sicherheitsnetz gegen übersehene Notfälle bieten kann, wobei die Ärztinnen und Ärzte die endgültigen Entscheidungen behalten.
Zitation: Yang, Z., Xu, S., Wang, B. et al. AI-driven diagnosis of acute aortic syndrome based on multi-modal information fusion. Sci Rep 16, 8332 (2026). https://doi.org/10.1038/s41598-026-39111-4
Schlüsselwörter: akutes Aortensyndrom, Aortendissektion, medizinische KI, multimodale Diagnose, graphneuronales Netzwerk