Clear Sky Science · de
EEG-basierte Prädiktoren der motorischen Erholung während immersiver VR-BCI-Rehabilitation
Bewegung nach dem Schlaganfall neu verkabeln
Bei vielen Menschen, die einen Schlaganfall überleben, bleibt eine Schwäche in Arm oder Hand über Jahre bestehen und schränkt alltägliche Tätigkeiten wie Ankleiden, Kochen oder Tippen stillschweigend ein. Diese Studie untersucht eine hochmoderne Form der Rehabilitation, die Gehirn–Computer-Schnittstellen mit immersiver Virtual Reality kombiniert, um dem Gehirn zu helfen, das Bewegen einer geschwächten Extremität neu zu erlernen. Indem die Forscher die Hirnwellen genau betrachteten, stellten sie eine praktische Frage: Können frühe Gehirnaktivitäten während dieses Trainings vorhersagen, wer am ehesten die Bewegungsfähigkeit zurückgewinnt?
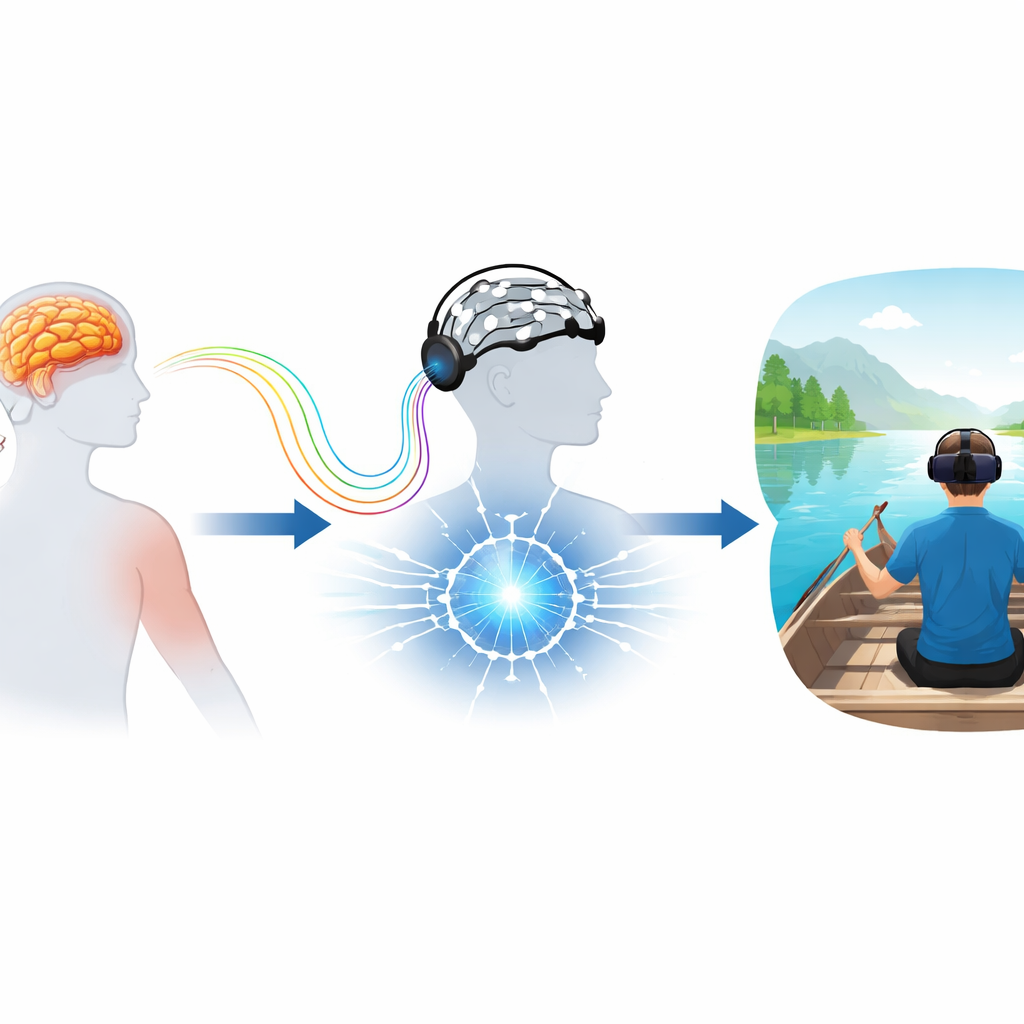
Das Gehirn in einem virtuellen Boot trainieren
Das Team arbeitete mit Erwachsenen, die nach einem ersten Schlaganfall eine chronische Armschwäche hatten. Über vier Wochen absolvierten die Teilnehmenden der Experimentalgruppe bis zu zwölf Sitzungen in einem immersiven Virtual-Reality-Spiel namens NeuRow. Mit einem Head-Mounted-Display und einer Kappe zur Aufzeichnung der Hirnsignale saßen sie in einem virtuellen Boot und sollten sich vorstellen, mit dem linken oder rechten Arm zu rudern, während sie eine virtuelle Avatarbewegung beobachteten. Wenn die Gehirnaktivität mit der beabsichtigten Bewegung übereinstimmte, bewegte sich das virtuelle Boot vorwärts und kleine Vibrationen in den Handcontrollern verstärkten die Aktion, wodurch eine enge Schleife zwischen mentaler Anstrengung und sensorischem Feedback entstand. Eine Kontrollgruppe erhielt stattdessen zusätzliche konventionelle Therapie anstelle dieses VR-basierten Trainings.
Dem Rhythmus des Gehirns lauschen
Die Forscher konzentrierten sich auf ein spezifisches Muster der elektrischen Hirnaktivität, genannt ereignisbezogene Desynchronisation (event-related desynchronization, ERD). Wenn wir eine Bewegung planen oder vorstellen, schwächen sich bestimmte rhythmische Hirnwellen, besonders über den motorischen Arealen, vorübergehend ab. Dieser Rückgang der Rhythmusstärke wird als Ausdruck der Aktivierung motorischer Netzwerke interpretiert. Mit Elektroenzephalographie (EEG) maß das Team, wie stark diese Rhythmen beim Vorstellen des Ruderns abnahmen und wie dieses Muster über beide Gehirnhälften verteilt war. Außerdem bestimmten sie für jede Person individualisierte Frequenzbänder, um der Tatsache Rechnung zu tragen, dass ein Schlaganfall diese Rhythmen auf subtile Weise verschieben kann.
Schlaganfallüberlebende und unverletzte Gehirne im Vergleich
Um zu verstehen, wie „gesunde“ motorbezogene Hirnrhythmen in derselben VR-Aufgabe aussehen, verglichen die Autorinnen und Autoren die Schlaganfallgruppe mit einer Referenzgruppe von 35 Personen ohne Schlaganfall, die zuvor dasselbe NeuRow-Protokoll durchlaufen hatten. Über den zentralen, motorisch relevanten Ableitungsorten zeigten Schlaganfallüberlebende deutlich schwächere ERD als die Referenzgruppe, und das Gleichgewicht zwischen linker und rechter Hirnhälfte war weniger stabil. Anders ausgedrückt: Ihre Gehirne aktivierten motorische Netzwerke schwächer und weniger konsistent während der vorgestellten Bewegung. Innerhalb der Schlaganfallgruppe veränderten sich diese ERD-Muster jedoch über die 12 Trainingseinheiten hinweg nur wenig, und die Lateralisierung, also das Links-Rechts-Gleichgewicht, blieb im Zeitverlauf relativ flach.
Basislinien-Hirnsignale als Kristallkugel
Obwohl die allgemeine Stärke der ERD durch das Training nicht stetig zunahm, erwies sich das zu Beginn gemessene ERD als hochgradig aussagekräftig. Mit statistischen Modellen, die individuelle Unterschiede berücksichtigten, fanden die Forschenden heraus, dass das Baseline-ERD in den betroffenen motorischen Arealen vorhersagte, wie sehr sich die Armfunktion, gemessen mit dem standardisierten Fugl–Meyer-Test, nach der Intervention verbessern würde. Teilnehmende, deren Gehirne zu Beginn einen stärkeren motorbezogenen Abfall der rhythmischen Aktivität zeigten, gewannen über den Monat hinweg tendenziell mehr Beweglichkeit. Im Gegensatz dazu war die Veränderung der ERD von Sitzung zu Sitzung ein weitaus schwächerer Prädiktor für die Erholung. Die Studie deutete außerdem an, dass insbesondere bei ischämischem Schlaganfall eine erhöhte Aktivität in der nicht geschädigten Hemisphäre kompensatorisch wirken könnte, wobei stärkere ipsilaterale ERD mit besseren Ergebnissen verbunden war.
Was das für die künftige Schlaganfallversorgung bedeutet
Für Patientinnen, Patienten und Therapeutinnen und Therapeuten deuten diese Befunde darauf hin, dass eine einfache EEG-Messung, die früh im VR–BCI-Training durchgeführt wird, einen starken Hinweis darauf geben kann, wer am meisten profitieren wird. Anstatt Wochen zu warten, um zu sehen, ob sich die Funktion verbessert, könnten Therapeutinnen und Therapeuten künftig Basislinien-Hirnrhythmen nutzen, um Behandlungspläne zu personalisieren, die Intensität anzupassen oder Therapien zu kombinieren bei denen, deren Gehirne eine schwächere Aktivierung zeigen. Die Studie unterstreicht auch, dass Erholung bei langfristigen Schlaganfallfolgen komplex ist: Klinische Verbesserungen traten zwar auf, die Hirnsignale folgten jedoch keiner einfachen, kontinuierlich ansteigenden Entwicklung. Indem sie jedoch zeigen, dass prä-trainings-Hirnrhythmen mit späteren Verbesserungen verknüpft sind, rückt diese Arbeit das Feld näher zu einer prädiktiven, maßgeschneiderten Neurorehabilitation, die die verbleibende Plastizität des Gehirns nutzt.
Zitation: Valente, M., Branco, D., Bermúdez i Badia, S. et al. EEG-based predictors of motor recovery during immersive VR-BCI rehabilitation. Sci Rep 16, 7870 (2026). https://doi.org/10.1038/s41598-026-39106-1
Schlüsselwörter: Schlaganfall-Rehabilitation, Virtual-Reality-Training, Gehirn-Computer-Schnittstelle, EEG-Biomarker, motorische Erholung