Clear Sky Science · de
Dlgap2-Mangel stört die synaptische Homöostase, indem er in einem valproinsäureinduzierten autismusähnlichen Modell den ubiquitinvermittelten Abbau von Itsn1 fördert
Warum ein gebräuchliches Medikament und die Gehirnverdrahtung wichtig sind
Valproinsäure ist ein seit langem verwendetes Medikament gegen Epilepsie und Stimmungsstörungen, steht aber bei Einnahme während der Schwangerschaft in Verbindung mit einem erhöhten Autismusrisiko bei Kindern. Diese Studie stellt eine dringende Frage für Familien und Ärztinnen: Was bewirkt dieses Medikament genau an der Verdrahtung des sich entwickelnden Gehirns? Indem die Forschenden Veränderungen bis hin zu spezifischen Molekülen an Synapsen — den Kommunikationsstellen zwischen Nervenzellen — zurückverfolgen, decken sie eine neue Abfolge von Ereignissen auf, die autismusähnliche Verhaltensweisen erklären und auf mögliche künftige Behandlungsansätze hinweisen kann. 
Über Arten hinweg nach gemeinsamen Schwachstellen suchen
Um verlässliche Hinweise zu finden, verließen sich die Forschenden nicht auf nur ein Tiermodell. Sie verglichen Gehirne bzw. gehirnähnliche Gewebe von menschlichen kortikalen Organoiden, Affen, Ratten und Mäusen, die vor der Geburt Valproinsäure ausgesetzt waren. Mithilfe groß angelegter Gen- und Proteinumfragen identifizierten sie eine kleine Gruppe von Genen, die in all diesen Systemen verändert waren und mit Synapsen sowie der Myelinisierung von Nervenfasern in Verbindung standen. Auffällig war eines besonders: Dlgap2, ein Gerüstprotein, das die postsynaptische Seite erregender Synapsen organisiert. Bei Mäusen mit pränataler Valproinsäureexposition sanken die Dlgap2-Spiegel in der Großhirnrinde und genauer in winzigen synaptischen Kompartimenten, was darauf hindeutet, dass dieses strukturstabilisierende Molekül eine zentrale Verlustquelle bei der Medikamentenexposition ist.
Von molekularen Veränderungen zu Verhaltensänderungen
Die Autorinnen und Autoren fragten dann, ob allein der Verlust von Dlgap2 ausreicht, die Gehirnfunktion zu stören. Sie verwendeten Viren, die kurze Haarnadel-RNA (shRNA) trugen, um Dlgap2 in kultivierten Mausneuronen und in neugeborenen Mäusen zu reduzieren. In der Zellkultur bildeten Neuronen mit reduziertem Dlgap2 kürzere Verästelungen und wiesen weniger postsynaptische Puncta auf — Anzeichen abgeschwächter Verbindungen. Im lebenden Tier führte die zielgerichtete Herunterregulierung von Dlgap2 im Gehirn zu autismusähnlichen Verhaltensweisen: junge männliche Mäuse hatten Schwierigkeiten, den Ort einer versteckten Plattform in einem Wassertest zu erlernen, und zeigten in einem Drei-Kammer-Test vermindertes Interesse an Sozialpartnern und an sozialer Neuheit. Diese Veränderungen ähneln den Lern- und Sozialdefiziten bei valproinsäureexponierten Tieren und untermauern die Auffassung, dass der Verlust von Dlgap2 nicht nur eine Begleiterscheinung, sondern ein Treiber veränderter Verhaltensweisen ist.
Ein anfälliger Partner an der Synapse
Um zu verstehen, wie sich Dlgap2-Verlust auf die Synapse auswirkt, betrachteten die Forschenden die Proteine der postsynaptischen Dichte genauer — das dichte molekulare Polster, das chemische Signale empfängt. Mithilfe der Proteomik stellten sie fest, dass die Reduktion von Dlgap2 die Häufigkeit hunderter synaptischer Proteine veränderte, besonders solcher, die an der Organisation von Synapsen und an der Wiederverwertung von Vesikeln durch Endozytose beteiligt sind. Ein Protein, Intersectin‑1 (Itsn1), fiel besonders stark ab. Weitere biochemische Arbeiten zeigten, dass Dlgap2 und Itsn1 in den gleichen Proteinkomplexen in synapsenreichen Fraktionen vorkommen und beide zu Genen gehören, die mit Autismus in Verbindung gebracht werden. Das deutet auf eine gezielte regulatorische Partnerschaft der beiden Moleküle in der dicht gepackten Synapsenlandschaft hin. 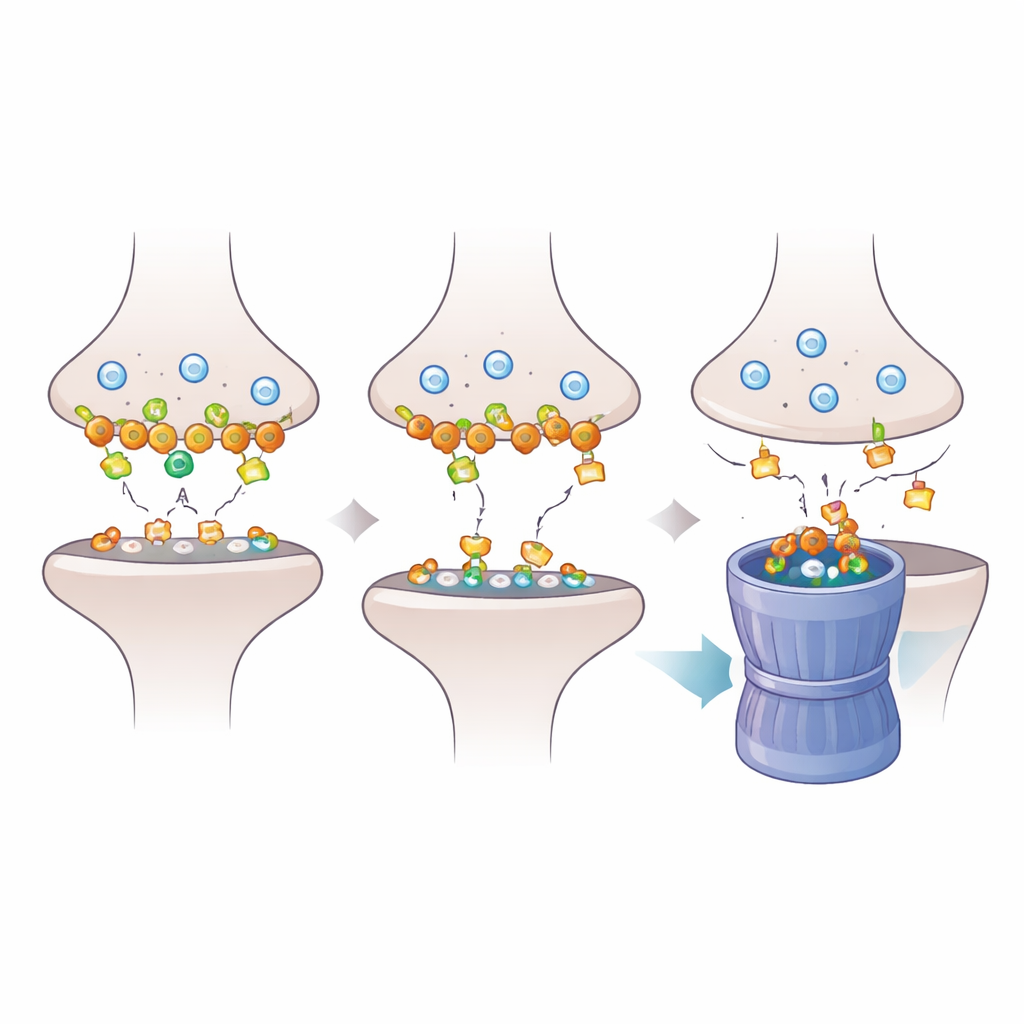
Ein verborgener Entsorgungsweg kommt ans Licht
Die Forschenden fragten als Nächstes, warum Itsn1-Spiegel fallen, wenn Dlgap2 fehlt. Sie beobachteten, dass in synaptischen Kompartimenten durch Dlgap2-Knockdown eine Form der Proteinmarkierung auslöste — K48-gekettete Ubiquitinierung —, die Proteine für den Abbau durch das zelluläre Proteasom markiert. Die Blockade dieses Entsorgungssystems mit dem Wirkstoff MG132 verhinderte den Verlust von Itsn1, was darauf hindeutet, dass Dlgap2 normalerweise Itsn1 davor schützt, markiert und zerstört zu werden. Ohne Dlgap2 wird Itsn1 vermehrt markiert, dem Proteasom zugeführt und aus Synapsen dezimiert, was Endozytose-Recycling und das Gleichgewicht synaptischer Aktivität untergräbt. Die Arbeit legt nahe, dass schon subtile Veränderungen der Abbaurate wichtiger Proteine Synapsen während der Gehirnentwicklung destabilisieren können.
Was das für Autismus und künftige Behandlungen bedeutet
In der Summe schlägt die Studie eine einfache, aber aussagekräftige Idee für ein allgemeines Publikum vor: Pränatale Exposition gegenüber Valproinsäure kann ein strukturelles „Stütz“-Protein (Dlgap2) an Synapsen schwächen. Geht diese Stütze verloren, gerät ihr Partnerprotein (Itsn1) stärker ins Visier der zellulären Müllentsorgung, was zu fehlerhafter Wiederverwertung synaptischer Komponenten und letztlich zu fehlverdrahteten Schaltkreisen und autismusähnlichem Verhalten bei Mäusen führt. Zwar tragen viele Gene und Umweltfaktoren zu Autismus bei, doch die Dlgap2–Itsn1-Achse bietet eine konkrete molekulare Kette von pränataler Medikamentenexposition bis zu veränderter Gehirnfunktion. Langfristig könnten Strategien, die diese Partnerschaft bewahren oder die Proteinentsorgungsmaschine an Synapsen feinjustieren, helfen, entwickelnde Gehirne vor ähnlichen Störungen zu schützen.
Zitation: Guo, X., Zhang, L. & Zhuang, K. Dlgap2 deficiency disrupts synaptic homeostasis by promoting ubiquitin-mediated Itsn1 degradation in a valproic acid-induced autism-like model. Sci Rep 16, 8305 (2026). https://doi.org/10.1038/s41598-026-39099-x
Schlüsselwörter: Valproinsäure und Schwangerschaft, synaptische Gerüstproteine, Mechanismen des Autismus-Spektrums, Ubiquitin-Proteasom-Weg, Mausmodelle für Autismus